TFOS DEWS II - Pathophysiology 病態生理
Anthony J. Bron, FRCOph, FMedSci, Cintia S. de Paiva, MD, PhD1, Sunil K. Chauhan, DVM, PhD1, Stefano Bonini, MD, Eric E. Gabison, MD, Sandeep Jain, MD, Erich Knop, MD, PhD, Maria Markoulli, PhD, MOptom, Yoko Ogawa, MD, Victor Perez, MD, Yuichi Uchino, MD, PhD, Norihiko Yokoi, MD, PhD, Driss Zoukhri, PhD, David A. Sullivan, PhD
TFOS DEWS Ⅱの病態生理に関する分科委員会は、過去の査読された文献に基づいて、ドライアイの中心的メカニズムは涙液の蒸発によって誘発される涙液の高浸透圧であり、これがこの疾患の特徴であると結論づけた。涙液の高浸透圧は、直接的にまたは炎症を惹起させることによって眼表面に傷害を与えることになる。ドライアイの悪循環として説明される、このサイクルを図2の中央に示した。
涙液分泌減少型ドライアイと涙液蒸発亢進型ドライアイといった、2種類のタイプのドライアイが認識されている。涙液分泌減少型ドライアイでは、眼表面からの涙液の蒸発が正常であるといった中で涙腺からの涙液分泌が減少することによって、涙液の高浸透圧が生じる。涙液蒸発亢進型ドライアイでは、涙腺からの涙液分泌が正常であるといった中で涙液層からの涙液の蒸発が亢進することによって、涙液の高浸透圧が生じる。涙液の浸透圧は、涙液分泌減少型ドライアイにしても涙液蒸発亢進型ドライアイにしても涙液の蒸発作用の影響を受けていることより、涙液の高浸透圧は眼表面からの蒸発に起因して生じており、その意味で、ドライアイのあらゆる形態が涙液蒸発型であると言える。言い換えれば、涙液蒸発亢進型ドライアイは、涙液の蒸発過多状態であると考えられる。
ドライアイでは、涙液の高浸透圧が眼表面の上皮細胞内のシグナル伝達事象のカスケードの引き金となっていると考えられており、これは炎症性メディエーターとプロテアーゼの放出につながっている。そのようなメディエーターは、涙液の高浸透圧性それ自体とともに、杯細胞や上皮細胞の減少、上皮糖衣への傷害を引き起こすと理解されている。眼表面に遊走してきた活性化T細胞からの炎症性メディエーターは傷害をさらに増長させる。その最終的な結果は、ドライアイに特徴的な点状表層(角膜)上皮症であり、角膜表面の数か所で早期の涙液層破綻をもたらす涙液層の不安定性である。この涙液層破綻は、涙液の高浸透圧を悪化かつ増幅させて、眼表面の傷害を招く悪循環を完成させるものである。最終的にこれは疾患の自己永続性につながると考えられている。
涙液層の不安定性は、眼表面に影響を及ぼす条件(眼球乾燥症、眼アレルギー、点眼薬の防腐剤の使用、コンタクトレンズの装用を含む)によって、涙液の高浸透圧が生じる以前に始まっていることがある。このような場合、最初は局所的に涙液層破綻を観察することとなるが、重症度が増していくと、ある時点において涙液メニスカスから採取したものに高浸透圧性が検出可能となることより、早期の涙液層破綻には涙液の高浸透圧といったものが基本的に存在するということが仮説とされている。これは、眼表面に関連したドライアイの形態として表されている。マイボーム腺機能不全関連のドライアイでは、涙液の高浸透圧は涙液油層の欠乏に起因する。涙液分泌減少型ドライアイでは、その疾患の経過中に早期の涙液層破綻が生じた後に、二次的にドライアイにおける涙液蒸発の要素が加わってくることもありうる。
涙液分泌減少型ドライアイには様々な原因が存在している。それは、涙液層の健常性を維持するために不可欠な涙腺への知覚神経をブロックすることによるものである。両眼に対する点眼麻酔は、涙液分泌の減少と瞬目回数の減少を引き起こす可能性がある。涙液の反射性分泌のブロックが原因のドライアイには、点眼麻酔薬の慢性的な乱用、三叉神経の損傷、レーシック手術を含む屈折矯正手術によって引き起こされる可能性がある。涙嚢への涙液の通過傷害は、鼻涙管閉塞によって生じている可能性もあり、これは、トラコーマ、眼類天疱瘡、多形性紅斑、移植片対宿主病、化学眼外傷などのあらゆる形態の瘢痕性結膜疾患で起こり得ることである。また、抗ヒスタミン薬、β遮断薬、鎮痙薬、利尿薬、一部の向精神薬などの全身投与されているいくつかの薬剤は、涙液分泌の低下を引き起こす可能性があり、ドライアイの危険因子となっている。また、涙液分泌率は人生の後半において低下していく。
西欧諸国において、涙液分泌減少型ドライアイの最も主要な原因は、涙腺の炎症性浸潤であり、その中には、シェーグレン症候群のような自己免疫疾患に関連するドライアイの中でも最も重症度の高いものや、非シェーグレン症候群のような比較的重症度の低いものがある。炎症は、涙腺腺房や導管上皮細胞の機能不全や破壊、可逆性ではあるものの神経分泌のブロックを引き起こす原因となる。ムスカリン(muscarine 3:M3)受容体に対する血中抗体もまた受容体のブロックを引き起こしうる。組織中のアンドロゲンの(ホルモン)レベルが低いと涙腺の炎症を起こしやすくする可能性がある。
眼表面における上皮の傷害や不十分な糖衣、涙液量の減少や杯細胞ムチンの減少は、摩擦による傷害や摩擦関連の自覚症状の増加を引き起こす。ドライアイによって引き起こされる涙液の高浸透圧や上皮の傷害は、角膜神経終末を刺激して、眼不快感や瞬目回数の増加をもたらし、涙液の代償性の反射性分泌を引き起こす可能性もある。この涙液の代償性の分泌は、涙腺機能が潜在的に正常である涙液蒸発亢進型ドライアイにおいて生じる可能性が高い。
涙液蒸発亢進型ドライアイの主な原因であるマイボーム腺機能不全について、その病因と機序を模式図(シェーマ)として図3に示す。マイボーム腺機能不全の機序に関しては、まだ不明な点が多いが、この図は現在の見解の要約を試みるものである。この図の上部では、マイボーム腺分泌の低下をもたらすマイボーム腺機能不全において、瘢痕性と非瘢痕性といった2つの形態をとるマイボーム腺機能不全の病因について示している。
年齢とともに、特に50歳を過ぎてくると、マイボーム腺の脱落が増加して、これは原発性のマイボーム腺機能不全の発症と相関している。生物学的に利用可能なアンドロゲンの減少はこれらの現象に関与している。青年期においては、シス‐レチノイン酸による尋常性痤瘡の治療は、マイボーム腺の腺萎縮やマイボーム腺機能不全を誘発する可能性があるが、高年齢層においては、アンドロゲン受容体の感受性低下や遮断(ブロック)は、マイボーム腺機能不全の徴候を誘発する可能性がある。抗緑内障薬であるピロカルピンやチモロールもまた、ヒトのマイボーム腺上皮細胞に直接作用する可能性があり、これはマイボーム腺の形態、生存、増殖能力に影響を及ぼし、おそらくマイボーム腺機能不全を促進するものと考えられる。ポリ塩化ビフェニルは、マイボーム腺機能不全様の特徴を含む全身性疾患を引き起こす可能性がある。酒さ性痤瘡、アトピー性皮膚炎、脂漏性皮膚炎、乾癬のようなある種の皮膚疾患は、非瘢痕性マイボーム腺機能不全と関連しているが、トラコーマ、多形性紅斑、天疱瘡のような瘢痕性結膜疾患は、瘢痕性マイボーム腺機能不全を引き起こす。
非瘢痕性マイボーム腺機能不全における重要な事象は、導管末端における過角化であり、これはマイボーム腺の導管閉塞、導管拡張、腺萎縮をもたらす。その後に、腺開口部の消失が起こることもある。マイボーム腺の閉塞は、分泌物の粘調度を増加させるような油成分の変化によって悪化するとされている。マイボーム腺機能不全に罹患したマイボーム腺周囲の炎症性変化の程度については、報告によって様々であるが、眼瞼縁において炎症が存在するのは常識とされている。炎症性メディエーターや脂質は、涙液中や眼表面上に放出されて、上皮に傷害を引き起こす。瘢痕性マイボーム腺機能不全においては、結膜の粘膜下組織の瘢痕化は、マイボーム腺開口部、導管末端、粘膜皮膚移行部を後方に移動させて、眼瞼縁後方を横切って瞼板のところまで至ることがあり、そこで狭窄や変位を生じた導管からはもはや涙液油層へ効率的に分泌物を供給することができない。マイボーム腺の分泌低下や油成分の変化は、涙液層の不安定性、涙液蒸発量の増加、そして最終的には、ドライアイを引き起こす可能性がある。腺分泌低下を示すマイボーム腺機能不全においては、その自覚症状は局所的な眼瞼疾患自体、眼表面の傷害を伴う眼瞼疾患、そして涙液蒸発亢進型ドライアイから生じるものであると考えられている。
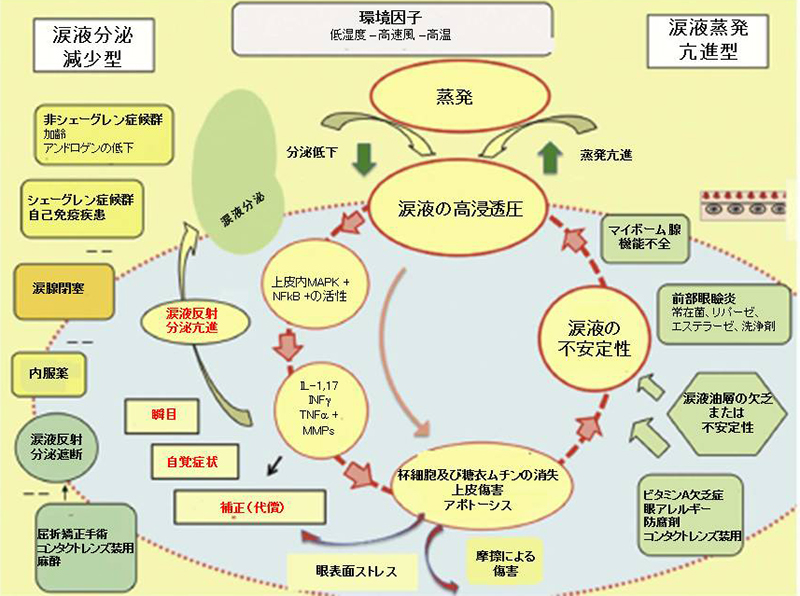 図2 ドライアイの病態生理
図2 ドライアイの病態生理
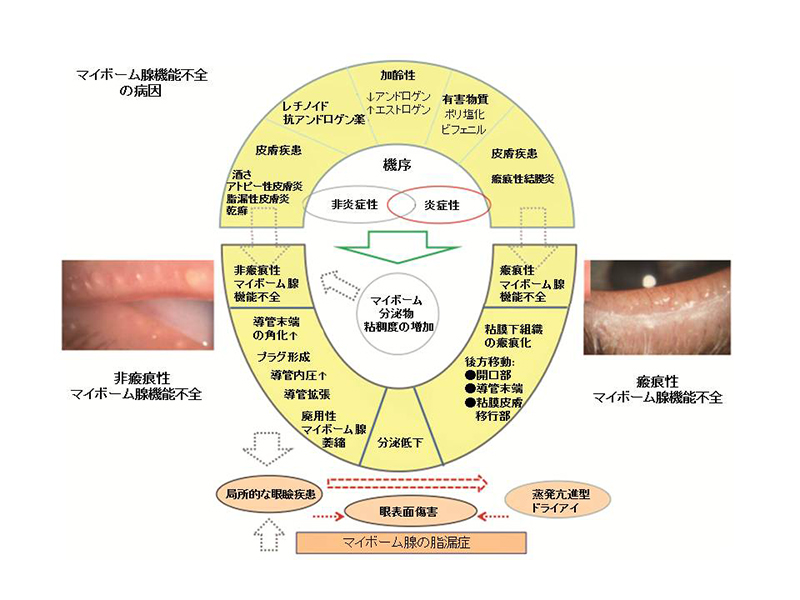 図3 マイボーム機能不全の病態生理
図3 マイボーム機能不全の病態生理
Questo sito utilizza cookie di profilazione propri e di siti terzi. Se vuoi saperne di più consula la cookie policy. Chiudendo questo banner acconsenti all'uso dei cookie. GrazieOk
Leggi di più
 図2 ドライアイの病態生理
図2 ドライアイの病態生理
 図3 マイボーム機能不全の病態生理
図3 マイボーム機能不全の病態生理