TFOS DEWS II - Informe de gestión y tratamiento
Lyndon Jones, FCOptom, PhD1,'Correspondence information about the author FCOptom, PhD Lyndon JonesEmail the author FCOptom, PhD Lyndon Jones, Laura E. Downie, BOptom, PhD, , Donald Korb, OD, Jose M. Benitez-del-Castillo, MD, PhD, Reza Dana, MD, Sophie X. Deng, MD, PhD, Pham N. Dong, MD, Gerd Geerling, MD, FEBO, Richard Yudi Hida, MD, Yang Liu, MD, Kyoung Yul Seo, MD, PhD, Joseph Tauber, MD, Tais H. Wakamatsu, MD, PhD, Jianjiang Xu, MD, PhD, James S. Wolffsohn, FCOptom, PhD, Jennifer P. Craig, MCOptom, PhD
Translated into Spanish by Allergan
| Descargue esta sección en formato PDF |
RESUMEN
Los miembros del Subcomité de gestión y tratamiento realizaron una revisión basada en evidencias de los tratamientos actuales para el ojo seco y las opciones para su gestión. Las opciones de gestión revisadas en detalle incluían tratamientos para la insuficiencia lagrimal y las anomalías de los párpados, así como medicamentos antiinflamatorios, enfoques quirúrgicos, modificaciones de la dieta, consideraciones medioambientales y tratamientos complementarios. Tras esta amplia revisión, quedó claro que muchos de los tratamientos disponibles para la gestión de la enfermedad del ojo seco carecen de la evidencia de nivel 1 necesaria para respaldar su recomendación, a menudo debido a una falta de enmascaramiento, aleatorización o controles apropiados y, en algunos casos, debido a problemas de sesgo en la selección o un tamaño muestral inadecuado.
Reflexionando sobre la evidencia disponible, se derivó un algoritmo de gestión estratificado que presenta un enfoque gradual para implementar las distintas opciones de gestión y tratamiento de acuerdo con la gravedad de la enfermedad. Mientras que este ejercicio indicaba que la diferenciación entre ojo seco con déficit acuoso y ojo seco evaporativo era esencial a la hora de seleccionar la estrategia de gestión más apropiada, también puso de relieve los desafíos, basándose en la evidencia limitada que hay disponible actualmente, para la predicción de beneficios relativos de opciones de gestión concretas y la gestión de los dos subtipos de enfermedad de ojo seco.
Se requieren más evidencias que respalden la introducción y el uso continuado de muchas de las opciones de tratamiento actualmente disponibles para gestionar la enfermedad del ojo seco, así como para informar los puntos iniciales apropiados de tratamiento y entender la especificidad del tratamiento en relación con el subtipo de enfermedad de ojo seco.
© 2017 Elsevier Inc. Todos los derechos reservados.
Palabras clave: Enfermedad del ojo seco, Taller sobre el ojo seco, Gestión. TFOS DEWS II, Tratamiento
Este informe resume las opciones de gestión y tratamiento para el tratamiento de la enfermedad del ojo seco (EOS). Los objetivos de este comité eran revisar los métodos apropiados para el manejo de la EOS y recomendar una estrategia para su aplicación clínica, basándose en una revisión basada en evidencias de la literatura. El nivel de evidencia para respaldar los datos de la literatura se evalúa de acuerdo con las directrices de las Prácticas Preferidas de la Academia Americana de Oftalmología (American Academy of Ophthalmology Preferred Practices) (Tabla 1).
Siempre que fuera posible, se han utilizado publicaciones con revisión científica externa, en lugar de resúmenes, para guiar las recomendaciones para la gestión. En algunos casos, debido a la reciente introducción del tratamiento a debate, no fue posible. El informe fue revisado por todos los miembros del subcomité y se entregó a todos los miembros del 2.º Taller sobre el Ojo Seco de la Sociedad para la Película Lagrimal y la Superficie Ocular (Tear Film and Ocular Surface Society’s Dry Eye Workshop II [TFOS DEWS II]) para que realizaran una crítica constructiva. Los comentarios y las revisiones sugeridos fueron comentados por los miembros del subcomité e incorporados al informe cuando se consideraron apropiados por consenso.
Los avances en nuestra comprensión de los factores de riesgo, la etiología y la fisiopatología de la EOS han contribuido a la evolución de las estrategias de tratamiento con el tiempo. En los años posteriores a la publicación del Informe de gestión y tratamiento original del Taller sobre el Ojo Seco de TFOS (DEWS) [1], se ha venido produciendo una creciente concienciación de la importante contribución de la disfunción de la glándula de Meibomio (DGM) tanto a los síntomas como a los signos de EOS [2].
Mientras en otras secciones de este informe se discute más en detalle la clasificación [3], es importante advertir que las etiquetas de diagnóstico tienen una influencia significativa en la posterior gestión y tratamiento. Por lo general, se cree que, en lugar de representar dos categorías distintas, la mayoría de las personas con síntomas relacionados con la enfermedad de la superficie ocular (ESO) sufren combinaciones variables tanto de fisiología anómala de la glándula de Meibomio (que provoca EOS evaporativa) como infraproducción de lágrimas (que provoca una EOS con déficit acuoso). Las estimaciones del grado de solapamiento entre estas dos categorías han ido desde el 30 al 70 %, pero se trata de estimaciones realizadas por médicos aplicando el criterio clínico. Un estudio publicado determinó que los pacientes con EOS tenían una probabilidad dos o tres veces superior de que se les subclasificara como con ojo seco evaporativo (OSE) que con ojo seco con déficit acuoso (OSDA), y más del 30 % de los pacientes tenía ambos tipos de EOS [4].
Con independencia de la exactitud de estas cifras, los médicos de todo el mundo reconocen la necesidad de tratar a los “pacientes de ojo seco” de un modo integral, teniendo en cuenta sus síntomas, la fisiología de la glándula de Meibomio, la calidad y la cantidad lipídica de la película lagrimal, la permeabilidad del orificio de la glándula de Meibomio y también la producción, la pérdida y la evacuación de lágrimas [5 - 9]. Si solo una de estas dos amplias categorías de ESO (OSE y OSDA) se aborda terapéuticamente, los pacientes pueden seguir sufriendo síntomas y referir insatisfacción con el tratamiento prescrito. Es necesario diagnosticar primero a los pacientes de forma precisa, con respecto al reconocimiento de la principal causa tras su EOS, antes de elaborar un plan de tratamiento. En el informe sobre metodología de diagnóstico de TFOS DEWS II se da más información sobre el diagnóstico de la ESO [10].
2. Tratamientos para la insuficiencia lagrimal volver arriba
Históricamente, se ha considerado que la EOS se debe en gran medida a la insuficiencia lagrimal y se ha tratado prescribiendo productos sustitutivos de las lágrimas o conservando las lágrimas mediante tapones lagrimales. Los tratamientos más recientes han incluido el uso de métodos para estimular las lágrimas.
2.1. Enfoques para la sustitución de lágrimas
La sustitución de lágrimas por lubricantes oculares se considera tradicionalmente un pilar del tratamiento de la EOS y existen numeras fórmulas tópicas disponibles. Los productos de venta sin receta suelen denominarse “lágrimas artificiales” que, tal como su nombre sugiere, intentan sustituir y/o suplementar la película lagrimal natural. Sin embargo, estos productos no actúan sobre la fisiopatología subyacente de la EOS, y los mecanismos de cualquier acción paliativa son generalmente poco conocidos.
2.1.1. Sustitutos de lágrima artificial
Los sustitutos de las lágrimas constan de diversos productos, que normalmente tienen como objetivo actuar sobre una o varias de las capas de la película lagrimal. La amplia variedad de propiedades de estos lubricantes oculares se ha revisado en otros trabajos [11 - 15].
Los lubricantes oculares se consideran en gran medida seguros, aunque existen algunos efectos secundarios notificados, principalmente visión borrosa, diversos niveles de “molestias oculares” y sensación de tener cuerpos extraños [16]. Existen relativamente pocos ensayos controlados aleatorizados (ECA) que han comparado la relativa superioridad de un determinado producto de venta sin receta con otros productos para el tratamiento de la EOS [17]. Una reciente revisión sistemática de Cochrane, que perseguía evaluar el efecto de los productos de suplemento lagrimal de venta sin receta para el tratamiento de la EOS, incluía 43 ensayos controlados aleatorizados que habían comparado las fórmulas de lágrima artificial con la ausencia de tratamiento o con un placebo [16]. La medida principal del resultado fueron los síntomas notificados por el paciente. Los autores notificaron que la calidad general de la evidencia era baja para las distintas fórmulas de suplementos lagrimales comparadas en la revisión, y concluyeron que, aunque las lágrimas artificiales podían ser eficaces para el tratamiento de la EOS, seguía existiendo una necesidad de futuras investigaciones para permitir extraer conclusiones sólidas acerca de la efectividad de fórmulas individuales de lágrima artificial de venta sin receta.
2.1.1.1. Suplementación acuosa.
Mientras que la osmolaridad, la viscosidad y el pH de las fórmulas de los lubricantes oculares pueden variar, la mayoría comparten similitudes en sus principales componentes. El componente más abundante en los colirios lubricantes es la base acuosa. Para mejorar la lubricación y prolongar el tiempo de conservación en la superficie ocular, con frecuencia se incorporan agentes optimizadores de la viscosidad.
2.1.1.1.1. Agentes optimizadores de la viscosidad.
Los agentes que optimizan la viscosidad utilizados en las fórmulas de los suplementos lagrimales incluyen carbómero 940 (ácido poliacrílico), carboximetilcelulosa (CMC), dextrano, ácido hialurónico (AH), guar-HP, hidroxipropilmetilcelulosa (HPMC), alcohol polivinílico (APV), polivinilpirrolidona (PVP) y polietilenglicol.
Los optimizadores de la viscosidad se consideran beneficiosos para la superficie ocular en la EOS por medio de diversos mecanismos notificados. Estos incluyen el aumento del grosor de la película lagrimal, la protección frente a la desecación, el fomento de la conservación de lágrimas en la superficie ocular, la protección de la superficie ocular, el mantenimiento del grosor fisiológico corneal, la mejora de la densidad de las células calciformes y el alivio de los síntomas del ojo seco [18,19]. Aunque existen puntuaciones de fórmulas y productos disponibles, que varían de una región a otra, no parece que haya ninguna diferencia sustancial entre ellas en cuanto a efectividad [16,20]. Sin embargo, las diferencias en la viscosidad de las gotas pueden influir en su uso. Los colirios con una gran viscosidad pueden aumentar el tiempo de conservación en la superficie ocular, pero también pueden causar trastornos visuales temporales y provocar residuos no deseados en los párpados y las pestañas, que provocan una tolerancia y un cumplimiento menores. Los colirios con una viscosidad muy alta suelen recomendarse para su uso durante la noche, mientras que los colirios con una baja densidad se utilizan durante el día.
2.1.1.1.1.1. Carboximetilcelulosa (CMC)
La CMC es un derivado de la celulosa con grupos carboximetil y se forma a partir de las paredes celulares de las plantas. A menudo se utiliza como su sal de sodio, carboximetilcelulosa sódica, y también se conoce como carmelosa sódica. Se trata de un agente optimizador de la viscosidad utilizado con mucha frecuencia en lubricantes oculares, así como en productos farmacéuticos, alimentos y cosméticos [21].
La CMC se puede unir a las células epiteliales corneales fomentando la curación de las células epiteliales [22,23]. Los productos a base de CMC han demostrado tener éxito en la gestión del ojo seco de leve a moderado en diversos estudios [24 - 26].
2.1.1.1.1.2. Hidroxipropilmetilcelulosa (HPMC)
Los éteres de celulosa son polisacáridos viscolásticos que aumentan la viscosidad de las lágrimas. De estos, la HPMC se ha utilizado durante muchos años en lubricantes artificiales y sigue siendo uno de los ingredientes más habituales. Está disponible en una amplia variedad de concentraciones (de 0,2 a 0,8 %) y se utiliza en combinación con muchos otros componentes en los lubricantes oculares modernos [11,14]. Debido a esta amplia disponibilidad y uso a lo largo de muchos años, múltiples estudios han explorado su potencial para gestionar pacientes con EOS [16]. Una revisión de su rendimiento muestra que es un lubricante seguro y eficaz para aquellos con síntomas de bajos a moderados de EOS [16].
2.1.1.1.1.3. Ácido hialurónico (AH)
El ácido hialurónico (AH), también conocido como hialurón y hialuronato sódico, es un glicosaminoglucuronano no sulfatado aniónico presente de forma natural que se distribuye ampliamente por los tejidos conectivos, epiteliales y neuronales. Puede ser muy grande, con un peso molecular que a menudo llega a varios millones de Daltons. El AH es un componente importante del cartílago articular y se encuentra con abundancia en los líquidos sinoviales alrededor de las articulaciones, en el humor vítreo y el humor acuoso [27]. Diversos estudios han demostrado su capacidad para unirse a las células de la superficie ocular y sus potenciales propiedades curativas de heridas [28 - 33].
El AH se utiliza en diversos suplementos lagrimales para aumentar la viscosidad y proporcionar una mejor lubricación. El AH muestra propiedades no newtonianas de pseudoplasticidad [34], donde la viscosidad varía con la tensión de rotura. Para fórmulas basadas en AH, la viscosidad disminuye a medida que aumenta la tensión de rotura, al igual que ocurre durante un parpadeo.
A medida que el catálogo de productos comerciales que contienen AH crece, se han publicado cada vez más estudios clínicos de nivel 1 y 2 que demuestran la buena tolerabilidad y la capacidad para mejorar los síntomas del ojo seco [35 - 42].
2.1.1.1.1.4. Combinación de CMC y AH
Tal como se describía previamente, existen diversas publicaciones que respaldan el uso de colirios tópicos que contienen CMC o AH para el tratamiento de la EOS. Optive Fusion™ (Allergan, Parkway Parsippany, NJ, EE. UU.) contiene una combinación de CMC al 0,5 %y AH al 0,1 % en una única fórmula tópica. En un estudio murino del ojo seco, los ratones que recibieron CMC + AH por vía tópica mostraron una tinción corneal con fluoresceína significativamente menor y una mayor densidad de las células calciformes que los ratones tratados con gotas que contenían solo CMC o AH [43]. En un estudio de 3 meses con doble enmascaramiento y multicéntrico, en el que participaban 305 sujetos con EOS, la combinación comercialmente disponible de CMC + AH mejoró los síntomas y signos de EOS en mayor grado que una fórmula tópica disponible en el mercado basada solo en CMC [44]
2.1.1.1.1.5. Guar hidroxipropil (guar-HP)
Guar-HP es un espesante polimérico no iónico que puede proporcionar rápidamente gran viscosidad mediante un proceso dependiente del pH [45,46]. Un producto basado en guar-HP, Systane® ULTRA (Alcon, Ft Worth, TX, EE. UU.), incluye dos demulcentes (polietilenglicol 400 y propilenglicol) y sorbitol, y está tamponado con borato, lo que produce un gel de borato/guar-HP reticulado en la botella [47]. El pH de Systane ULTRA es 7,9 pero cuando se instila sobre la superficie ocular, la reducción del pH y la disolución de la concentración de sorbitol aumentan la densidad de las reticulaciones de borato/guar-hidroxipropil, produciendo un gel de muy baja viscosidad [45].
Los productos basados en guar-HP han demostrado mejorar los síntomas del ojo seco, aumentar el grosor de la capa de mucosa, reducir la inflamación y proteger la superficie ocular [47 - 53].
2.1.1.1.1.6. Combinación de AH y guar-HP
Una fórmula que contiene los demulcentes propilenglicol y polietilenglicol y una combinación de polímero doble de AH y guar-HP (Systane® ULTRA HYDRATION; Alcon, Ft Worth, TX, EE. UU.) ha demostrado ser eficaz en la protección de la desecación y en la conservación de la superficie ocular en un estudio de laboratorio basado en células corneales [54].
2.1.1.1.1.7. Hidroxipropilcelulosa
El concepto de usar una inserción de hidroxipropilcelulosa soluble en la superficie ocular para tratar la EOS fue aprobada en primer lugar por la Administración de Alimentos y Medicamentos (Food and Drug Administration, FDA) hace más de 30 años, pero durante muchos años se dejó de lado debido a las molestias y a una eficacia relativamente baja [55]. La versión más reciente de este concepto es LACRISERT™ (Bausch & Lomb, Rochester, NY, EE. UU.), que es un lubricante estéril, translúcido, con forma de vara, soluble en agua, sin conservantes y de liberación lenta que se coloca en el fondo de saco conjuntivo inferior con la ayuda de un aplicador reutilizable. Comienza a ablandarse en cuestión de minutos, disolviéndose en el curso de unas 12 horas y espesando la película lagrimal precorneal. Se recomienda para su uso en pacientes con EOS de moderada a grave, se introduce normalmente una vez al día y está contraindicado en pacientes que son hipersensibles a la hidroxipropilcelulosa.
Se realizó un estudio multicéntrico abierto, de 2 visitas y de 4 semanas de duración para determinar la aceptabilidad de las inserciones en 520 sujetos con EOS [56]. Se produjo una mejoría significativa de los síntomas, la tinción corneal con ?uoresceína, la tinción conjuntival y el volumen lagrimal. Los usuarios de lentes de contacto notificaron mejoras significativas similares a las de los no usuarios de lentes de contacto. Las complicaciones notificadas incluyen visión borrosa temporal, molestias o irritación (en particular si no se coloca debidamente), expulsión en pacientes con fondos de saco conjuntivales poco profundos y rigidez o viscosidad de las pestañas.
2.1.1.1.2. Agentes osmóticos.
El informe original de TFOS DEWS atrajo la atención sobre la importancia de la osmolaridad lagrimal, lo que demuestra que un aumento de la osmolaridad lagrimal está asociado a la EOS [57]. Desde ese momento, numerosos estudios han examinado el vínculo entre la EOS y la osmolaridad. Sin embargo, relativamente pocos estudios han investigado el impacto de los colirios hipoosmolares o hiperosmolares de suplementos lagrimales sobre la osmolaridad de las lágrimas y cualquier mejora de la EOS. Gilbard realizó diversos experimentos que muestran que el uso de un lubricante ocular hipoosmolar podría revertir diversos cambios en la superficie ocular (densidad de las células calciformes notablemente reducida) inducidos en un modelo de ojo seco en conejos [58 - 60]. Dos estudios más recientes que utilizan lubricantes oculares hipotónicos basados en ácido hialurónico demostraron una mejora tanto de los síntomas como de diversos signos de EOS [61,62]. Sin embargo, se necesitan más estudios que vinculen la capacidad de los lubricantes de reducir la osmolaridad de la película lagrimal y su impacto sobre los síntomas y los signos de EOS.
Diversos estudios publicados demuestran el potencial de mejorar la osmolaridad lagrimal con tratamientos para la EOS [63 - 70], incluso en ausencia de un cambio [71,72] o en asociación con resultados negativos [68,73,74] en otros cuadros clínicos.
Desde la publicación del primer informe de TFOS DEWS, se han publicado varios ejemplos de tratamiento de seguimiento del ojo seco con osmolaridad lagrimal. Un estudio que investiga los efectos de un tratamiento de combinación de metilprednisolona y AH al 0,1 % sin conservante cuatro veces al día demostró una reducción significativa de la osmolaridad a las ocho semanas, que igualó las reducciones significativas de IL-1β y IL-8, así como del tiempo de desintegración lagrimal (TDL) y de las tinciones corneal y conjuntival [75]. Los autores concluyeron que medir los cambios en los niveles de citocina y en la osmolaridad lagrimal podría evaluar objetivamente los efectos antiinflamatorios de la metilprednisolona tópica aplicada en el tratamiento de pacientes con síndrome de ojo seco de moderado a grave. Un ensayo similar de ocho semanas de un HA modificado aplicado tres veces al día provocó mejoras significativas en la puntuación del índice de enfermedad de la superficie ocular (IESO), el TDL, la densidad de las células calciformes conjuntivales, el daño corneal y conjuntival y la osmolaridad lagrimal [66].
La osmolaridad lagrimal también ha demostrado igualar las mejoras en los síntomas y signos del ojo seco que se producen cuando los pacientes utilizan ciclosporina tópica [63,76,77], AH [40,66,78 - 80], colirios osmoprotectores [40,67,69] y colirios de PEG/guar-HP [81].
2.1.1.1.3. Osmoprotectores.
Los osmoprotectores (p. ej., L-carnitina y betaína) son un grupo de solutos compatibles que protegen las células bajo un estrés osmótico extremo equilibrando la presión osmótica sin alterar el metabolismo celular [82 - 85]. El efecto osmoprotector depende de la cantidad de captación del fármaco y de su tiempo de conservación, y las combinaciones de osmoprotectores con distintas cinéticas farmacéuticas puede funcionar mejor que los osmoprotectores individuales.
Existen distintos estudios que demuestran que los osmoprotectores tienen un efecto beneficioso en el tratamiento de la EOS. Un estudio in vitro demostró que los osmoprotectores L-carnitina y eritritol pueden proteger células humanas epiteliales corneales cultivadas frente a condiciones de hiperosmolaridad mediante la reducción de los niveles de proteína quinasa activada por mitógenos [86]. Los osmoprotectores también mostraron propiedades de supresión de la inflamación bajo estrés hiperosmótico [87]. Un estudio del ojo seco realizado en ratones demostró que los osmoprotectores pueden reducir la tinción corneal, reducir la apoptosis celular y las citocinas inflamatorias, y aumentar el número de células calciformes [88].
La trehalosa es un disacárido producido de forma natural, presente en numerosas especies de no mamíferos, que permite que las células sobrevivan en entornos desfavorables. Está implicada en la anhidrobiosis, que se relaciona con la capacidad de plantas y animales para resistir periodos prolongados de desecación. Tiene capacidades muy elevadas de retención de agua y tiene propiedades tanto de bioprotección como de osmoprotección [89 - 94]. Estudios in vitro e in vivo han demostrado que la trehalosa protege las células corneales frente a la desecación [95], además de proteger las células corneales y conjuntivales frente a la apoptosis [90,96]. La trehalosa también ha demostrado proteger las células corneales frente al daño oxidativo inducido por la luz ultravioleta (UV) mediante la aceleración de la curación corneal [97] y la reducción de las citocinas inflamatorias conjuntivales en un modelo murino de EOS [92]. También ayuda a restablecer el equilibrio osmótico en la superficie ocular, además de prevenir la desnaturalización de las dos capas lipídicas de la membrana celular y las proteínas para mantener la homeostasis de las células corneales [90 - 92].
Se ha desarrollado una nueva fórmula de colirio que contiene tanto AH como trehalosa para aprovechar las propiedades lubricantes del AH y las propiedades bioprotectoras de la trehalosa [98].
2.1.1.1.4. Antioxidantes.
La presencia de radicales libres de oxígeno en las lágrimas de pacientes con EOS [99] ha provocado la exploración de la posible aplicación de antioxidantes para la gestión de la EOS.
En un estudio en animales, la acetilcisteína tópica, un aminoácido con actividad antioxidante, disminuyó la expresión de las citocinas inflamatorias en los tejidos de la superficie ocular de un modelo murino de EOS, pero no alteró la tinción corneal [100]. Otro colirio antioxidante, la vitamina A (palmitato de retinol), demostró tener efectos significativos en la mejora de la visión borrosa, el TDL, la puntuación de Schirmer y los hallazgos de la citología de impresión en sujetos con EOS en un estudio prospectivo aleatorizado controlado con grupos paralelos [101]. Sin embargo, también se sabe que los metabolitos de la vitamina A causan DGM en modelos animales, incluidas queratinización glandular y atrofia, calidad reducida del meibum, reducción del tiempo de desintegración de la película lagrimal, aumento de la osmolaridad de la película lagrimal y síntomas de ojo seco (se incluyen detalles adicionales en el Informe sobre ojo seco iatrogénico de TFOS DEWS II) [102].
Un estudio en el que se utilizaron células humanas epiteliales estratificadas del limbo corneal mostró que varios antioxidantes pueden ser beneficiosos si se incorporan a lubricantes oculares tópicos [103]. La quercetina, el galato de epigalocatequina, el galato de n-propilo y el ácido gálico mostraron una buena biodisponibilidad, fueron eficaces en la neutralización de especies reactivas de oxígeno y podrían ser eficaces en la protección del epitelio corneal contra el daño oxidativo.
Visomitin es el primer fármaco registrado con propiedades antioxidantes que actúa sobre el estrés oxidativo en las mitocondrias, y está disponible como fármaco tópico en Rusia. Un recuente estudio clínico, multicéntrico, aleatorizado, con doble enmascaramiento y controlado con placebo demostró que un ciclo de 6 semanas de Visomitin tópica redujo la tinción corneal y mejoró los síntomas de 240 sujetos con EOS [104]. Puede actuar reduciendo las especias reactivas de oxígeno en la superficie ocular, pero se requieren otros estudios para confirmarlo.
La selenoproteína P (SelP) es una glicoproteína secretada que participa en el transporte o el almacenamiento de selenio y está implicada en el metabolismo del estrés oxidativo [105]. En un modelo de ojo seco en ratas, el uso de colirios SelP durante 3 semanas suprimió los marcadores de estrés oxidativo, y las lágrimas recogidas de sujetos humanos con tinción corneal tuvieron un menor contenido en SelP [106]. Los autores concluyeron que la SelP lagrimal es una molécula clave para proteger la superficie ocular contra el estrés oxidativo medioambiental.
2.1.1.1.5. Conservantes.
Los lubricantes artificiales multidosis normalmente requieren un conservante para prevenir el crecimiento microbiano, mientras que los viales de dosis unitaria que se desechan después de un solo uso no lo requieren. Sin embargo, los viales de dosis unitaria son más caros y pueden ser más difíciles de abrir para personas menos diestras. Ahora hay disponibles varios productos nuevos que utilizan dispensadores con válvulas unidireccionales incorporadas que permiten que los frascos multidosis no lleven conservantes.
Se está prestando cada vez más atención a la relación entre el uso crónico de tratamientos tópicos, como los medicamentos para el glaucoma, y la ESO. Ahora se sabe bien que la exposición crónica de la superficie ocular a conservantes induce toxicidad y cambios adversos en la superficie ocular [107 - 112]. El cloruro de benzalconio (CBA) es el conservante utilizado con más frecuencia en los preparados de colirios. Existen numerosos estudios in vitro e in vivo que demuestran que el CAB puede inducir la apoptosis de las células epiteliales corneales y conjuntivales, daño en los nervios corneales, retraso de la curación de las heridas de la córnea, intervenir en la estabilidad de la película lagrimal y causar pérdida de células calciformes [113 - 115]. En un estudio in vitro, una concentración de CAB superior al 0,005 % alteró de forma significativa la distribución de los lípidos y afectó a la morfología de la capa lipídica de las lágrimas [116]. Existe suficiente evidencia para confirmar que los pacientes con EOS, en especial aquellos con EOS grave que requieren la administración frecuente de lubricantes o que utilizan lubricantes oculares junto con otros tratamientos tópicos crónicos como los medicamentos para el glaucoma, deben evitar el uso de lubricantes oculares conservados con CAB [102].
Para evitar problemas relacionados con una exposición a largo plazo a conservantes, se han desarrollado nuevas variantes de conservantes diseñados para tener un menor impacto sobre la superficie ocular, incluidos conservantes oxidativos (clorito sódico: Purite® y OcuPure™, y perborato sódico: GenAqua™), polyquaternium-1 (Polyquad®) y Sof-Zia™. El clorito sódico se degrada en iones de cloro y agua tras la exposición a la luz UV después de su instilación, y el perborato sódico se convierte en agua y oxígeno al entrar en contacto con la película lagrimal. Algunos informes sugieren que incluso los llamados “conservantes que desaparecen” pueden mostrar algunos efectos negativos sobre la superficie ocular [117]. Por lo tanto, los colirios sin conservantes pueden ser una mejor opción para pacientes que presentan afecciones preexistentes en la superficie ocular y/o necesitan la instilación frecuente de colirios. Los colirios sin conservantes han demostrado una mayor efectividad que los colirios con conservantes en la reducción de la inflamación de la superficie ocular y en el aumento del contenido antioxidante en las lágrimas de pacientes con EOS [118]. Pese a que todos los productos recetados para el ojo seco se suministrarían en dosis unitarias o en frascos de dosis múltiples sin conservantes, las consideraciones de los costes y la disponibilidad del producto suelen impedir que esto sea posible.
Puede encontrar información adicional sobre las interacciones de los conservantes con la superficie ocular en el informe del ojo seco iatrogénico de TFOS DEWS II [102].
2.1.1.1.6. Agentes inactivos
2.1.1.1.6.1. Tampones
La estabilidad de las soluciones oftalmológicas más frecuentemente utilizadas se controla en gran medida mediante el pH de su entorno. Además de la estabilidad, el pH puede influir en la comodidad, la seguridad y la actividad del producto. Los productos para el ojo seco contienen una amplia variedad de tampones para controlar el pH, incluidos tampones de citrato, fosfato y borato. La concentración de estos tampones es crítica, ya que existen informes de calcificación corneal tras el uso prolongado de un producto para el ojo seco conservado con niveles elevados de fosfato de calcio [119].
El borato sódico, también conocido como tetraborato de sodio o tetraborato disódico, es una sal de ácido bórico. El ácido bórico es un ácido débil que se usa como agente tamponador en algunos colirios. Algunos estudios han demostrado que las soluciones multiusos (multipurpose solutions, MPS) para lentes de contacto con ácido bórico pueden presentar citotoxicidad del epitelio corneal [120]. Sin embargo, otros estudios han indicado que los defectos en la superficie ocular inducidos por MPS pueden atribuirse equivocadamente al ácido bórico [121]. Los posibles beneficios o ausencia de beneficios del ácido bórico o, de hecho, de cualquier otro tampón en las fórmulas para el ojo seco siguen sin estar claros. Sin embargo, cabe destacar que el ácido bórico en el pH de la superficie ocular también actúa como un agente de reticulación y se une electroestáticamente al guar hidroxipropil (guar-HP) [122,123].
2.1.1.1.6.2. Excipientes
Debido a la delicada estructura de los tejidos oculares, la cantidad de excipientes aceptables para los colirios es limitada y consiste principalmente en agentes isotónicos iónicos y no iónicos. Existen limitados estudios publicados relativos al efecto de los excipientes sobre la superficie ocular [124]. Recientemente, el macrogolglicerol hidroxiestearato 40 (MGH 40) se ha utilizado como colirio sin conservantes como excipiente solubilizante. Un estudio en animales demostró que el MGH 40 se tolera bien [125]. Sin embargo, un estudio in vitro previo reveló que el MGH 40 desencadena efectos perjudiciales en las células, similares a los que se observan con BAK [126]. Otro estudio examinó el papel de poli(L-lisina)-injerto-poli(- etilenglicol) (PLL-g-PEG) como un nuevo excipiente polimérico en lágrimas artificiales [127]. Un estudio realizado en un único centro demostró que PLL-g-PEG fue efectivo en la prolongación del tiempo de desintegración no invasiva (TDNI) 15 min después de su instilación [127]. Se necesitan más estudios para aclarar el impacto de varios excipientes venosos en la superficie ocular.
2.1.1.1.6.3. Electrolitos
La película lagrimal precorneal es un entorno complejo que es rico en electrolitos, incluidos sodio, potasio, cloro, magnesio y calcio [128]. Al secretarse, las lágrimas son isotónicas con respecto al suero, aunque las proporciones de iones son algo distintas, especialmente en el caso del potasio [129,130]. En la EOS, la concentración de electrolitos de la película lagrimal normalmente aumenta debido a la evaporación y/o la reducción de la producción acuosa.
Los electrolitos desempeñan papeles críticos en la homeostasis de la superficie ocular. Las observaciones sugieren que los niveles relativamente elevados de potasio en las lágrimas pueden desempeñar un papel en la protección del epitelio corneal frente a la radiación UV-B [131,132]. El potasio también ha demostrado ser necesario para mantener un grosor corneal normal, y las disminuciones en las concentraciones de potasio pueden provocar un aumento del grosor corneal [133]. Finalmente, la calidad de la integridad de la superficie epitelial de la córnea y las propiedades de dispersión de la luz, medidas por microscopía especular, han demostrado depender de la composición electrolítica [134]. La superficie epitelial se mantiene mejor con una solución tamponada que contiene potasio, calcio, magnesio, fosfato, bicarbonato y cloruro sódico, siendo el potasio especialmente importante [134].
Determinados lubricantes lagrimales, como TheraTears® (Akorn Lake Forrest, IL, EE. UU) y Bion® Tears (Alcon Ft Worth, TX, EE. UU.), tienen un perfil electrolítico diseñado para imitar el de la película lagrimal. Algunas de las sales o electrolitos utilizados con frecuencia incluyen cloruro sódico, cloruro potásico, cloruro cálcico, cloruro de magnesio, cloruro de zinc, borato sódico, fosfato sódico y ácido bórico. El bicarbonato sódico se utiliza para tamponar la solución, pero también tiene un efecto electrolítico [135]. Una fórmula de lágrima artificial basada en electrolitos ha demostrado aumentar la densidad de las células calciformes de la conjuntiva y el contenido de glucógeno corneal en un modelo de EOS en conejos [58,59]. Otros estudios han demostrado que la inclusión de potasio con AH en lágrimas artificiales no conservadas mejora la curación de las heridas corneales en un modelo de raspado mecánico [33]. La adición de bicarbonato a una solución de lágrima artificial isotónica sin conservantes fomenta la recuperación del epitelio corneal en comparación con la misma solución tamponada con borato o sin tampón [136]. Un estudio independiente demostró que la adición de bicarbonato fomentó la recuperación de la función de la barrera epitelial y mantuvo la ultraestructura corneal y de la capa de mucina normales tras la exposición a CAB [137]. Hasta la fecha, los estudios in vitro, en animales y en humanos sugerirían que determinadas composiciones electrolíticas podrían tener un papel positivo en la gestión de la EOS con lubricantes oculares.
2.1.1.2. Suplementación lipídica.
La capa lipídica de la película lagrimal tiene un papel importante que desempeñar en la prevención de la evaporación lagrimal [138]. Los colirios que contienen lípidos están creciendo tanto en disponibilidad como en popularidad [139,140], principalmente debido al aumento de la atención que se presta a la DGM y al déficit lipídico. Varios aceites, como los aceites minerales y los fosfolípidos, se han incorporado a las fórmulas de lubricantes oculares para ayudar a restaurar la capa lipídica de la película lagrimal [46,141,142].
Los colirios que contienen lípidos están formulados como emulsiones. Las emulsiones se definen como líquidos no solubles que se dispersan finamente en otro líquido, como el aceite y el agua [143]. Las emulsiones no se forman fácilmente y se deben aplicar fuerzas de transversales y presiones extremas con los surfactantes apropiados para vencer los efectos de la tensión superficial [143].
Las emulsiones se pueden categorizar a grandes rasgos en tres tipos, basándose en el tamaño de las gotas. Las macroemulsiones contienen gotas de más de 100 nm (nm), las nanoemulsiones tienen gotas de entre 10 y 100 nm y las microemulsiones tienen gotas <10 nm. Las macroemulsiones están turbias debido a que los tamaños de las gotas grandes dispersan la luz y estas formulaciones pueden inducir la vista borrosa cuando se aplica por vía tópica. Con el fin de minimizar el posible efecto de visión borrosa, así como la estabilidad de la emulsión tras la instilación, se pueden manipular el tamaño de las partículas, la concentración y el tipo de lípidos. Los tamaños de gotas más pequeños minimizan la visión borrosa tras su instilación debido a que las estructuras de las gotas son menores que las longitudes de onda visibles, lo que evita la dispersión. Diversos productos comerciales emplean emulsiones metaestables para minimizar el tiempo de visión borrosa y, por tanto, requieren invertir o agitar el frasco de dispensación para mejorar la uniformidad de la emulsión antes de la aplicación.
Las emulsiones han demostrado administrar de manera eficaz fármacos lipofílicos, una tarea que supone todo un reto para los portadores con base acuosa. Los nuevos enfoques emplean vectores catiónicos de aceite en agua submicrométricos, que explotan las cargas negativas en la capa de mucina [144]. Una nanoemulsión catiónica de aceite en agua es una fórmula bifásica que consta de nanogotas de aceite con carga positiva (la fase de aceite) dispersadas en agua (la fase continua). La carga positiva de las nanogotas de aceite se genera mediante un surfactante catiónico que se localiza en la interfaz de aceite. Se cree que cuando se instila un colirio de nanoemulsión catiónico de aceite en agua, la atracción electrostática resultante entre las nanogotas de aceite con carga positiva y las mucinas de la superficie ocular con carga negativa se manifiesta macroscópicamente como una mejora en el tiempo de conservación y dispersión [145]. Es posible que esta interacción pudiera modificarse mediante la exposición a las proteínas catiónicas de la película lagrimal, como la lisozima. Esto es especialmente interesante para pacientes con DGM que muestran una estabilidad reducida de la película lagrimal, debido a un déficit lipídico en las lágrimas [146].
Incluso en ausencia de un principio activo, se ha observado que estas nanoemulsiones catiónicas de aceite con agua en estudios preclínicos tienen un beneficio inherente sobre la superficie ocular [147,148]. Cationorm® (Santen Osaka, Japón) es una emulsión catiónica sin conservantes indicada para el tratamiento de la EOS. El excipiente catiónico es el cloruro de cetalconio, un derivado alquilo de CAB que es lipofílico [148]. Algunos estudios han demostrado que las células humanas epiteliales de la córnea en cultivo toleran bien Cationorm [146,149]. Sin embargo, otro estudio in vitro demostró que las córneas tratadas con Cationorm sufrieron pérdida epitelial y alteraciones en el estroma corneal superficial [150]. Los nanosistemas con base catiónica que incorporal quitosano proporcionan estrategias de formulación alternativas [151 - 153].
La seguridad a largo plazo de nanoemulsiones en la superficie ocular está pendiente de ser evaluada.
2.1.1.2.1. Tipología y propiedades de los lípidos.
Se han propuesto distintos tipos de lípidos para intentar imitar de la mejor forma posible el meibum natural. Los tipos de lípidos utilizados incluyen fosfolípidos, ácidos grasos saturados e insaturados y triglicéridos [154]. Se han descrito el aceite mineral en distintas concentraciones, el aceite de ricino, el aceite de oliva, los carbómeros de glicerina, el aceite de coco, el aceite de soja y la lecitina, en combinación con varios agentes emulsionantes y surfactantes [155 - 161].
Los fosfolípidos pueden ser neutros (zwitteriónicos), con carga negativa (aniónicos) o con carga positiva (catiónicos). Systane® Balance (Alcon Ft Worth, TX, EE. UU.) contiene un fosfolípido polar, DMPG (dimiristoilfosfatidilglicerol). Existen muchos tipos de fosfolípidos y, de ellos, dos se encuentran con frecuencia en las lágrimas: la fosfatidilcolina y la fosfatidiletanolamina [162 - 172]. Parece que los fosfolípidos aniónicos tienen una mayor capacidad para incrementar el grosor de la capa lipídica que los compuestos zwitteriónicos [46,173]. Una posible razón es que los fosfolípidos con carga negativa contribuyen a una interfaz estable entre los lípidos no polares en la superficie de la capa acuosa hidrofílica [174]. Esto respalda la hipótesis de que los fosfolípidos polares ayudan a formar una película lipídica multimodular estable [175]. Algunos estudios sugieren que los niveles de los dos fosfolípidos polares son más bajos en personas con deficiencias en la película lagrimal [165,176]. Puede obtener información adicional en el informe sobre la película lagrimal de TFOS DEWS II [128].
Múltiples estudios han demostrado que las gotas basadas en lípidos y los sprays liposomales pueden mejorar los signos y síntomas del ojo seco (Tabla 2) [65,141,142,177 - 182].
2.1.2. Sustitutos biológicos de las lágrimas
2.1.2.1. Suero autólogo
2.1.2.1.1. Introducción.
El suero es el componente líquido de la sangre que permanece tras la coagulación. Aunque el uso tópico de suero autólogo se describió en la década de 1970 [183], solo se popularizó para la gestión de la ESO grave tal como la asociada a las quemaduras químicas, al síndrome de Stevens-Johnson y, muchos años más tarde, al síndrome de Sjögren [184 - 186]. Más recientemente, también se ha utilizado para varias afecciones menos graves, incluido el posoperatorio de queratomileusis epitelial con láser (LASEK), las erosiones corneales recurrentes, las pústulas supurantes de aparición tardía tras trabeculectomía o necrosis tisular tras implantes orbitales [187 - 189].
La ventaja del suero autólogo es que muchas de sus características bioquímicas, incluidos pH, contenido de nutrientes, vitaminas, ?bronectina y factores de crecimiento como el factor de crecimiento epitelial (epithelial growth factor, EGF) o el factor de crecimiento nervioso (nerve growth factor, NGF) son similares a las de las lágrimas humanas. Varios estudios in vitro e in vivo han demostrado que el suero y otros derivados de la sangre mejoran la curación de las heridas epiteliales de la córnea, probablemente debido a estos factores [190 - 194]. También se determinó que el suero inhibe la liberación de citocinas inflamatorias y aumenta el número de células calciformes y la expresión de mucina en la conjuntiva en una serie de casos clínicos [195,196]. Pese a que la evidencia procedente de cultivos celulares sugiere que la proliferación de células epiteliales mejora al diluir el suero al 20 % o menos, la migración epitelial y la deposición de la matriz extracelular de los fibroblastomas se estimulan mejor mediante el suero al 50 % o al 100 % [197,198].
En un modelo en conejos, el suero sin diluir fue más eficaz que el suero diluido en la curación de una herida epitelial en la córnea [192].
El uso extendido del suero autólogo está limitado por diversos factores. La producción de productos sanguíneos está regulada por las leyes nacionales, que pueden diferir de forma significativa entre los distintos países. Con frecuencia, el proceso lo llevan a cabo bancos de sangre y está centralizado en algunos países [199 - 201]. Los requisitos legales incluyen pruebas serológicas para el virus de la inmunodeficiencia humana (VIH), hepatitis y otras afecciones, con el fin de minimizar el riesgo de transmisión de la enfermedad durante la producción o la aplicación por parte de otros, ya que se han observado enfermedades infecciosas sistémicas desconocidas en más del 3 % de los productos sanguíneos [202]. La composición del suero autólogo obtenido depende de una serie de parámetros de producción, incluidos el tiempo de coagulación y centrifugado, y es probable que tenga un impacto sobre los efectos epiteliotróficos [203]. Con el fin de optimizar el producto y permitir la comparación entre estudios, los protocolos estandarizados se han desarrollado conforme al trabajo in vitro, pero aún no se han confirmado en estudios clínicos comparativos [204,205]. Además de los problemas de producción, existen otros problemas alrededor del almacenamiento del producto, ya que la concentración de factores de crecimiento en suero autólogo puede reducirse con el tiempo cuando se almacena a 4 °C [206]. A -20 °C, se determinó que la composición del suero autólogo era estable durante un máximo de 9 meses [206 - 208]. Finalmente, el coste del suero autólogo puede demostrar ser problemático, ya que un suministro de 2-3 meses puede suponer un coste de cientos de dólares [205,209]. Sin embargo, a pesar de estos problemas, el uso de suero autólogo en la gestión de la ESO ha ganado una amplia aceptación y, por tanto, puede lograr una mayor cobertura sanitaria en el futuro [210,211].
2.1.2.1.2. Rendimiento clínico.
En un estudio de Nivel 3, el suero autólogo mejoró los síntomas del ojo seco en 10 días en aproximadamente el 60 % de los pacientes y en dos meses en el 79 % de los pacientes [212]. Este efecto se mantuvo durante un seguimiento de 12 meses utilizando diversos cuestionarios sobre los síntomas.
La Tabla 3 presenta los resultados de 14 estudios clínicos (niveles 1 y 2) sobre la eficacia del suero autólogo en la EOS [184,186,213 - 224]. En estos estudios, 349 pacientes recibieron suero autólogo, principalmente para EOS grave debido al síndrome de Sjögren. Entre estos estudios existe una variación notable para los parámetros de producción, criterios de valoración, frecuencia posológica y duración del tratamiento. En todos estos ensayos, con un seguimiento de entre 1 y 3 meses, los sujetos mostraron una mejoría significativa de los síntomas, con una respuesta positiva en un 60-80 % de los pacientes. Normalmente, el TDL, la tinción corneal con ?uoresceína y la citología de impresión conjuntival mejoraron, mientras que las puntuaciones Schirmer permanecieron sin cambios.
Estudios prospectivos y comparativos de cohortes demostraron que el suero autólogo era menos eficaz en pacientes que fueron clasificados históricamente con síndrome de Sjögren secundario en comparación con el primario y que era más probable que reapareciera la ESO crónica que la ESO aguda tras la interrupción del suero autólogo [184,186].
En un estudio retrospectivo de casos y controles (nivel 2) de 16 pacientes con neuropatía corneal y foto-alodinia (aumento de la sensibilidad a la luz) asociadas al ojo seco, la microscopía confocal in vivo reveló una reducción en la longitud y el número subbasales de nervios corneales [222]. El tratamiento con suero autólogo durante 3-4 meses provocó una reducción significativa de la gravedad de los síntomas y mejoras sustanciales en diversos parámetros nerviosos. Estos hallazgos respaldan los efectos positivos notificados para el suero autólogo en la queratopatía neurotrófica en una cohorte clínica de 42 sujetos (nivel 3) [225].
2.1.2.1.3. Complicaciones y conclusión.
Aunque la contaminación del suero autólogo es frecuente tras un uso prolongado (30 días) de los frascos goteros, son poco frecuentes las complicaciones a consecuencia de la contaminación [226 - 228]. Sin embargo, la falta de una metodología universalmente aceptada para la preparación del suero autólogo y las preocupaciones por la contaminación pueden retrasar la aprobación regulatoria y limitar su adopción masiva por los médicos. Para superar esto, se ha propuesto plasma autólogo al 100 % procedente de la plasmaféresis, que contribuye a minimizar la contaminación [229].
En resumen, el suero autólogo contiene factores epiteliotróficos específicos como EGF, NGF y otros, además de una elevada concentración de proteínas como albúmina y fibronectina.
El suero autólogo apoya directamente la proliferación y la migración de células epiteliales o mejora de manera indirecta la viabilidad epitelial mediante la unión y la neutralización de las citocinas inflamatorias. La mayoría de los ensayos clínicos y las series de casos que estudian el suero autólogo sugieren que puede ser eficaz en la gestión de la ESO secundaria a la EOS, probablemente debido a sus funciones antiinflamatorias, epiteliotróficas y neurotróficas, que mejoran de forma significativa los signos y síntomas en unas pocas semanas. Aunque el tratamiento requiere muchos recursos, presenta pocas complicaciones, pero la ESO puede reaparecer tras el cese del tratamiento.
2.1.2.2. Suero alogénico de adulto.
Ha surgido inquietud acerca del uso de suero autólogo cuando los pacientes presentan inflamación sistémica activa o temen la venopunción, así como en bebés, personas muy ancianas o personas con anemia crónica [230]. El suero alogénico puede ser una alternativa para estos pacientes y, dado que se puede preparar a partir de sangre previamente almacenada, es más rápido de producir y, por tanto, potencialmente más conveniente. Sin embargo, sigue existiendo preocupación por el uso de fuentes alogénicas para proteínas debido al riesgo teórico de una respuesta inmunitaria a antígenos extraños.
Existen datos clínicos limitados sobre la evaluación del papel del suero alogénico para el tratamiento de la EOS. En una serie de 16 pacientes con enfermedad de injerto contra huésped (graft versus host disease, GVHD), se observaron mejoras en los síntomas medidos por el IESO, la tinción corneal con ?uoresceína, el TDL, la densidad de células calciformes y la osmolaridad lagrimal después del tratamiento con colirio de suero alogénico al 20 % preparado a partir del cónyuge del paciente o donantes relacionados y utilizado 6-8 veces al día durante 4 semanas [231]. Harritshoj y colegas informaron de una serie de 20 pacientes con EOS debida a GVHD, artritis reumatoide y otras enfermedades inmunitarias sistémicas, y determinaron que 16/20 (80 %) de estos pacientes mostraron mejoras en signos objetivos y síntomas subjetivos de la EOS con un tratamiento con suero alogénico al 20 % 6 veces al día durante 2-4 semanas [232]. Estos investigadores utilizaron donantes varones específicos de ABO para excluir el riesgo de reactividad inmunitaria de anticuerpos ABO con antígenos de la superficie ocular. Sin embargo, en Nueva Zelanda se llevan utilizando gotas de suero no equiparadas de donantes de ambos sexos del grupo sanguíneo AB desde 2007, sin que se hayan notificado acontecimientos adversos [233]. Hasta la fecha, en la literatura no ha habido informes de complicaciones significativas asociadas al suero alogénico no equiparado, utilizado por vía tópica.
2.1.2.3. Suero del cordón umbilical.
El suero del cordón umbilical tiene ventajas similares al suero alogénico, ya que se puede preparar en grandes cantidades (hasta 250 ml) a partir de un único donante y se puede usar para muchos pacientes. Además, resulta útil en pacientes con inflamación sistémica, anemia o enfermedades crónicas, que pueden no ser candidatos ideales para colirios de suero autólogo. Para preparar el suero del cordón umbilical, se toma sangre de la vena el cordón umbilical después del parto. Después del centrifugado, el suero se diluye a una concentración del 20 % y se administra de 4 a 6 veces al día [234].
El suero del cordón umbilical tiene una mayor concentración de componentes lagrimales como EGF, NGF y factor de crecimiento transformante (TGF)-b comparado con el suero de sangre periférica [235]. Se ha demostrado que las puntuaciones de los síntomas, la TDL, la tinción corneal de fluoresceína y los hallazgos de la citología de impresión mejoran de forma significativa después de la aplicación de colirios de suero de cordón umbilical en pacientes con EOS resistente al tratamiento convencional [235] en el caso de GVHD ocular [236]. La comparación del suero de cordón umbilical con el suero autólogo administrados de 6 a 10 veces al día demostró que, aunque ambos colirios de suero provocaron mejorías, el suero de cordón umbilical generó menores puntuaciones de los síntomas y de la tinción corneal con ?uoresceína en EOS grave y una mayor densidad de células calciformes en el síndrome de Sjögren que el suero autólogo [216], lo cual se cree que es debido a una mayor concentración de factores de crecimiento y citocinas.
2.1.2.4. Preparados plaquetarios.
Las plaquetas son un depósito de factores de crecimiento activos biológicamente. Hartwig y colegas sugirieron el uso potencial de preparados de plaquetas para tratar los trastornos de la superficie ocular [193,194]. Liu et al. compararon el contenido del factor de crecimiento de pasma fresco congelado y concentrado plaquetario con el del suero y evaluaron sus efectos sobre la proliferación, migración y diferenciación de las células epiteliales corneales, en un sistema in vitro [237]. Determinaron que el contenido de factor de crecimiento era mayor en concentrado plaquetario que en plasma o suero, con una mejor proliferación celular, pero que el suero tenía una mejor migración y diferenciación celular debido a su mayor contenido de fibronectina y vitaminas.
Existen numerosos preparados de plaquetas que se utilizan en estudios clínicos, incluidos el plasma rico en plaquetas, el plasma rico en factores de crecimiento y el lisado de plaquetas. Estos preparativos difieren ampliamente en su método de procesamiento [193,194,237 - 241].
En un estudio prospectivo, Alio y asociados notificaron que el uso de plasma rico en plaquetas de 4 a 6 veces al día en 18 pacientes con EOS produjo una mejora en los síntomas en el 89 % de los pacientes y redujo la tinción corneal en el 72 % de los pacientes después de 1 mes [242]. El plasma rico en factores de crecimiento, administrado 4 veces al día a 16 pacientes con EOS, resultó ser eficaz en la reducción de los síntomas en el 75 % de los pacientes al cabo de 3 meses de tratamiento [243]. El lisado plaquetario (30 %) aplicado 4 veces al día fue efectivo en una serie de 23 pacientes con GVHD resistente, con mejora de la tinción corneal con ?uoresceína en el 70 % de los pacientes tras 6 meses de uso [244]. El plasma rico en plaquetas mejora los síntomas y signos de EOS después de la queratomileusis in situ asistida con láser (laser in-situ keratomileusis, LASIK) [242]. Sin embargo, su preparación es más compleja, y los efectos beneficiosos y las indicaciones sobre el uso de productos derivados de plaquetas sobre el suero para la gestión de la EOS no se han abordado en la literatura.
2.1.3. Otros agentes
2.1.3.1. Mucolíticos.
Los mucolíticos son un grupo de sustancias que despolimerizan la mucina e incluyen ambroxol (Mucosolvan® Boehringer Ingelheim, Ingelheim am Rhein, Alemania) y bromhexina, que se utilizan en la gestión de las molestias pulmonares que provocan un exceso en la producción de mucosa. Un pequeño ensayo clínico en sujetos con síndrome de Sjögren demostró que ambroxol oral mejoró los síntomas de sequedad [245]. Se ha notificado que otro colirio mucolítico, acetilcisteína, que también presenta propiedades antioxidantes [246], tiene un mejor efecto en la reducción de los síntomas subjetivos de EOS que las lágrimas artificiales, pero no tuvo efecto en los signos objetivos [247]. Además, los mucolíticos se pueden usar para el tratamiento paliativo de la queratitis filamentaria, que es una posible complicación de la EOS [248].
2.1.3.2. Antagonistas del receptor de TRPV1.
Se ha encontrado un canal del receptor de potencial transitorio de tipo vaniloide 1 (transient receptor potential vanilloid type 1, TRPV1) en el tejido de la superficie ocular, que se puede activar mediante hipertonía para inducir dolor e inflamación [249,250]. La administración tópica de SYL1001, un TRPV1 dirigido al ARN de interferencia corte (ic) (a una dosis de 1,125 % una vez al día), produjo una reducción significativa de las puntuaciones de los síntomas en sujetos con EOS en comparación con el placebo [251]. La inhibición selectiva de la producción del receptor TRPV1 puede reducir los síntomas del ojo seco y puede proporcionar una nueva oportunidad terapéutica para el alivio del ojo seco, pero se necesita más investigación para investigar esta hipótesis.
2.2. Enfoques para la conservación de las lágrimas
2.2.1. Oclusión del conducto lagrimal
El concepto de oclusión temporal o permanente de uno de los conductos lagrimales o de ambos es la retención de lágrimas en la superficie ocular mediante el bloqueo de su drenaje.
2.2.1.1. Indicaciones y contraindicaciones.
Cualquier afección que pudiese obtener beneficios de la retención acuosa en la superficie ocular es una indicación razonable para la oclusión unilateral [252] o bilateral del conducto lagrimal [253]. Estas afecciones incluyen el uso sintomático de lentes de contacto [254,255], ojo seco relacionado con cirugía refractiva [256 - 258], OSDA secundario a una variedad de enfermedad sistémicas (incluidos síndrome de Sjögren, GVHD, enfermedades autoinmunes) [259,260], ojo seco asociado a un TDL rápido [252], medicamentos sistémicos que reducen la producción de película lagrimal, queratoconjuntivitis límbica superior [261], cualquier irregularidad corneal o cicatriz que afecte a la estabilidad lagrimal, parálisis del parpado o anomalías en el cierre del párpado, y epiteliopatía tóxica [262].
El uso de la oclusión del conducto lagrimal en presencia de inflamación de la superficie ocular es un tema controvertido, dado que la oclusión teórica del flujo lagrimal de salida podría prolongar la presencia de citocinas proinflamatorias en la superficie ocular y, por tanto, se recomienda el tratamiento de la inflamación previa a la oclusión. Sin embargo, un estudio reciente demostró que la oclusión del conducto lagrimal en 29 personas con EOS moderada durante 3 semanas provocó una reducción de la tinción corneal con ?uoresceína y de las puntuaciones de los síntomas, sin elevación de los niveles de citocina o metaoloproteinasas de matriz (matrix metalloproteinase, MMP)-9, lo que cuestiona si los niveles de citocina se elevan necesariamente con la oclusión del conducto lagrimal durante cortos periodos de uso [263].
2.2.1.2. Oclusión del conducto lagrimal con tapones.
La manera más frecuente de realizar la oclusión del conducto lagrimal es utilizando tapones lagrimales. El tapón se puede colocar al nivel de la abertura del conducto lagrimal o a nivel más profundo en el canalículo. Aunque es relativamente sencillo entender la justificación para usar tapones lagrimales para el OSDA, su uso para la gestión del OSE sigue siendo controvertido y los resultados son equívocos en lo que respecta a su efectividad para la mejora del estado de la glándula de Meibomio y la inestabilidad de la capa lipídica [264 - 267].
2.2.1.2.1. Tipos de dispositivos.
Los tapones lagrimales se dividen en dispositivos absorbibles y no absorbibles.
Los dispositivos absorbibles son inserciones temporales que normalmente se utilizan como dispositivos “de prueba” para determinar la eficacia de la oclusión antes de realizar una oclusión permanente. Los tapones a base de colágeno, que se absorben en entre 1 y 16 semanas, son los que se utilizan con más frecuencia [253,268,269]. El atelocolágeno es una solución de colágeno que se extrae del tejido dérmico animal, del que se eliminan los telopéptidos antigénicos acoplados a ambos extremos de la molécula de colágeno mediante tratamiento con pepsina [270]. A temperaturas de 4 °C o menores, el atelocolágeno se disuelve en una solución tampón de fosfato neutra. Si esta solución se inyecta a través del punto lagrimal, se convierte en un gel de color blanco a temperatura corporal. El tapón de atelocolágeno inyectable tiene un éxito demostrado en diversos estudios [270-272]. Los tapones de colágeno succilinado [273] y la hipromelosa al 2 % [274] pueden ser alternativas prometedoras para la oclusión temporal del conducto lagrimal.
Los tapones no absorbibles o “permanentes” suelen ser a base de silicona y existen en una gran variedad de diseños. El tapón de estilo Freeman consta de un collar de superficie que descansa sobre la abertura del conducto lagrimal, un cuello y una base ancha, mientras que el tapón Herrick es un tapón de silicona intracanalicular con forma de cono [275]. Algunos tapones de silicona tienen un canal interior para la oclusión parcial, que podría permitir un drenaje limitado. El SmartPlug™ cilíndrico es un tapón intracanalicular fabricado a partir de un polímero termolábil que cambia de tamaño y forma al introducirlo en punto lagrimal [276 - 279]. El tapón intracanalicular FORM FIT® (Oasis Medical, Glendora, CA, EE. UU.) está fabricado a partir de un hidrogel inyectable que se hidrata in situ durante un periodo de 10 minutos y se expande para ajustarse a la forma del canalículo [280], lo que elimina el requisito de seleccionar un tapón del tamaño adecuado. El tapón se suministra en una inserción precargada que dispensa el tapón desde dentro de una funda de poliamida.
Además de dispositivos, determinados tipos de adhesivos de cianoacrilato se pueden utilizar para la oclusión temporal del conducto lagrimal antes de determinar si está justificada una oclusión a largo plazo [281,282]. Para la oclusión permanente, existe una variedad de opciones quirúrgicas que se pueden usar, tal como se describe en la sección 2.2.1.3.
2.2.1.2.2. Complicaciones.
La complicación más frecuente de la oclusión del conducto lagrimal es la extrusión espontánea del tapón [265,283 - 286], que puede producirse hasta en un 60 % de los casos [287 - 289]. Otras complicaciones notificadas incluyen infección [290 - 292], migración canalicular del tapón [286,290], granuloma piogénico, agrandamiento del conducto lagrimal [286] y, en raras ocasiones, tumores [293]. Las infecciones (como queratitis, conjuntivitis, canaliculitis o dacriocistitis) se producen con más frecuencia con dispositivos intracaniculares [291,294]. Otras complicaciones menos graves, con frecuencia debidas a la presencia mecánica del dispositivo, incluyen conjuntivitis, hemorragia subconjuntiva, quemosis, epifora, eritema del conducto lagrimal, molestias y sensación de cuerpos extraños [294].
2.2.1.3. Oclusión quirúrgica del conducto lagrimal.
El cierre quirúrgico permanente del conducto lagrimal suele reservarse para pacientes que no pueden tolerar los tapones lagrimales. Existe una amplia variedad de métodos quirúrgicos [281], incluida la cauterización térmica total o parcial [295 - 298], oclusión del conducto lagrimal con un colgajo conjuntival [299], injerto conjuntival [300], sutura del tapón del conducto lagrimal [301], destrucción total (extirpación) del canalículo [302] y ligadura canalicular [303]. Los métodos térmicos incluyen cauterización, diatermina y el uso de un láser de argón, y estos métodos pueden realizarse en profundidad dentro del canalículo o superficialmente en la parte exterior del conducto lagrimal [259,297,298]. Hoy en día, la cauterización térmica manual desechable es el método utilizado con más frecuencia en la práctica clínica.
Actualmente no existen estudios de nivel 1 y solo existe un número limitado de informes de nivel 2 acerca de la eficacia del cierre quirúrgico de los conductos lagrimales para el tratamiento de la EOS. Series de casos comparativos han demostrado que el cierre permanente de los conductos lagrimales mediante cauterización mejora significativamente los síntomas, la puntuación Schirmer, la tinción corneal con ?uoresceína, las puntuaciones de rosa bengala y el TDL en pacientes con GVHD y síndrome de Stevens-Johnson [259,304].
Se han notificado muy pocas complicaciones con la cauterización. La epifora puede ser un problema potencial si tanto el conducto lagrimal superior como el inferior están total y permanentemente cerrados. Para evitar esto, la oclusión incompleta del conducto lagrimal se puede lograr con cauterización térmica. En pacientes con síndrome de Sjögren, esta técnica de oclusión parcial ha provocado una mejora de los síntomas, del TDL, de la tinción conjuntival y la tinción corneal con ?uoresceína [298]. Puede producirse recanalización, dependiendo de la técnica utilizada y de la respuesta inflamatoria que tenga lugar, y en estos casos se necesita repetir el procedimiento para cerrar completamente el conducto lagrimal [297]. Parece que las técnicas que implican la cauterización superficial tienen una tasa superior de recanalización [305], y que los procedimientos quirúrgicos más profundos pueden incrementar la tasa de éxito [296].
2.2.1.4. Resumen de la oclusión del conducto lagrimal.
La oclusión del conducto lagrimal puede tener mayor éxito si se combina con otros tratamientos para la EOS [306]. Ervin et al. realizaron una revisión sistemática de la oclusión del conducto lagrimal para la EOS, que incluía 7 estudios con 305 sujetos [307]. La conclusión del autor fue que, aunque los tapones lagrimales proporcionaban una mejora sintomática y los resultados clínicos mejoraron con respecto a las medidas iniciales, pocos estudios demostraron un beneficio de los tapones lagrimales con respecto a una intervención comparativa. Además, estos autores afirmaron que, aunque la evidencia es muy limitada, los datos sugieren que los tapones de silicona pueden proporcionar un alivio sintomático en el ojo seco grave y que los tapones de colágenos temporales parecen tener una efectividad similar a la de los tapones de silicona a corto plazo [307].
Hasta la fecha, no existen estudios de nivel 1 a gran escala que respalden la afirmación de que la oclusión del conducto lagrimal de cualquier tipo es efectivo en la gestión de la EOS. Sin embargo, en la Tabla 4 [252,257,263,270,272,274,283,308 - 313] se recogen 14 estudios de Nivel 2 que lo respaldan.
2.2.2. Gafas con cámara de humedad y humidificadores
Las gafas con cámara de humedad son gafas especialmente diseñadas para ralentizar la evaporación de las lágrimas proporcionando un entorno húmedo y minimizando el flujo de aire sobre la superficie ocular. Hay disponibles varios de estos dispositivos. Pese a que la eficacia clínica de las gafas con cámara de humedad se ha notificado en casos prácticos [314,315], hasta la fecha ningún estudio de alto nivel ha investigado el valor terapéutico de estos dispositivos, pero parece que pueden revelarse como un posible complemento al tratamiento prescrito, especialmente en entornos adversos [316].
Los dispositivos humidificadores situados localmente también se han propuesto para mejorar la humedad o la calidad del aire local. Sin embargo, hasta ahora solo un estudio controlado respalda su efectividad en la gestión del ojo seco [317].
2.3. Enfoques para la estimulación lagrimal
Hay varios agentes farmacológicos tópicos que estimulan la secreción acuosa, de mucina y/o lípidos, que están disponibles en determinados mercados o en desarrollo.
2.3.1. Secretagogos tópicos
2.3.1.1. Secretagogos acuosos.
El dicuafosol tetrasodio (Diquas®; Santen, Osaka, Japón) está aprobado como una solución oftalmológica a una concentración al 3 % en Japón y Corea del Sur para el tratamiento del ojo seco. Se trata de un agonista del receptor purinérgico P2Y2 que estimula la secreción de agua y mucina de las células epiteliales conjuntivales y de las células calciformes, que conduce a una mejor estabilidad de la película lagrimal en el ojo seco [14,318,319]. Varios ensayos aleatorizados y controlados han demostrado que la aplicación de dicuafosol tópico mejora de forma significativa marcadores objetivos de la EOS, como la tinción corneal y conjuntival con ?uoresceína y, en algunos estudios, del TDL y de las puntuaciones Schirmer [38,320,321]. El dicuafosol tiene utilidad potencial en diversos trastornos específicos de ojo seco, incluido el síndrome de Sjögren [322], OSDA [323], ojo seco con TDL corto [324], DGM [325], ojo seco tras LASIK [326] y cirugía de cataratas [327], así como en usuarios de lentes de contacto [325]. Recientemente, Byun et al. demostraron que el dicuafosol es efectivo en el fomento de la curación de las heridas epiteliales corneales y que este efecto puede ser el resultado de la proliferación celular estimulada por cinasas y regulada por el receptor del factor de crecimiento epidérmico o por señales extracelulares y de la migración celular por medio de la elevación del calcio intracelular mediada por el receptor de P2Y2 [328]. En estudios en EE. UU., el ciquafosol tetrasodio al 2 % no alcanzó sus criterios de valoración principales y secundarios y no consiguió la aprobación de la FDA [329].
La lacritina es una glicoproteína que tiene actividad prosecretora en la glándula lagrimal y actividad mitogénica en el epitelio corneal y se reduce en las lágrimas de pacientes con síndrome de Sjögren [330] y otras formas de ojo seco [128]. La lacritina administrada por vía tópica tiene el potencial terapéutico para tratar el OSDA [331].
2.3.1.2. Secretagogos de mucina.
Existen diversos fármacos que específicamente actúan sobre el déficit de mucina en la EOS, incluido el dicuafosol tetrasodio (ver la sección 2.3.1.1).
La suspensión oftálmica de rebamipida (Mucosta®; Otsuka Pharmaceutical, Chiyoda, Japón) está aprobada actualmente en Japón para el tratamiento del ojo seco. Se trata de un secretagogo de mucina que fomenta la producción de glicoproteínas similares a la mucina en células humanas epiteliales de la córnea, aumentando los niveles de expresión de MUC1, MUC4 y MUC16 por medio de señales implicadas en la activación del receptor del factor de crecimiento epidérmico [14,332]. En un estudio multicéntrico, abierto y de un solo grupo, un total de 154 pacientes recibieron rebamipida al 2 % cuatro veces al día durante 52 semanas [333]. La tinción conjuntival con verde de lisamina, la tinción corneal con fluoresceína, el TDL y los síntomas subjetivos mejoraron significativamente a las 2 semanas en comparación con el inicio, y se observaron mejoras adicionales en cada visita hasta la semana 52. La rebamipida tópica también es potencialmente efectiva en el tratamiento de otros trastornos de la superficie ocular, como el ojo seco con TDL corto [334], la epiteliopatía del párpado en limpiaparabrisas [335] y el daño ocular por álcalis [336,337]. La rebamipida también ha demostrado ser efectiva en la mejora del aspecto de la superficie ocular y de la calidad óptica en pacientes con ojo seco que se someten a cirugía refractiva [338]. Aunque ha recibido la aprobación en Japón, ensayos de fase III para rebamipida realizados en EE. UU. no fueron capaces de proporcionar los datos necesarios para que la FDA diera su aprobación [329].
La galectina-3, un miembro de la familia de la lectina, es una proteína de unión a los carbohidratos que controla múltiples procesos biológicos en el epitelio o la superficie ocular. Se ha demostrado que las personas con EOS tienen una mayor concentración de la proteína galectina-3 en sus lágrimas en comparación con las personas normales, y se ha concluido que la liberación de galectina-3 celular en las lágrimas se asoció al desarrollo de daño epitelial [339]. El dipéptido derivado de extracto placentario (JBP485), un dipéptido que fomenta la producción de galectina-3, fomenta la expresión y secreción de la mucina formadora del gel 5AC (MUC5AC) en epitelio conjuntival de conejo [340]. JBP485 también ha demostrado elevar la expresión de mucinas unidas a membranas (MUC1/4/16) en epitelio corneal de conejo. JBP485 indujo la secreción lagrimal en el modelo de conejo y provocó una reducción del daño epitelial de la córnea en un modelo de ojo seco de ratón. Por tanto, JBP485 fomentó tanto las mejoras en la secreción de mucina como de lágrima acuosa en modelos animales [340].
El micofenolato de mofetilo (MMF) es un inhibidor de linfocitos utilizado con frecuencia en el tratamiento de enfermedades autoinmunes y el rechazo de trasplantes. Se ha notificado que una baja concentración de MMF puede fomentar la proliferación de células calciformes conjuntivales humanas y aumentar la producción de ARN mensajero (ARNm) de MUC5AC in vitro [341], pero aún se tienen que llevar a cabo los estudios clínicos.
La eupatilina es un tipo de ?avonoide. Tiene efectos potentes en la inducción de la secreción de mucinas en las células conjuntivales, tanto en estudios in vitro como in vivo, lo que sugiere que podría tener potencial como un tratamiento futuro para la EOS [342,343].
Los factores trébol son productos secretores de células secretoras de mucina. Se ha determinado que los niveles de la familia de péptidos trébol 3 (TFF3) son elevados en las lágrimas de pacientes con EOS. En un estudio in vitro se demostró que algunas citocinas proinflamatorias (pero no la hiperosmolaridad) inducían también la producción de TFF3, lo que sugiere que TFF3 podría ser un objetivo potencial para el tratamiento de la EOS [344,345].
El NGF regula el crecimiento, la proliferación y el mantenimiento de determinadas neuronas. En un estudio in vitro, se demostró que el NGF estimula la diferenciación celular del epitelio conjuntival y la producción de mucina [346].
2.3.2. Estimulación lipídica
El factor de crecimiento simular a la insulina 1 (IGF-1) tiene efectos estimuladores de los lípidos en las células de la glándula de Meibomio in vitro [347]. Se ha determinado que los andrógenos regulan al alza los genes implicados en las vías metabólicas de los lípidos y regulan a la baja aquellos relacionados con la queratinización en células humanas epiteliales de la glándula de Meibomio en diversos estudios de laboratorio [348 - 351]. Los resultados de ensayos clínicos de fase II muestran que el tratamiento de pacientes con DGM con testosterona tópica mejora la calidad de las secreciones de la glándula de Meibomio y reduce las molestias oculares [352]. Actualmente se están realizando en Europa otros ensayos clínicos para el tratamiento de la DGM con testosterona tópica.
Puede encontrar más detalles sobre el impacto de los andrógenos y el IGF-1 en el informe sobre sexo, género y hormonas de TFOS DEWS II [353].
2.3.3. Secretatogos orales
Dos agonistas colinérgicos administrados oralmente, pilocarpina y cevimelina, están disponibles en el mercado para el tratamiento del ojo seco asociado al síndrome de Sjögren. Las personas con síndrome de Sjögren tienen autoanticuerpos que se unen a los receptores muscarínicos de acetilcolina en las glándulas exocrinas, y la pilocarpina y la cevimelina son agonistas del receptor muscarínico de acetilcolina (parasimpatomiméticos) que tienen como objetivo anular este efecto.
Las personas con síndrome de Sjögren tratadas con pilocarpina oral durante 12 semanas experimentaron un efecto beneficioso sobre los síntomas y una reducción en la tinción con rosa de bengala, pero no se pudo sustanciar un aumento de la producción lagrimal [354]. Otros estudios han demostrado una mejora de los síntomas, la tinción corneal con ?uoresceína, la tinción con rosa de bengala, la densidad de las células calciformes y el TDL, pero de nuevo no se demostró mejora alguna en la producción lagrimal mediante la prueba de Schirmer [355,356]. Sin embargo, la pilocarpina oral fue capaz de aumentar la altura del menisco lagrimal (AML) en personas con síndrome de Sjögren [357]. El efecto secundario notificado con más frecuencia de esta medicación es la sudoración excesiva, que se produjo hasta en un 25 % de los pacientes [358].
Petrone et al. evaluaron la seguridad y eficacia de 2 dosis de cevimelina para el tratamiento de la xerostomia y el ojo seco en pacientes con síndrome de Sjögren en un estudio de 12 semanas, con doble enmascaramiento, aleatorizado y controlado con placebo [359]. Los pacientes que tomaron cevimelina tres veces al día tuvieron mejoras significativas en la evaluación subjetiva de la sequedad ocular, la boca seca y un aumento de las tasas de flujo salival y lagrimal [359]. Los acontecimientos adversos notificados con frecuencia incluían dolor de cabeza, aumento de la sudoración, dolor abdominal y náuseas [359,360].
La eficacia de los secretagogos orales parece ser mayor en el tratamiento de la sequedad oral que de la sequedad ocular [361,362]. Se ha determinado que los pacientes con síndrome de Sjögren tienen más probabilidad de continuar con cevimelina que con pilocarpina a largo plazo, debido a que los efectos secundarios notificados con cevimelina son menores. El fracaso terapéutico de un secretagogo no predijo resultados similares con el otro, donde los usuarios que repiten el uso tienen más probabilidad de continuar con el tratamiento a largo plazo [358].
2.3.4. Neuroestimulación nasal
La neuromodulación es una estrategia terapéutica que implica la interactuación directamente con el sistema nervioso a través de metodologías eléctricas, electromagnéticas, químicas u optogenéticas [363,364]. El objetivo es la activación, inhibición, modificación y/o regulación a largo plazo de la entrada neural para corregir disfunciones orgánicas o tisulares, así como los síntomas de la enfermedad. El reflejo nasolagrimal regula al alza la producción lagrimal tras la estimulación química o mecánica de la mucosa nasal [365,366]. El arco reflejo nasolagrimal comienza en los nervios sensoriales que recubren la cavidad nasal (el brazo aferente) y termina con la inervación parasimpática de los principales tejidos objetivo que contribuyen a la producción lagrimal (el brazo eferente) [367]. En un estudio prospectivo de casos y controles en pacientes con una producción lagrimal normal, se ha demostrado que anestesiar la mucosa nasal reduce el lagrimeo basal en un 34 % en comparación con un control salino [368].
Se ha desarrollado un neuroestimulador lagrimal intranasal para inducir la producción lagrimal normal por medio de la estimulación del reflejo nasolagrimal. Este dispositivo consta de un estimulador manual equipado con una punta doble de hidrogel desechable y un cargador externo. El neuroestimulador lagrimal intranasal permite la autoadministración de corrientes eléctricas mínimas al nervio etmoidal anterior, estimulando así la producción lagrinal natural inmediata en pacientes con EOS [366]. Cuarenta sujetos con ESO de leve a grave utilizaron un prototipo de neuroestimulador lagrimal intranasal en un estudio piloto abierto de un solo grupo y no aleatorizado de 180 días de duración [369]. Los sujetos recibieron instrucciones para realizar la estimulación con el dispositivo 2 o más veces al día, según sus necesidades. En el día 180, la estimulación con el dispositivo había aumentado de forma significativa las puntuaciones medias de Schirmer en comparación con las puntuaciones de producción lagrimal iniciales sin estimulación. Al final del periodo de seguimiento, las puntuaciones medias de los síntomas y de la tinción conjuntival fueron significativamente menores con respecto al inicio. Los resultados preliminares también han mostrado un efecto positivo del neuroestimulador sobre la función de las células calciformes [370].
El neuroestimulador lagrimal intranasal TrueTear™ (Allergan, Parkway Parsippany, NJ, EE. UU.) recibió recientemente la aprobación de la FDA con una indicación aprobada para proporcionar un aumento temporal en la producción lagrimal durante la neuroestimulación en pacientes adultos. Una serie de estudios adicionales están en curso, y los resultados están a la espera de publicación [371,372].
2.3.5. Varios métodos de estimulación lagrimal
Se han notificado otros métodos nuevos para estimular la producción lagrimal. Estos incluyen la respiración abdominal durante 3 minutos, que supuestamente aumentaron el volumen del menisco lagrimal en mujeres sanas [373].
Los termorreceptores fríos se activan mediante el secado de la superficie ocular, y la estimulación de estos receptores podría aumentar la producción lagrimal [374,375]. La existencia del canal catiónico del potencial transitorio del receptor, subfamilia M, miembro 8 (TRPM8) en las terminaciones nerviosas de los termorreceptores fríos de la córnea es coherente con el hallazgo de que su estimulación con mentol y temperaturas frescas podría aumentar la producción lagrimal [376,377]. Finalmente, la cafeína, probablemente la sustancia psicoactiva que más se consume, parece estimular la secreción lagrimal en sujetos sanos sin ojo seco [378].
3. Tratamientos para las anomalías del párpado volver arriba
3.1. Blefaritis anterior
3.1.1. Higiene del párpado
Una apropiada higiene del párpado es importante en la gestión de diversas afecciones del párpado que provocan ojo seco (en particular blefaritis) y, si se emplea debidamente, puede reducir los derivados lipídicos y bacterias lipolíticas asociadas a estas afecciones [379 - 385]. Los limpiadores de párpados que utilizan una disolución suave de champú de bebé aplicado con un hisopo o bastoncillo de algodón han sido el tratamiento más ampliamente aceptado [382,386,387]. Un reciente estudio de nivel 1 demostró la eficacia de los limpiadores de párpados para eliminar las costras en la blefaritis anterior, tanto con un limpiador de párpados comercial como con un champú para bebé diluido [388]. Sin embargo, en relación con el champú para bebé, el limpiador específico para párpados mostró niveles reducidos de MMP-9 en la superficie ocular, una mayor calidad de la capa lipídica y una mejor tolerancia. Además, se encontró que el champú para bebés estaba asociado a una reducción de los niveles de MUC5AC de la superficie ocular, lo que sugiere que el champú para bebés puede tener un efecto adverso en la función de las células calciformes [388]. Con preferencia al uso de champú de bebé, existe una amplia variedad de productos exclusivos para la limpieza del párpado, que utilizan distintos mecanismos de administración, incluidos cepillos, espumas, soluciones y toallitas; su descripción individual queda fuera del alcance de esta revisión.
El informe del taller de TFOS MGD informó de que “la higiene del párpado es ampliamente considerada como un tratamiento establecido efectivo para la DGM y la blefaritis” [389]. Sin embargo, el cumplimiento con el seguimiento de las instrucciones de higiene del párpado es notablemente deficiente. Un reciente estudio transversal de 207 sujetos a los que se prescribieron procedimientos de higiene del párpado (compresas calientes diarias y limpieza del párpado con cepillo) determinaron que solo el 55 % cumplían con el tratamiento tras 6 semanas de uso [390].
A pesar del hecho de que varias organizaciones profesionales sugieren formas de limpiar los párpados, hasta la fecha no existen directrices universalmente aceptadas para la limpieza de los párpados y se carece de evidencia en publicaciones con revisión científica externa, lo que sugiere que se trata de un área merecedora de estudio. Se debe tener precaución al limpiar los párpados en los que se aplica maquillaje para evitar la posterior contaminación de la superficie ocular [391 - 393].
La Tabla 5 recoge información sobre estudios de nivel 2 relacionados con métodos de limpieza de los párpados y su impacto en la blefaritis o el ojo seco (no se incluyen combinaciones con otros tratamientos farmacológicos) [386,387,394 - 400].
3.1.1.1. Sobrecolonización bacteriana
3.1.1.1.1. Antibióticos tópicos. La higiene del párpado para reducir la carga bacteriana en el margen del párpado normalmente se lleva a cabo en la gestión de la EOS asociada a la blefaritis [401]. Sin embargo, por lo general no se recomienda a largo plazo lograr esto únicamente mediante la prescripción de pomadas o colirios antibióticos tópicos (como ácido fusídico), pero es un enfoque que adoptan algunos facultativos [402] y se ha recomendado una dosis corta de antibióticos tópicos en informes basados en el consenso [403]. Un reciente estudio de nivel 2 demostró que una pomada basada en o?oxacino fue valiosa en la gestión de pacientes con DGM obstructiva. La azitromicina tópica (un antibiótico macrólido) se ha utilizado en la gestión de la EOS, pero se cree que tiene un efecto antiinflamatorio en lugar de simplemente reducir la flora bacteriana del párpado (consultar la sección 4.5). Se requieren más estudios de nivel 1 para examinar el potencial de prescribir solamente antibióticos tópicos para la gestión de la EOS.
3.1.1.2. Infestación por Demodex.
La infestación por Demodex es un factor causante en muchos casos de blefaritis intratable y a menudo se asocia a síntomas del ojo seco [404], aunque actualmente no existen evidencias que muestren una asociación directa con el desarrollo de DGM [389]. Históricamente, el tratamiento del Demodex ocular incluía una amplia gama de productos, la mayoría de los cuales carecían de evidencia de alto nivel para respaldar su uso. Estos incluían gel de metronidazil tópico al 2 % [405,406], pomada de óxido de mercurio al 1 % [407] y gel de pilocarpina al 4 % [408]. Más recientemente, se ha encontrado una gestión apropiada con el uso de productos tópicos que contienen aceite del árbol del té o ivermectina oral, tal como se resumen en la Tabla 6 [409 - 415].
3.1.1.2.1. Aceite de árbol del té.
El aceite del árbol de té (AAT) es un aceite natural y esencial procedente de hojas vaporizadas de Melaleuca alternifolia (de la melaleuca de hoja estrecha o árbol del té, originario de Australia) que muestra propiedades antimicrobianas, antiinflamatorias, antifúngicas y antivirales [416] y es tóxico para el Demodex [417]. En un estudio clínico de nivel 2, un frotado semanal del párpado con AAT al 50 % acompañado de un frotado diario del párpado con champú del árbol del té fue más efectivo en la erradicación del Demodex ocular que el frotado diario del párpado con un champú para bebés con una concentración del 50 % [417]. Sin embargo, el AAT puede ser tóxico para el ojo y causa escozor e irritación oculares si se utiliza en su forma pura. El componente activo del AAT es el 4-terpineol [418,419], y actualmente hay disponibles en el mercado toallitas preformuladas que son equivalentes al 25 % del AAT puro. Estos reducen el riesgo de toxicidad para la superficie ocular en comparación con el uso de concentraciones más elevadas de AAT. Varios estudios han demostrado una reducción considerable en el número de Demodex en las pestañas después del tratamiento con AAT [409,410,413,414,417].
Hasta la fecha, existe información muy limitada sobre el impacto positivo del AAT sobre los síntomas y signos del ojo seco [420] y se necesitan más estudios sobre este tema.
3.1.1.2.2. Ivermectina.
La ivermectina es un fármaco antiparasitario de amplio espectro que se utiliza principalmente para tratar la estrongiloidiasis y controlar la oncocercosis. Se trata de un medicamento de dosis única de bajo coste que tiene una buena tolerabilidad entre los pacientes. Una dosis oral de ivermectina ha demostrado reducir con éxito el número de Demodex encontrados junto a las pestañas de pacientes con blefaritis [411,412]. El rendimiento ha mejorado al combinar el uso de la ivermectina con metronidazol [415] o con crema de permetrina [421]. Se necesitan más estudios para confirmar el papel de la ivermectina en el tratamiento de los síntomas y signos de EOS.
3.2. Disfunción de las glándulas de Meibomio
La definición de 2011 de DGM formulada por el taller TFOS MGD resaltó la importancia de la obstrucción de los conductos terminales en la DGM [2], que ha fomentado el uso de tratamientos para eliminar la obstrucción del conducto terminal y del sistema de conductos de las glándulas de Meibomio. Por tanto, existe un papel significativo para los tratamientos convencionales en el tratamiento de la DGM, incluidos los lubricantes oculares, la higiene del párpado y las compresas calientes.
3.2.1. Lubricantes oculares
Como la DGM provoca la reducción del grosor de la capa lipídica, puede ser beneficioso reemplazar los lípidos por colirio lubricante ocular o sprays que contengan lípidos. Diversos estudios han descubierto una mejora de los signos y síntomas con el uso de colirios a base de lípidos para tratar el ojo seco (Tabla 7) [65,141,142,157,182,422 - 427]. Un estudio de nivel 1 ha confirmado el grado de grosor de la capa lipídica y el TDNI en ojos normales tratados con un spray liposomal [178]. Para mejorar el potencial rendimiento de los colirios a base de lípidos, se han incorporado conceptos de nanotecnología a los colirios de emulsión lipídica [147,428].
3.2.2. Compresas calientes
A pesar de la eficacia demostrada de las compresas calientes en muchos estudios clínicos, el cumplimiento es, con frecuencia, deficiente, debido al tiempo necesario y a la dificultad que supone mantener la temperatura de la compresa durante un periodo prolongado de tiempo [389,390,429 - 432]. Un método para prolongar el tiempo durante el que un paño facial retiene el calor es envolver varios paños unos con otros asemejándose a la estructura de un fardo [433].
La capacidad para calentar desde una compresa caliente para suavizar o licuar las secreciones en glándulas obstruidas en el caso de DGM está respaldada por evidencias de nivel 2 y 3 [433 - 436]. La temperatura y el tiempo necesarios para fundir el material obstructivo en el conducto secretor de la glándula de Meibomio no se han establecido de forma definitiva. Evidencias preliminares de múltiples estudios han señalado un rango de puntos de fusión (32 °C-45 °C) para el contenido de las glándulas de Meibomio, lo que refleja en parte que el meibum es una mezcla lipídica muy compleja [434,435,437 - 439]. El material de la glándula de Meibomio que provoca una obstrucción grave tiene un punto de fusión superior que el material de glándulas menos obstruidas [434,437,440]. Las evidencias de nivel 2 y 3 sugieren que puede ser necesario calentar la glándula de Meibomio individual a una temperatura de ≥40 °C para lograr un tratamiento óptimo con compresas calientes [433,437,441]. La recomendación de 40 °C hace referencia a la temperatura de la conjuntiva palpebral y la glándula, no la temperatura en la superficie de contacto del dispositivo de tratamiento o la temperatura de la piel externa de los párpados.
Arita y colegas evaluaron el impacto de 5 dispositivos de calentamiento del párpado disponibles en el mercado en 10 sujetos con DMG y 10 controles durante un periodo de entre 2 y 4 semanas [442]. Los 5 dispositivos constaban de 2 métodos secos (no húmedos) y 3 métodos húmedos. Una única aplicación de los 5 dispositivos mejoró las puntuaciones de los síntomas, aumentó el TDL y aumentó las temperaturas de la superficie ocular, pero solo durante un máximo de 30 min. Los dispositivos húmedos provocaron la “humedad” de la superficie de la piel del párpado, que provoca el enfriamiento evaporativo que tendió a limitar los efectos beneficiosos del calentamiento del párpado. Sus resultados mostraron que un calentamiento repetido del párpado con un dispositivo no húmedo mejoró la función de la película lagrimal en personas normales y puede tener efectos beneficiosos tanto en la película lagrimal como en la función de la glándula de meobomio en pacientes con DG. Concluyeron que se requería un calentamiento repetido no húmedo durante 2 o 4 semanas para lograr una mejora estable en personas normales y con DGM, respectivamente [442].
Un estudio prospectivo aleatorizado del ojo contralateral recomendó la aplicación de compresas calentadas a 45 °C en el exterior del párpado durante un mínimo de 5 min. Se debe lograr un contacto óptimo entre la compresa y el párpado, y las compresas deben sustituirse cada 2 minutos para garantizar que se mantiene la temperatura [443]. Varios estudios preliminares en participantes sin ojo seco han investigado el efecto de distintas compresas de calentamiento sobre la temperatura del párpado [433,444]. Todas las compresas demostraron un aumento de la temperatura en la superficie conjuntiva del párpado inferior y ninguna causó daños en los párpados. Sin embargo, solo la aplicación estratificada y continua de toallitas calientes empaquetadas calentadas en el microondas fue capaz de mantener una temperatura de 40 °C en la superficie conjuntival del párpado inferior [433]. Este estudio concluyó que una superficie húmeda mejoraba la transmisión del calor a través del párpado y se debe emplear frente a los tratamientos secos [433]. Debe tenerse cuidado de no calentar la piel del párpado más de 45 °C para evitar el daño térmico [445,446]. Por fortuna, una salvaguarda es la respuesta de la persona al dolor, que le protege frente a un daño térmico extenso en la piel del párpado, ya que un paciente no tolerará un paño demasiado caliente [447].
Un posible problema es el calentamiento de la córnea de aproximadamente 36 °C a 39,4 °C después de aproximadamente 8 minutos [448]. Si se frota el ojo cuando la temperatura de la córnea es elevada, puede producirse una deformación corneal y visión borrosa [449]. Se ha considerado que los riesgos del masaje ocular con una temperatura requieren instruir al paciente sobre cómo llevar a cabo el procedimiento de forma óptima [448,450].
Un estudio de sujeto con DGM demostró que 12 semanas de tratamiento de calentamiento del párpado provocaban un beneficio terapéutico, con una reducción del exceso de actividad de la fosfolipasa de la superficie ocular (que es perjudicial para la estabilidad de la película lagrimal) [451].
Además de las compresas caseras, ahora hay una amplia variedad de dispositivos disponibles en el mercado para la gestión de las anomalías del párpado que elevarán la temperatura del párpado durante un periodo de tiempo más prolongado [431,432].
3.2.2.1. Blephasteam.
Blephasteam® (Thea Pharmaceuticals, Newcastle under Lyme, Reino Unido) se asemeja a unas gafas de natación y se conecta a una toma eléctrica para suministrar calor latente, sin presión, a los párpados. Se coloca una inserción humedecida en cada cámara sellada herméticamente para proporcionar un entorno caliente y de humedad elevada sobre cada ojo. Un estudio preliminar en sujetos normales determinó que el dispositivo aumentó la temperatura de los párpados [433], y un estudio en pacientes con ojo seco notificó que la evaporación de la película lagrimal se redujo un 32 % inmediatamente después del tratamiento [452]. Dos estudios aleatorizados, controlados y enmascarado para el investigador determinaron una mayor eficacia con Blephasteam® que con el tratamiento con toallas calientes [429,453], y un estudio cruzado, aleatorizado y enmascarado para el investigador realizado en voluntarios sanos determinó que Blephasteam® calentó el párpado inferior durante un período de tiempo significativamente más prolongado que las compresas calientes [453]. La agudeza visual también mejoró de manera significativa después del uso de Blephasteam® [453]. Dos estudios prospectivos no aleatorizados determinaron una mejoría de los síntomas en pacientes con DGM [430,454] y un aumento del TDL. También se observó la reducción del diámetro y del área acinar en personas que no respondieron al tratamiento con compresas calientes [430].
3.2.2.2. MGDRx EyeBag®.
La bolsa para los ojos MGDRx EyeBag® (The EyeBag Company, West Yorkshire, Reino Unido) es una compresa caliente reutilizable, formada por un algodón y una bolsa de seda que contiene semillas de linaza, que se calienta en un microondas durante 30 s. Estudios realizados en ojos normales determinaron que la bolsa para los ojos MGDRx EyeBag® logró temperaturas oculares superiores que otra máscara de calentamiento [455], y también mantiene el calor más tiempo que un sencillo paño para la cara calentado en estudios tanto in vitro como in vivo [431,432]. Un estudio contralateral aleatorizado y enmascarado para el investigador informó de una mejora de los síntomas después de usar MGDRx EyeBag® dos veces al día durante dos semanas [456]. Los beneficios duraron hasta 6 meses, con sesiones de retratamiento ocasionales que provocaron un mayor confort.
3.2.2.3. Máscara EyeGiene®.
La máscara EyeGiene® (Eyedetec Medical, Danville, CA, EE. UU.) utiliza unidades de calentamiento desechables activadas con presión [455]. Un estudio aleatorizado controlado y con enmascaramiento para el examinador determinó que la máscara EyeGiene® tenía una eficacia similar a una toalla caliente, pero no era tan efectiva como Blephasteam® [429] ni tan efectiva en la elevación de la temperatura ocular como una máscara ocular a base de semillas de linaza [457].
3.2.2.4. Dispositivo de compresión caliente con infrarrojos.
El dispositivo de compresión caliente con infrarrojos consta de una máscara ocular con dos parches rígidos sobre los ojos. Cada parche tiene 19 diodos luminosos que emiten radiación casi infrarroja de 850 a 1050 nm, con un pico a 940 nm. El dispositivo de compresión caliente con infrarrojos se utilizó para tratar a 37 sujetos con DGM obstructiva en una serie de casos prospectivos intervencionistas no comparativos durante 5 minutos, dos veces al día, durante 2 semanas con los párpados cerrados. Las puntuaciones totales de los síntomas subjetivos mejoraron y también se produjo una mejora significativa en las tasas de evaporación lagrimal durante el parpadeo forzado, la tinción con ?uoresceína y con rosa de bengala y la puntuación de la obstrucción de los orificios glandulares [458].
3.2.3. Tratamientos físicos
El objetivo de aplicar tratamiento físico a las glándulas de Meibomio consiste en mejorar y/o restaurar la función de las glándulas mejorando o eliminando la obstrucción de los conductos, permitiendo así que las glándulas vuelvan a ser plenamente funcionales [459]. El exprimido para la mejora terapéutica del material obstructivo no se debe confundir con el exprimido diagnóstico, en el que se utilizan fuerzas mínimas para determinar si la glándula es funcional [441].
Existen tres métodos establecidos para tratar físicamente la obstrucción de los conductos; las compresas calientes y distintos dispositivos de calentamiento emplean calor para elevar la temperatura con el fin de suavizar o preferiblemente licuar el material obstructivo; la fuerza física se emplea para comprimir las glándulas con el fin de exprimir físicamente el material de la glándula obstruida, y la exploración intraductal introduce un fino cable en el orificio obstruido y luego emplea la fuerza para expulsar el material obstructivo.
3.2.3.1. Exprimido forzado.
Existe un largo historial que describe diversos métodos para el exprimido forzado de las glándulas de Meibomio sin la aplicación de calor [460 - 462]. Estos métodos incluyen el aislamiento del párpado para exprimirlo entre los dedos del examinador y aplicar fuerza apretando los parpados uno contra el otro o bien utilizando un objeto rígido en la superficie interior del párpado y el pulgar, el dedo u otro objeto rígido en el párpado exterior para aplicar fuerza [460,463]. Sin embargo, un factor limitante en todos estos métodos es el dolor que experimenta el paciente, que solo se alivia mínimamente con anestésicos tópicos. La cantidad de dolor aumenta rápidamente a medida que la fuerza de expresión supera las 5 libras por pulgada cuadrada (pounds per square inch, PSI) [464]. La máxima fuerza tolerable habitual es de 15 PSI, que, con frecuencia, es marginal o inadecuada para exprimir material obstructivo [464].
Un estudio investigó la eficacia de cuatro exprimidos forzados en la consulta durante un periodo de 6 meses junto con el tratamiento de compresión con calor diario [461]. El número de glándulas exprimibles, la calidad de la secreción y el grosor de la capa lipídica mejoraron de forma significativa y todos los pacientes notificaron una mejora del confort y una disminución de los síntomas asociados a la EOS [461].
3.2.3.2. LipiFlow.
LipiFlow® TearScience, Morrisville, NC, EE. UU.) se diseñó para evitar los impedimentos de la transferencia de calor a través del tejido del párpado y al mismo tiempo evacuar el contenido glandular, a la vez que se calientan las glándulas a niveles terapéuticos de 42,5 °C [459,465]. Se ha demostrado, en ambos ensayos clínicos aleatorizados y no controlados, que el procedimiento único de 12 minutos del sistema LipiFlow® es seguro y efectivo para tratar la DGM y que el efecto se puede mantener [465]. El primer estudio prospectivo, abierto, aleatorizado, cruzado y multicéntrico comparó un único tratamiento Lipi- Flow® con el tratamiento diario de compresas calientes [459]. El grupo que se sometió al tratamiento con LipiFlow® mostró una mejoría significativa de los síntomas, la secreción de la glándula de Meibomio y el TDL al cabo de un mes, mientras que el grupo de compresas calientes mostró una mejora solo de los síntomas. Después de recibir el tratamiento cruzado, el grupo de las compresas calientes también demostró una mejora significativa en la función glandular y el TDL.
Más recientemente, un ensayo clínico prospectivo aleatorizado cruzado y con enmascaramiento para el observador comparó un único tratamiento de LipiFlow® con un régimen sólido de 3 meses de compresas calientes dos veces al día combinado con masaje e higiene del párpado [72]. Estos sujetos fueron evaluados durante seis meses, demostrando que un único tratamiento con LipiFlow® funciona al menos tan bien como el régimen riguroso de higiene, calor y masaje y que los efectos del tratamiento único con LipiFlow® se mantuvieron durante seis meses [466]. Un ensayo clínico prospectivo multicéntrico abierto de 12 semanas de duración más reciente aleatorizó a 200 sujetos (400 ojos) y notificó que el efecto del tratamiento único con LipiFlow®, con una mejora de la función glandular y de los síntomas de ojo seco, se puede mantener durante un máximo de 12 meses [467]. Un estudio observacional no controlado y de un único centro detectó una mejora significativa y sostenida de la función de la glándula de Meibomio y de los síntomas durante un máximo de 3 años después de un único tratamiento [468].
3.2.3.3. Luz pulsada intensa (LPI).
Se ha utilizado luz pulsada intensa (LPI) en dermatología para suministrar pulsos intensos de luz con una longitud de onda no sistemática de 500 nm a 1200 nm para tratar diversas afecciones, incluida la pigmentación de la piel, el daño por el sol y el acné [469]. Un flash manual controlado por ordenador administra la luz apropiada, que se filtra para la acción específica.
La LPI se describió por primera vez de forma anecdótica hace más de 15 años para el tratamiento de la DGM. Un estudio prospectivo, con doble enmascaramiento, controlado con placebo y de pares de ojos realizado más recientemente comparó el efecto de múltiples pulsos de LPI en un ojo, mientras el otro recibía un tratamiento simulado. El tratamiento aportó una mejoría en la calidad de la película lagrimal y una reducción de los síntomas [470]. Un análisis retrospectivo de historias clínicas ha demostrado de forma independientemente una mejora del 77 % en la función de la glándula de Meibomio en al menos un ojo y una mejora del 89 % en los síntomas del ojo seco cuando se usó la LPI en combinación con el exprimido manual de la glándula de Meibomio [471]. Una revisión de cohortes retrospectiva y multicéntrica de 100 pacientes con DGM tratados con LPI mostró mejoras clínicas similares y concluyó que el tratamiento con LPI era un tratamiento seguro y eficaz para el OSE [472].
3.2.3.4. Exploración intraductal.
La exploración intraductal de la glándula de Meibomio se describió por primera vez en 2010 [473]. Esta publicación inicial comunicó datos de una revisión retrospectiva de historias clínicas de 25 pacientes consecutivos que presentaban en todos los casos signos y síntomas de DGM obstructiva. 24 de los 25 pacientes experimentaron un alivio inmediato después de la exploración, y todos los pacientes experimentaron un alivio de los síntomas al cabo de 4 semanas después del procedimiento. Cinco pacientes requirieron una o dos sesiones de tratamiento. Los pacientes que se sometieron a un único tratamiento fueron objeto de seguimiento durante una media de 11,5 meses después del tratamiento. Ninguno de los pacientes presentaba síntomas en la última visita de seguimiento [473]. Un estudio prospectivo y longitudinal realizó la exploración de un ojo en 16 personas que presentaban DGM, mientras que el otro ojo se utilizó como control. El tiempo de desintegración, el dolor y la fotofobia mejoraron a la semana y a los 6 meses después del tratamiento [474]. Un estudio de tres pacientes con DMG obstructiva resistente investigó la cantidad y el cambio en la viscosidad del meibum después de la exploración. Todos los pacientes mostraron mejoras en los niveles lipídicos y en la viscosidad, y 2 de los 3 mostraron una mejora del TDL [475]. Un estudio también informó de la mejora de los síntomas después de la exploración de 10 pacientes con rosácea ocular, DGM y enfermedad de la superficie resistente a la gestión convencional. Los síntomas mejoraron en aproximadamente el 50 % de los sujetos al cabo de 1 y 6 meses, la doxiciclina se interrumpió en 9 de los 10 pacientes y todos los pacientes notificaron una reducción del uso de lubricantes oculares [476].
Pese a que es necesario realizar más investigaciones, especialmente a la vista de la naturaleza invasiva del procedimiento, la posibilidad del daño al complejo sistema de conductos y el tamaño reducido de la muestra de sujetos de los que se ha informado hasta la fecha, los datos notificados sugieren que la exploración intraductal puede ofrecer alivio a los pacientes de DGM que no respondan al tratamiento convencional.
3.2.3.5. Raspado de desbridamiento.
Uno de los principales mecanismos que impulsan la obstrucción de las glándulas de Meibomio es la hiperqueratinización del margen del párpado y los orificios de los conductos [477]. A medida que el material queratinizado se acumula en torno al orificio y en su interior, la glándula se obstruye y no puede suministrar meibum a la película lagrimal. El desbridamiento de la línea de Marx, que marca la unión mucocutánea y el margen queratinizado del párpado, se notificó por primera vez en 2013 [478]. Se cree que esta técnica funciona eliminando mecánicamente los restos acumulados y las células queratinizadas del margen del párpado para permitir un mayor flujo de meibum a la película lagrimal. El estudio prospectivo con enmascaramiento para el investigador realizado por Korb y colegas incluyó un grupo de prueba de 16 sujetos y un grupo de control de 12 sujetos, todos con síntomas de ojo seco y cambios visibles en la línea de Marx [478]. La línea de Marx tintada y la achura entera del margen queratinizado del párpado inferior se desbridaron en el grupo de prueba utilizando un rascador en forma de palo de golf de acero inoxidable. Un mes después del tratamiento se produjeron mejoras significativas de los síntomas en el 22 % de los sujetos, mientras que la función de la GM mejoró significativamente en el 46 % de los sujetos [478]. Recientemente se ha publicado un estudio piloto prospectivo, aleatorizado, sin enmascaramiento y controlado para determinar el efecto del desbridamiento del párpado en sujetos con síndrome de Sjögren [479]. Los 14 sujetos eran mujeres; siete de ellas fueron aleatorizadas al grupo de tratamiento y siete eran controles. Un mes después del raspado de desbridamiento, los sujetos notificaron mejoras de los síntomas, se redujo la tinción ocular y se demostró el restablecimiento de la función de la glándula de Meibomio [479].
Se debe considerar la falta de tratamiento simulado y de enmascaramiento en ambos estudios notificados [478,479]. Se necesitan estudios más grandes y diseños de estudio adicionales para confirmar los mecanismos de acción que expliquen los resultados positivos notificados hasta la fecha.
3.3. Anomalías en el parpadeo y exposición ocular
El parpadeo incompleto o la imposibilidad de cerrar los ojos del todo durante el sueño puede provocar el secado de la superficie ocular [480 - 482] y, por tanto, merece la pena considerar medidas apropiadas para abordar cualquier anomalía en el parpadeo o el cierre de los párpados en la gestión del paciente con signos o síntomas de EOS.
En el informe sobre fisiopatología de TFOS DEWS II se incluyen más detalles sobre el impacto de patrones de parpadeo o cierre del ojo anormales con EOS [483].
3.3.1. Tratamiento de la exposición corneal
Los estudios que investigan los tratamientos para cualquier forma de cierre inadecuado de los párpados son, en su mayoría, de nivel 3 [481,484 - 487] e incluyen la evaluación de suplementos lagrimales, pomadas (normalmente aplicadas por la noche), gafas de humedad, protectores oculares nocturnos que logran el cierre mecánico de los párpados y el cierre forzado temporal de los párpados mediante el uso de parches o cinta. Para aquellos que no estén dispuestos o no puedan pegarse físicamente los párpados con cinta durante la noche, como personas con dermatitis por contacto o preocupadas por la depilación iatrogénica de las pestañas [481,484], existen métodos alternativos. Estos métodos incluyen copas oculares de distintos diseños y materiales y el uso de finas películas de polímero (como envoltorio de plástico para alimentos). La evidencia de nivel 1 sugiere que la película proporciona una mejor protección para la córnea expuesta que los lubricantes, con menos complicaciones que estos [488]. Se ha informado de que el cierre mecánico de los párpados por diversos métodos en poblaciones de enfermos críticos iguala o mejora la protección de la córnea expuesta, con menos complicaciones que los lubricantes [488,489]. Sin embargo, aunque se acepta universalmente que el cierre mecánico de los párpados es obligatorio para la gestión de la queratopatía grave por exposición, no existen estudios clínicos controlados, aleatorizados y prospectivos con el fin de establecer la eficacia o la superioridad de distintos tratamientos.
Los casos persistentes o graves de exposición corneal pueden requerir uno de varios procedimientos quirúrgicos, incluida la implantación de pesos en los párpados superiores [481,490,491], muelles para párpados, reconstrucción de párpados o tarsorrafía parcial/completa. Las lentes esclerales rígidas permeables gases también pueden ser una opción en casos de queratitis por exposición, tal como se detalla en la sección 3.3.3.2.
3.3.2. Entropión y ectopión
El entropión y el ectopión causan exposición de la superficie ocular, y el entropión con frecuencia provoca triquiasis concurrente, causante de síntomas del ojo seco [492]. La parálisis del nervio facial provoca el ectropión del párpado inferior paralítico y retracción del párpado superior debido a la menor actividad del músculo orbicularis oculi. Otras causas incluyen trauma, tumores, cirugía facial y laxitud del párpado relacionada con la edad.
La gestión tanto del entropión como el ectropión suele ser quirúrgica y las técnicas incluyen endurecimiento de los tendones cantales y la eliminación de una cicatriz u otra razón mecánica para la colocación incorrecta del párpado [493 - 497]. En un estudio de nivel 2, la corrección del entropión mejoró la visión, la queratopatía punteada y el TDL, pero no los resultados de Schirmer [498]. Un estudio adicional de nivel 2 demostró que la tarsorrafía fue un procedimiento exitoso para el entropión y respaldó la curación epitelial en ojos con sequedad grave [499].
3.3.3. Lentes de contacto
El uso de lentes de contacto para la corrección del error refractivo en ojos sanos puede ir acompañado de síntomas de sequedad y molestias, y las opciones para la gestión de estas molestias se han abordado en detalle en otros trabajos [500]. A pesar de estar asociadas con la sequedad, las lentes de contacto tienen un papel potencial en la gestión de la EOS. En el marco del informe TFOS DEWS original, el uso de lentes de contacto se enumeró junto con la oclusión permanente del conducto lagrimal y las lágrimas de suero como opciones para la EOS más avanzada [1]. La principal razón por la que el uso de lentes de contacto se reservó para la gestión de formas más graves de EOS es reconocer que la ESO y el uso de lentes de contacto son factores de riesgo por separado para la queratitis microbiana, aunque se desconoce el factor de riesgo compuesto. Aún debe explicarse en detalle el mecanismo por el que el uso de lentes de contacto es terapéutico, pero algunos aspectos relevantes son la protección mecánica y la reducción de la desecación corneal.
En la decisión de utilizar lentes de contacto en la gestión terapéutica de la EOS se deben considerar los riesgos y beneficios del caso concreto. Han aparecido informes de la queratitis microbiana ocurrida en pacientes usuarios de lentes de contacto para la gestión de la ESO [501], incluidos casos que progresaron a endoftalmitis [502]. Las lentes de contacto utilizadas para la EOS grave suelen usarse durante periodos prolongados, lo que se asocia a un mayor riesgo de queratitis microbiana con respecto al uso diario [503 - 506].
La gestión de la EOS se puede realizar con lentes blandas o rígidas. Dependiendo de la gravedad y la naturaleza de la ESO, las lentes de contacto blandas terapéuticas, que a menudo se denominan lentes de contacto de tipo vendaje, pueden prescribirse para uso a corto plazo (días) o a largo plazo (años) y se pueden usar a diario o durante periodos prolongados de tiempo.
3.3.3.1. Lentes de contacto blandas terapéuticas (lentes de tipo venda).
La finalidad de las lentes de contacto de tipo venda es mejorar el confort ocular y reducir los efectos de un entorno adverso. La disponibilidad de materiales de lentes blandas de hidrogel de silicona, con una alta capacidad de transmisión de oxígeno, ha fomentado la aplicación de estos dispositivos para el tratamiento terapéutico de la EOS, y normalmente se usan de forma prolongada [507].
Las lentes de contacto de venda se consideran una opción de tratamiento complementaria útil para diversas patologías de la superficie ocular, incluida la erosión corneal recurrente [508], la abrasión corneal [509], la queratopatía bullosa [510] y el posoperatorio de la cirugía corneal [511 - 514]. Se ha sugerido que las lentes de contacto de venda pueden estabilizar la película lagrimal y ayudan a restaurar la renovación de las células epiteliales [515] y potencialmente ayudar en la gestión del dolor corneal aislando nervios corneales sensibilizados por la estimulación ambiental [516,517]. El mecanismo exacto por el que las lentes de contacto de venda alivian el dolor no se ha esclarecido, pero es probable que implique el blindaje directo de los nociceptores en la superficie ocular o el respaldo de la estructura celular y de los elementos de la matriz extracelular que ejercen de blindaje. Puede producirse un efecto protector en la prevención del secado o el enfriamiento de la superficie ocular o en el blindaje de los nociceptores de la superficie ocular frente al trauma relacionado con la conjuntiva palpebral o tarsiana, por ejemplo en enfermedades de cicatrización. El uso de lentes de contacto blandas de vendaje para la OES está respaldado por la evidencia de nivel 3 de que se puede lograr el alivio del dolor con lentes de contacto blandas de vendaje en enfermedades corneales distintas de la EOS [518], por ejemplo, cuando existe un dolor nociceptivo después de un trauma o una cirugía [519].
Actualmente existe una escasez relativa de literatura sobre la aplicación específica de lentes de contacto de vendaje para el tratamiento de la EOS. Un reciente estudio prospectivo aleatorizado (de nivel 1) en 40 sujetos con síndrome de Sjögren que comparó la eficacia de las lentes de contacto de vendaje con el suero autólogo concluyó que las lentes de contacto de hidrogel de silicona (utilizadas como lentes de contacto de vendaje) no eran eficaces para la gestión de la EOS asociada al síndrome de Sjögren [223]. Al cabo de seis semanas, los sujetos con lentes de contacto de vendaje experimentaron una mejora significativa en la máxima agudeza visual corregida (que permaneció estable durante un máximo de seis semanas después de interrumpir el uso de lentes de contacto), así como una mejora significativa de las puntuaciones de IESO, en comparación con los sujetos tratados con suero autólogo. Ambos grupos de intervención también mostraron mejoras relativas en las puntuaciones de la calidad de vida, del tiempo de desintegración lagrimal y de la tinción corneal en comparación los valores iniciales; no se observó ningún acontecimiento adverso en el grupo. Además, en un estudio de nivel 2 en el que participaron 7 pacientes con GVHD y EOS de moderada a grave, el uso de lentes de hidrogel de silicona, utilizadas siete noches seguidas durante un mes, redujo los síntomas de ojo seco y mejoró la agudeza visual con respecto a antes del tratamiento [515].
El tratamiento oportuno de cualquier epiteliopatía corneal se considera importante para minimizar el riesgo de desarrollar dolor crónico; una vez que se ha producido la centralización del dolor neuropático, unas lentes de contacto de vendaje, que podrían reducir la señalización periférica, pueden no ser suficientes para reducir los síntomas [516].
3.3.3.2. Lentes de contacto rígidas permeables a gases.
Existe una impresión cada vez mayor de que el uso diario de lentes esclerales rígidas permeables a gases puede desempeñar un papel importante en la gestión de la EOS de moderada a grave, posiblemente debido al hecho de que pueden proporcionar un depósito de lágrimas entre las lentes y la superficie ocular. El uso de lentes esclerales se ha investigado en otras afecciones como la GVHD crónica [520 - 522] y el síndrome de Stevens-Johnson [523]. El uso de lentes esclerales como un dispositivo protésico en una serie de pacientes, incluidos aquellos con EOS, se notificó por primera vez en Estados Unidos en 1990 [524], con informes similares aparecidos por todo el mundo esa misma década [525,526]. Una serie de casos (evidencia de nivel 3) ha descrito la aplicación a largo plazo de lentes de contacto esclerales como una alternativa a la tarsorrafía en tres pacientes que habían desarrollado lagoftalmos unilateral y anestesia corneal secundaria a la parálisis de los nervios faciales después de la cirugía [527]. Se informó de que la modalidad de las lentes esclerales proporcionaba una protección eficaz de la superficie ocular y la optimización de la función visual en estos pacientes. El uso de lentes esclerales para la ESO se notificó de forma más amplia en diversas revisiones [528 - 530].
Estudios clínicos recientes refirieron el éxito en la gestión de la EOS con lentes esclerales, lentes miniesclerales y PROSE (Reemplazo protésico del ecosistema de la superficie ocular, Prosthetic Replacement of the Ocular Surface Ecosystem) [520,522,527,531 - 538].
4. Tratamiento antiinflamatorio volver arriba
4.1. Glucocorticoides tópicos
Los corticosteroides se han utilizado con éxito en el tratamiento de una amplia variedad de enfermedades inflamatorias, incluida la EOS.
4.1.1. Investigación básica
El estrés desecante puede inducir el daño en la superficie ocular y generar respuestas inmunitarias innatas o adaptativas. Estas cascadas inflamatorias conducen a un mayor daño de la superficie ocular y al desarrollo de un ciclo inflamatorio que se autoperpetúa. La inflamación también puede causar alteraciones en la neurobiología de la superficie ocular, tal como se describe en el informe sobre dolor y sensación de TFOS DEWS II [539].
Se ha determinado que los esteroides son útiles en la modulación del dolor neuronal, que puede resultar beneficioso en la gestión del dolor neuropático, pero esta modulación no se ha evaluado en el ojo [540]. Queda claro a raíz de los numerosos estudios experimentales en modelos animales que los corticosteroides tópicos son eficaces en la ruptura del círculo vicioso de respuestas inmunitarias en la EOS. El tratamiento tópico con metilprednisolona (1 %) suprimió la expresión de citocinas inflamatorias y MMP-9, así como la activación de la proteína cinasa activada por mitógenos en el epitelio corneal de ojo seco murino experimental. Como consecuencia, disminuyó la descamación de células epiteliales corneales apicales y se mantuvo la integridad de las zonulas occludens del epitelio corneal [541,542]. En la EOS inducida por la inyección de toxina botulínica B en la glándula intralagrimal en un modelo de ratón, la fluorometolona tópica al 0,1 % sola o en combinación ciclosporina A fue capaz de restablecer parcialmente la producción lagrimal y de mejorar de forma significativa la superficie ocular [543]. Estudios murinos han explorado nuevos agentes terapéuticos para la EOS. Un estudio mostró que se observó una reducción significativa de la tinción corneal con fluoresceína después del tratamiento tópico con metilprednisolona al 1 %, antagonista de interleucina (IL)-1R al 5 % y ciclosporina A al 0,05 % [544]. También se demostró una reducción significativa en los números de células CD11b+ corneales centrales, en el crecimiento linfático corneal y en la expresión de IL-1β corneal tras el tratamiento con un antagonista de IL-1R y metilprednisolona, que no se observó después del tratamiento con el vehículo [544].
También se pueden usar agonistas selectivos del receptor de glucocorticoides como objetivo terapéutico para la EOS. En el ojo seco inducido por atropina de un modelo en conejos, los agonistas selectivos del receptor de glucocorticoides y la dexametasona al 0,1 % fueron totalmente eficaces, manteniendo el volumen y el tiempo de desintegración lagrimales [545]. Ninguno de los agentes mostró efectos sobre la presión intraocular (PIO) o en el peso corporal, mientras que la dexametasona aumentó de forma significativa la PIO e inhibió el aumento de peso corporal debido al desgaste muscular [545]. Además, la inhibición selectiva del receptor de ciclooxigenasa-2/eicosanoides-prostanoides (receptor COX-2/EP) se sugiere como un objetivo terapéutico en un modelo murino de EOS [546]. Los inhibidores tópicos del receptor COX-2/EP reducen el número de células CCR7+CD11b+ en la superficie celular con inhibición del alojamiento de ganglios linfáticos celulares y la supresión de respuestas inmunitarias impulsadas por Th17. La pérdida de células calciformes conjuntivales inducida por el ojo seco se revirtió, y la erosión corneal mejoró con cada uno de los tratamientos tópicos [546].
4.1.2. Estudios clínicos
Se pueden utilizar distintos preparados de corticosteroides tópicos para modular la inflamación del segmento anterior, y múltiples estudios han demostrado el valor clínico de su uso a corto plazo en la gestión de la EOS. Se han publicado varios ECA que investigan el valor de usar varias fórmulas de corticosteroides para la gestión de la EOS (Tabla 8) [547 - 557].
Recientemente ha surgido interés en que el diagnóstico por imagen (en lugar de las evaluaciones clínicas que normalmente se asocian a la evaluación del ojo seco) también puede ser valioso a la hora de establecer el potencial predictivo para la gestión de la EOS con corticosteroides tópicas [555,558].
4.1.3. Complicaciones
Pese a que parece que los corticosteroides tópicos pueden ser valiosos para la gestión de la EOS, su uso a largo plazo no está exento de riesgo de complicaciones. Estas complicaciones incluyen hipertensión ocular, cataratas e infecciones oportunistas, incluso después de breves periodos de uso [547]. Para pacientes con enfermedad de moderada a grave que no se controla con otros tratamientos, el tratamiento repetido con pulsos de corticosteroides a corto plazo puede ser un enfoque alternativo. Cincuenta y tres pacientes con síndrome de Sjögren fueron tratados con metilprednisolona tópica al 1 % sin conservantes cuatro veces al día durante 2 semanas, tras lo cual fueron reevaluados y se redujo la medicación hasta que dejaron de mostrar tinción corneal con ?uoresceína o síntomas [559]. La mayor parte de los pacientes se encontraban en un estado libre de enfermedad durante un periodo relativamente largo (57 semanas) después del primer tratamiento de pulsos, y 11 individuos (21 %) experimentaron una recurrencia de los síntomas o los signos. Después del segundo tratamiento de pulsos, se observó un periodo libre de enfermedad de 72 semanas y solo el 1,9 % de los pacientes presentó recurrencia. No se encontraron complicaciones graves (como elevación de la PIO o formación de cataratas) durante todo el periodo de seguimiento [559].
También se puede considerar el uso de esteroides tópicos como fluorometolona y loteprednol, que tienen una menor probabilidad de aumentar la PIO y de inducir la formación de cataratas [560 - 562]. Sin embargo, se ha descrito que incluso la fluorometolona causa cataratas después de un periodo de aplicación continuo de 4 meses [563]. Un reciente estudio de seguridad retrospectivo en el que se recogían 77 estudios publicados concluyó que el tratamiento tópico con loteprednol etabonato tiene un efecto mínimo en la PIO cuando se usa en el tratamiento de una amplia variedad de trastornos inflamatorios intraoculares y de la superficie ocular, incluida la alergia ocular, EOS, uveitis anterior, queratoplastia penetrante, queratoplastia endotelial y dolor posoperatorio después de la cirugía ocular [564].
4.1.4. Pretratamiento con esteroides
En un ECA prospectivo multicéntrico con doble enmascaramiento, el tratamiento con loteprednol al 0,5 % dos semanas antes del inicio de la ciclosporina tópica al 0,05 % a largo plazo proporcionó una mejora más rápida de la puntuación Schirmer, de la tinción corneal con ?uoresceína, de la tinción con verde de lisamina y de los síntomas en comparación con la ciclosporina tópica o las lágrimas artificiales solas [554]. El tratamiento de inducción con loteprednol etabonato redujo de forma significativa la incidencia de tinción grave y la interrupción de ciclosporina tópica [554]. De forma similar, el tratamiento con metilprednisolona tópica al 1 % y ciclosporina durante un periodo inicial de tres semanas proporcionó un alivio más rápido de los síntomas y una mejora más rápida de los signos oculares que la ciclosporina tópica sola [565].
4.1.5. Opciones sin conservantes
Está generalmente aceptado que el uso de conservantes en la EOS es perjudicial para la superficie ocular [98,566,567] y, por tanto, está creciendo el uso de esteroides tópicos sin conservantes. En un estudio de casos y controles, aleatorizado y de grupos paralelos, la eficacia del AH al 0,1 % sin conservantes y de la fluorometolona 0,1 % en combinación con ciclosporina al 0,05 % se comparó con la eficacia del AH al 0,1 % con conservantes y la fluorometolona 0,1 % en combinación con ciclosporina al 0,05 %, en el tratamiento de la EOS [118]. Los colirios sin conservantes mejoraron los síntomas subjetivos, el TDL, la puntuación Schirmer y los hallazgos de la citología de impresión en mayor medida que los colirios conservados [118]. De forma similar, una revisión retrospectiva de 31 pacientes tratados con dexametasona tópica al 0,01 % con conservante mostró una mejora subjetiva de los síntomas en el 84 % de los sujetos con irritación crónica de la superficie ocular y/o lagrimeo resistente a varios esteroides tópicos con conservante, incluidos loteprednol al 0,2 %, ?uorometolona al 0,1 % y prednisolona al 1 % [553]. En el informe sobre ojo seco iatrogénico de TFOS DEWS II se dan más detalles sobre este tema [102].
4.1.6. Esteroides sexuales
Un cuerpo considerable de ciencia básica e investigación clínica ha investigado los papeles de los esteroides sexuales (andrógenos, estrógenos y progestinas) en la regulación de los tejidos de la superficie ocular y los anejos. Estudios clínicos han explorado la eficacia de estas hormonas en el tratamiento de la EOS. Esta información se detalla en el informe sobre sexo, género y hormonas de TFOS DEWS II [353].
4.2. Inmunomoduladores no glucocorticoides
Con la excepción de la ciclosporina, comparativamente se han realizado pocos ensayos clínicos utilizando medicamentos inmunomoduladores en personas con EOS, pero la demostración de la eficacia con este grupo terapéutico ofrece potencialmente claves importantes sobre la patogénesis de la enfermedad y puede estimular la investigación adicional que podría conducir al desarrollo comercial de compuestos que pueden ofrecer un beneficio demostrable al paciente.
4.2.1. Ciclosporina A
El informe inicial de TFOS DEWS advirtió la importancia de la inflamación de la superficie ocular no solo en el desarrollo de la EOS, sino también en un efecto descendente y propagador de la enfermedad, y revisó diversos tratamientos que funcionan, al menos en parte, mediante mecanismos de acción antiinflamatorios [1].
Se entiende que la ciclosporina es un fármaco inmunomodulador con propiedades antiinflamatorias, además de tener otras acciones relevantes para la gestión de la EOS [568 - 570]. La ciclosporina es un antimetabolito fúngico que inhibe la activación de linfocitos con IL-2 [570]. Se utiliza de forma sistemática como un tratamiento anti rechazo en pacientes con trasplantes de órganos [571,572] y en enfermedades autoinmunes [573,574], así como tópicamente en el tratamiento de patologías alérgicas, atópicas, disfunción de las células madre del limbo y enfermedad inflamatoria ocular autoinmune [575 - 578]. La ciclosporina tópica fue aprobada por la FDA para el tratamiento de la EOS de moderada a grave en 2003, basándose en una mejora de la producción lagrimal medida por la prueba de Schirmer en el 15 % de los pacientes en comparación con el 5 % de los controles tratados con el vehículo. El tratamiento con ciclosporina reduce muchos marcadores de inflamación [579,580] y también reduce una osmolaridad lagrimal elevada [63]. La ciclosporina también tiene efectos anti-apoptóticos relevantes para la anulación de la normal relación de las células epiteliales/leucocitos en la EOS [581,582], un efecto que no produce el tratamiento con corticosteroides [583 - 585]. Adicionalmente, se ha informado de que el tratamiento con ciclosporina provoca una recuperación de la disminución de la densidad de células calciformes en la conjuntiva de sujetos con EOS [586,587].
Se han publicado diversos estudios de nivel 1 [588 - 591] y nivel 2 [592,593] (Tabla 9) y varios metanálisis [594 - 597] (Tabla 10) que respaldan la eficacia de la ciclosporina en la gestión de la EOS. Sin embargo, las medidas de los resultados (tanto los síntomas como los signos) y las escalas de clasificación difieren sustancialmente entre los estudios, lo que dificulta las comparaciones del trabajo publicado. No obstante, tomado como un cuerpo de trabajo, existen fuertes evidencias de nivel 1 para respaldar el uso de ciclosporina tópica en el tratamiento de EOS. Sin embargo, existen diversas exclusiones y salvedades. Es importante advertir que se ha notificado que la ciclosporina A carece de eficacia para el tratamiento de la EOS provocada por procedimientos quirúrgicos, el uso de lentes de contacto y en la orbitopatía tiroidea, y además ha demostrado una mejora del daño en la superficie ocular en solo el 53 % (9/17) de los ensayos clínicos aleatorizados [595].
Los estudios sobre la calidad de vida han concluido que la ciclosporina tópica es rentable para el tratamiento de la EOS en comparación con el uso de lubricantes oculares [598]. Un estudio de Nivel 1 también ha informado del valor añadido del tratamiento con ciclosporina tópica en pacientes equipados con tapones lagrimales [306]. Menos estudios han diferenciado entre pacientes de OSDA y aquellos con OSE, pero varios estudios de nivel 1 [599 - 602] (Tabla 11) han notificado resultados positivos (de nuevo, con distintas escalas y medidas de los resultados) tras el tratamiento con ciclosporina para la EOS evaporativa/DGM.
El tratamiento de pacientes con EOS utilizando ciclosporina tópica debe continuar durante periodos prolongados de tiempo, tal como evidencia la baja frecuencia de una “cura” clínica (ausencia de síntomas después de la interrupción del fármaco) [603]. La mala solubilidad en agua de la ciclosporina dificulta la formulación en un colirio tópico. Recientemente ha salido al mercado una formulación nueva de ciclosporina al 0,1 % en una emulsión catiónica de una única dosis sin conservante en Europa [604]. La fórmula del fármaco activo era superior al vehículo en el cambio de la tinción corneal con fluoresceína desde el inicio y en la reducción de la inflamación, tal como evidencia la respuesta del antígeno leucocitario humano relacionado con D (human leukocyte antigen D-related, HLA-DR), durante 6 meses, pero no se produjo ningún cambio de los síntomas con el tiempo según el IESO, y el 29 % de los sujetos seguían experimentando molestias con la instilación, en comparación con el 9 % de sujetos que utilizaban el vehículo [604].
4.2.2. Tacrolimus
El tacrolimus, un macrólido producido por Streptomyces tsukubaensis, fue descubierto en 1984 en Japón mientras se buscaban nuevos agentes inmunosupresores y quimioterapéuticos contra el cáncer. Al igual que la ciclosporina, bloquea la actividad de los linfocitos T, pero su potencial inmunosupresor es superior al de la ciclosporina [605].
En un estudio abierto y prospectivo con 14 pacientes con GVHD con EOS grave e intolerancia a la ciclosporina tópica, los pacientes recibieron instrucciones para instilar tacrolimus tópico al 0,03 % una vez al día durante tres meses [606]. Los síntomas y signos del ojo seco mejoraron de forma significativa con tacrolimus, y los autores concluyeron que el tacrolimus tópico al 0,03 % puede ser una alternativa viable para pacientes con intolerancia a la ciclosporina tópica o en pacientes en los que la respuesta a la ciclosporina tópica es mala. En un estudio prospectivo con doble enmascaramiento de tacrolimus tópico al 0,03 % instilados dos veces día en 24 pacientes con ojo seco relacionado con el síndrome de Sjögren, las puntuaciones de la tinción corneal media con ?uoresceína y con rosa de bengala mejoraron estadísticamente al cabo de siete días de tratamiento y siguieron mejorando durante 90 días [607]. Los valores de Schirmer y TDL no cambiaron hasta 21 días después del tratamiento, pero mostraron una mejoría después de 28 días de tratamiento con respecto al inicio.
4.2.3. Fármacos antiinflamatorios no esteroideos
Se han utilizado diversos fármacos antiinflamatorios no esteroideos (AINE) para el tratamiento de la EOS, incluidos pranoprofeno al 0,1 % [608], diclofenaco al 0,1 % [609,610], ketorolaco al 0,4 % [611] e indometacina al 0,1 % [610]. El efecto osmoprotector de distintos AINE fue evaluado por Sawazaki et al. en un modelo en ratas [612]. El diclofenaco fue capaz de suprimir la apoptosis inducida por la hiperosmolaridad y detener el crecimiento celular. Por contraste, el bromfenac no ejerció esta acción protectora.
Los ensayos clínicos demostraron que el uso de AINE va seguido de una reducción de las molestias oculares en pacientes con EOS [613]. Sin embargo, se han publicado informes de casos esporádicos en personas con EOD grave [614]. Por tanto, la mayoría de los estudios publicados con AINE en la EOS tienen una duración que no supera el mes [608,611,613], a pesar de que la EOS es una enfermedad crónica. Se ha estudiado el efecto del tratamiento con AINE sobre la sensibilidad corneal en sujetos normales y en pacientes con EOS. Los resultados de estos ensayos parecen demostrar que algunos AINE, en particular el diclofenaco, tienen el efecto de reducir la sensibilidad corneal tanto en sujetos normales como en sujetos con ojo seco [615]. Por lo tanto, se ha sugerido que los AINE deben usarse con precaución en pacientes con síndrome de Sjögren [610,616].
En un ensayo clínico con enmascaramiento simple, aleatorizado y prospectivo realizado en 32 pacientes con QCS con o sin síndrome de Sjögren, Avunduk et al. investigaron si las gotas antiinflamatorias (corticosteroides y AINE) tienen efectos terapéuticos [549]. Los sujetos aleatorizados para recibir lágrima artificial más gotas de corticosteroides tópicas tuvieron puntuaciones significativamente más bajas en la gravedad de los síntomas, tinción corneal con ?uoresceína, tinción con rosa de bengal, y células positivas para HLA-DR a los 15 y 30 días en comparación con los sujetos de los grupos de control. Los autores concluyeron que los corticosteroides tópicos tuvieron un efecto beneficioso en los síntomas y signos en la EOS de moderada a grave, pero no así los AINE tópicos [549].
4.2.4. Productos biológicos
4.2.4.1. Lubricina.
La lubricina (proteoglicano 4) es una glicoproteína lubricante similar a la mucina que se identificó por primera vez en el líquido sinovial [617]. Más recientemente, se ha descubierto lubricina en la superficie ocular y en las glándulas de Meibomio [618]. Se trata de un lubricante altamente efectivo que reduce la fricción de los bordes en superficies sintéticas y tisulares, funciona de forma sinérgica con AH [619 - 621] y posee propiedades antiinflamatorias [622 - 624]. La lubricina ha demostrado reducir la fricción y prevenir la tensión de cizalladura en la interfaz córnea-párpado, mientras que el déficit de lubricina conduce a un aumento de la tensión por cizalladura y la tinción corneal [618]. Recientemente se ha generado y caracterizado la lubricina recombinante de longitud completa in vitro [625].
Actualmente, no hay disponibles en el mercado lubricantes a base de lubricina. Un reciente estudio aleatorizado de grupos paralelos con doble enmascaramiento y de dos semanas de duración realizado en 39 sujetos con EOS moderada comparó la fórmula tópica de la lubricina humana recombinante con un colirio de AH al 0,18 % [626]. Se determinó que la lubricina humana recombinante logró una mejora significativa en los signos y los síntomas de EOS en comparación con el AH, con mejoras significativas en diversas variables clínicas, incluido el TDL, la tinción corneal con corneal ?uoresceína y el enrojecimiento del párpado y la conjuntiva.
4.2.4.2. Factor de crecimiento nervioso humano recombinante (Recombinant human nerve growth factor o RH-NGF).
El NGF participa en la regulación del crecimiento, la proliferación y la supervivencia de las neuronas y se encuentra de forma natural en las lágrimas [627 - 629]. Se ha notificado que el NGF tiene efectos tróficos en la superficie ocular por medio de la activación de la cinasa A del receptor de la tropomiosina (tropomyosin receptor kinase A, TrkA) y el receptor de neurotrofina p75 [630]. El NGF y el TrkA se expresan en toda la superficie ocular, incluidas las células epiteliales corneales y las neuronas sensoriales [631,632].
La aplicación tópica del NGF puede mejorar la producción y las características funcionales de la película lagrimal mejorando la sensibilidad corneal, con una mejora de los signos de la superficie ocular en perros con ojo seco inducido quirúrgicamente [633]. En humanos, también se han observado sensibilidad corneal, producción de lágrimas y mejora de la agudeza visual tras la administración tópica de colirios del NGF derivado de murino (a una concentración de 200 µg/ml cada 2 h durante 2 días seguido de una gota seis veces al día hasta la curación de la úlcera) [634]. Un estudio en conejos mostró que algunas de esta mejorías podían deberse a la regeneración nerviosa. Este estudio demostró que el NGF tópico aceleró la recuperación del plexo nervioso subbasal tras una cirugía LASIK [635].
Tavilermide (MIM-D3) es un peptidomimético del NGF de moléculas pequeñas que aumenta la lágrima y los líquidos similares a la mucina y que reduce la tinción corneal de ?uoresceína en un modelo de ojo seco en ratas [14,636]. En un ensayo clínico aleatorizado de fase II para estudiar el efecto del MIM-D3 tópico en pacientes con EOS tras la exposición a una cámara de entorno adverso controlado para exacerbar la gravedad del ojo seco, MIM-D3 al 1 % redujo la tinción corneal con ?uoresceína y la tinción conjuntival con verde de lisamina después de 28 días de tratamiento cuando se comparó con placebo [637]. De forma similar, MIM-D3 al 5 % redujo los síntomas de sequedad ocular cuando se comparó con placebo. En pacientes con síntomas más graves, el MIM-D3 en concentraciones del 1 % y del 5 % mostró una reducción significativa de los síntomas cuando se comparó con el placebo [637]. Sin embargo, cabe mencionar que el ensayo clínico de MIM-D3 no cumplió sus criterios de valoración principales previamente especificados con respecto a la tinción corneal con ?uoresceína total y a la peor puntuación de los síntomas [637].
4.2.4.3. Gen/proteína 6 estimulado/a por el factor de necrosis tumoral a (TSG-6).
Las células madre/estromales mesenquimatosas (mesenchymal stem/stromal cells, MSC) suprimen la inflamación en modelos animales de infarto de miocardio, lesión corneal y peritonitis [638 - 640]. Se ha propuesto que las MSC reducen la inflamación por medio de la secreción del gen/la proteína 6 del factor de necrosis tumoral-a (tumor necrosis factor, TNF) (TSG-6), que ha mostrado efectos terapéuticos en modelos experimentales de inflamación corneal [641 - 643]. En un estudio que investigó el efecto de TSG-6 en modelos murinos de ojo seco y síndrome de Sjögren, la aplicación tópica de TSG-6 mejoró la producción lagrimal, redujo la tinción corneal con fluoresceína e incrementó la densidad de las células calciformes cuando se comparó con controles tratados con tampón fosfato salino [644]. Además, TSG-6 redujo los niveles de IL-2, interferón-gamma (IFN-γ), IL-1β e IL-6 en la glándula intraorbital. En la superficie ocular, TSG-6 redujo de forma significativa los niveles de IL-2, IFN-γ, IL-1β e IL-6 cuando se comparó con los controles [644]. En un estudio comparativo para evaluar los efectos de la administración tópica de TSG-6, la ciclosporina y la prednisolona en un modelo murino de ojo seco, TSG-6 demostró un efecto similar al de la ciclosporina y la prednisolona, que produjo una mejora de la producción lagrimal y de la densidad de las células calciformes [642]. Además, el TSG-6 y la ciclosporina tuvieron un efecto similar, reduciendo la tinción corneal con ?uoresceína y reprimiendo los niveles de IFN-γ y TNF-α en la superficie ocular y dentro de la glándula lagrimal [642].
4.2.4.4. Antagonista del receptor de interleucina-1 (IL-1Ra).
El antagonista del receptor de interleucina-1 (IL-1Ra) es una proteína producida principalmente por monocitos activados y macrófagos del tejido, pero también por células epiteliales. Esta proteína inhibe la acción favorecedora de la inflamación de IL-1α e IL-1β bloqueando de forma competitiva su unión al receptor 1 de células productoras de IL-1 (IL- 1R1); cuando IL1-Ra se une a IL-1R1, no se genera ninguna señal, por lo que se trata de un ligando antagónico de IL-1 [645 - 647]. En estados inflamatorios, el gen IL-1Ra suele regularse al alza [646]. El tratamiento con IL-1Ra humano recombinante tópico reduce la inflamación en modelos animales de inflamación de la superficie ocular [647 - 650]. En un modelo murino de ojo seco, el tratamiento tópico con IL-1Ra fue más eficaz que el CMC en la reducción de la tinción con verde de lisamina y en el aumento de la secreción lagrimal. El IL-1Ra tópico redujo la acidificación aberrante de las mucinas de las células calciformes y la queratinización patológica [651]. En un estudio que comparó los efectos del IL-1Ra tópico, la ciclosporina y la metilprednisolona en ratones con ojo seco, la reducción de la tinción de corneal con ?uoresceína fue comparable entre los tres tratamientos. Sin embargo, solo el IL-1Ra y la metilprednisolona redujeron el número de células CD11b+ corneales centrales, el crecimiento linfático corneal y la expresión corneal del IL-1b corneal [544]. En un ensayo clínico aleatorizado de fase II que evaluó los efectos del IL-1Ra tópico (anakinra; Kineret®) y el vehículo tres veces al día durante 12 semanas, el tratamiento con IL-1Ra al 2,5 % redujo de forma significativa la tinción corneal con ?uoresceína en comparación con los valores iniciales, y redujo de forma significativa los síntomas en comparación con el vehículo [652]. Además, el tratamiento con IL- 1Ra indujo el aclaramiento bilateral completo de la tinción corneal con ?uoresceína en el 29 % de los sujetos, en comparación con el 7 % en los sujetos tratados con el vehículo.
4.2.4.5. Tratamiento anti factor de necrosis tumoral-a (TNF- a).
El TNF-a es una citocina con efectos favorecedores de la inflamación y coestimuladora de efectos en múltiples tipos de célula; regula el tráfico de las células inmunitarias y la activación [653,654]. La expresión de TNF-a es elevada en la conjuntiva y en el líquido lagrimal en modelos animales y en pacientes con síndrome de Sjögren y otros tipos de EOS [655 - 657]. Algunos estudios han evaluado el efecto del tratamiento sistémico con agentes bloqueantes de TNF-a como in?iximab y etanercept, en los que se han notificado resultados contradictorios [658 - 661]. Un estudio adicional que comparó in?iximab tópico y una solución salina equilibrada para tratar ratones con ojo seco inducido mostró que los ratones tratados con in?iximab tenían un aumento del volumen lagrimal y menores niveles de citocinas inflamatorias conjuntivales IL-1β, IL-6, IL-17 e IFN-γ, así como una mejora de la densidad de las células calciformes [662]. Los investigadores también han demostrado que ambos bloqueadores de TNF-α, HL036 y etanercept redujeron la inflamación en la glándula lagrimal y la córnea de ratones con ojo seco inducido experimentalmente mediante la supresión de IFN-γ, IL-21 e IL-6 [663].
4.2.4.6. Tratamiento contra la interleucina-17 (IL-17).
Se ha sugerido que las células Th17 están implicadas en la patogénesis de numerosas enfermedades autoinmunes. Un aumento de la expresión de la citocina IL-17 asociada a Th17 ha demostrado fomentar la alteración de la barrera epitelial de la córnea, desempeñando así un papel en la patogénesis de la EOS [664 - 666]. En un modelo in vivo de ojo seco, el tratamiento con anticuerpos anti IL-17 redujeron de forma significativa la tinción corneal con ?uoresceína en ratones [665]. Otro estudio demostró que la neutralización de anticuerpos de IL-17 en ratones con ojo seco experimental mejora la disfunción de la barrera epitelial corneal (reduciendo la permeabilidad de la ?uoresceína) y la expresión de MMP-3 y MMP-9 [666]. Además, el tratamiento con anticuerpo anti IL-17 ha demostrado reducir de forma significativa la linfangiogénesis en ratones con ojo seco, lo que puede ayudar en la reducción de la inmunidad relacionada con EOS [667].
En resumen, las moléculas biológicas siguen teniendo un futuro prometedor en el tratamiento de la EOS. Sin embargo, aunque muchos productos biológicos se han investigado ampliamente en modelos animales, los estudios en humanos siguen siendo escasos y se requieren ensayos en humanos bien diseñados para evaluar en mayor medida su papel terapéutico.
4.2.5. Neuropéptidos
La sustancia P, el péptido relacionado con el gen de la calcitonina (calcitonin gene-related peptide, CGRP), el neuropéptido Y (NPY) y el péptido intestinal vasoactivo (vasoactive intestinal peptide, VIP) se han evaluado en diversos estudios de laboratorio y estudios clínicos en ojos normales y en EOS. Los menores niveles lagrimales de NPY y CGRP en la EOS están relacionados con una disfunción de la función lagrimal [629]. Estos hallazgos sugieren que el NPY y el CGRP podrían convertirse en biomarcadores útiles y que tienen actividad terapéutica en el ojo seco [629,668].
El efecto de VIP se ha testado en células humanas epiteliales inmortalizadas de la glándula de Meibomio [669]. Las células transcriben y traducen los receptores VIP y mACh; VIP activa la vía de la adenilil ciclasa; VIP aumenta el [Ca2+] intracelular en las células de la glándula de Meibomio; y VIP estimula la proliferación de las células de la glándula de Meibomio al combinarse con la forskolina.
La mayoría de los estudios que investigan los neuropéptidos hasta la fecha se han realizado en la queratitis neutropénica de moderada a grave con EOS concomitante, pero no directamente en personas con EOS [670].
4.2.6. Conclusiones
El rango de mecanismos de acción de los medicamentos que se abordan en esta sección, que tienen al menos algo de eficacia demostrable en el tratamiento de pacientes con EOS, arroja algo de luz sobre la compleja fisiopatología de esta enfermedad. Claramente, se requieren investigaciones adicionales.
4.3. Antagonista del antígeno-1 asociado a la función linfocitaria (LFA-1)
Una estrategia para inhibir o reducir la inflamación mediada por linfocitos T en la EOS consiste en impedir que los linfocitos T interactúen con otros elementos celulares inmunológicamente activos. Las integrinas son receptores heterodiméricos de la superficie celular, ubicuos en distintos procesos celulares y fisiológicos, incluida la adhesión, la migración y la activación celulares, pasos cruciales para la actividad y la supervivencia de los linfocitos T [671]. De los 24 heterodímeros de integrina conocidos, la subfamilia β2 de integrinas solo se encuentra en los linfocitos [671]. El antígeno-1 asociado a la función linfocitaria (LFA-1) es un miembro de esta familia de integrinas. El ligando principal para LFA-1 es la molécula 1 de adhesión intercelular (ICAM-1), expresado en diversas células, incluidas las células endoteliales y epiteliales y las células presentadoras de antígenos [672]. La unión entre LFA-1 e ICAM-1 se ha descrito como la “sinapsis inmunológica” y como un paso crítico en la vía hacia la activación de los linfocitos T [673].
4.3.1. Li?tegrast
Li?tegrast es un antagonista de la integrina de molécula pequeña, diseñado para imitar el dominio de unión de ICAM-1 a LFA-1, y se cree que actúa como un antagonista competitivo para bloquear la unión entre LFA-1 e ICAM- 1, que provoca la inhibición de la migración de los linfocitos T a tejidos objetivo, la reducción de la liberación de citocinas y la reducción del nuevo reclutamiento de linfocitos T [674 - 676].
La solución oftalmológica de li?tegrast al 5 % se ha estudiado como un tratamiento tópico para la EOS y hasta la fecha se han publicado cinco ensayos clínicos. En un ensayo clínico de fase II en 230 pacientes [677], se observó una respuesta significativa para los criterios de valoración secundarios previamente especificados de cambio medio desde el inicio hasta el día 84 en la tinción corneal inferior y para una subescala de la función relacionada con la visión, pero no para el criterio de valoración principal de la eficacia de la tinción corneal inferior media. En un estudio clínico de fase III (OPUS-1) en el que participaron 588 sujetos con EOS [678], se encontró una respuesta significativa en la variable de eficacia principal del cambio medio desde el inicio hasta el día 84 en la tinción corneal inferior, así como en otros criterios de valoración secundarios de la eficacia (tinción corneal total y tinción conjuntival con verde de lisamina). Sin embargo, el estudio no cumplió el criterio de valoración coprincipal para los síntomas (la subescala de la función relacionada con la visión del IESO), aunque se notificó una mejora significativa para los sujetos tratados en varios criterios de valoración secundarios de la eficacia para los síntomas. Un segundo estudio clínico de fase III, OPUS-2, notificó resultados de 718 participantes tratados con li?tegrast al 5 % o placebo durante 84 días [679]. En este ensayo, se notificó una mejora significativa en el criterio de valoración principal de la eficacia (cambio desde el inicio hasta el día 84 en la puntuación de sequedad del ojo; escala visual analógica), así como el criterio de valoración secundario de los síntomas de molestias oculares. Sin embargo, no se observó una mejora en los sujetos tratados con li?tegrast en lo que respecta al criterio de valoración coprincipal del cambio medio desde el inicio hasta el día 84 en la tinción corneal inferior, en contraste con los resultados de OPUS-1. El estudio de seguridad a largo plazo SONATA informó acerca de 331 pacientes tratados con li?tegrast dos veces al día o con placebo durante 350 días [680]. Li?tegrast pareció ser seguro y bien tolerado, sin que se notificaran acontecimientos adversos oculares graves y con un perfil de seguridad que era similar al de los estudios publicados previamente.
Tomados en conjunto, estos estudios de nivel 1 demostraron la eficacia de li?tegrast y Xiidra™ (solución oftalmológica de li?tegrast al 5 % Shire, Lexington, MA, EE. UU.), aprobado por la FDA, en un formato unitario de dosis única, en julio de 2016, para el tratamiento tanto de los signos como de los síntomas de EOS.
4.4. Modulación inflamatoria con antibióticos sistémicos y tópicos
4.4.1. Tratamiento con tetraciclina
La tetraciclina y sus análogos (minociclina y doxiciclina) son antibióticos de amplio espectro que inhiben la síntesis proteica inhibiendo la unión de aminoacil ARNt al complejo ARNm-ribosoma. Se ha planteado la hipótesis de que una reducción de las exoenzimas lipolíticas productoras de bacterias [681,682] y la inhibición de la producción de lipasa [683], con la consiguiente disminución de los productos de descomposición de lípidos en la glándula de Meibomio, pueden contribuir a la mejora de los parámetros clínicos en la DGM y la blefaritis anterior asociada a la EOS. Estos agentes también presentan propiedades antiinflamatorias. Disminuyen la actividad de la colagenasa, la fosfolipasa A2 y varios MMP y reducen la producción de mediadores inflamatorios como IL-1 y TNF-a en una amplia variedad de tejidos, incluido el epitelio corneal [541,542,684 - 686]. En modelos murinos experimentales de ojo seco, se determinó que la doxiciclina aplicada por vía tópica conservaba la suavidad epitelial de la córnea y su función de barrera [541,542], además de aliviar la inflamación de la superficie ocular [687]. De forma similar, la minociclina disminuye la producción de diglicéridos y ácidos grasos libres en secreciones de Meibomio [681]. Sin embargo, existe evidencia que sugiere que la doxiciclina, tetraciclina y minociclina no duplican la capacidad de la azitromicina para estimular la diferenciación y la acumulación de lípidos en las células humanas epiteliales de la glándula de Meibomio [688].
La tetraciclina y sus análogos se utilizan con frecuencia para tratar alteraciones que están asociadas con la EOS, como el acné rosácea, la DGM y la blefaritis. La doxiciclina y la minociclina logran una mayor concentración en el tejido y tienen un menor aclaramiento renal, una mayor semivida y un mayor nivel de unión a las proteínas de suero que la tetraciclina y la oxitetraciclina [689], y a menudo se prescriben en casos de enfermedades oculares inflamatorias debido a estas propiedades.
La rosácea, incluidas sus manifestaciones oculares, es un trastorno inflamatorio que se produce principalmente en adultos, con el pico de gravedad en la tercera y cuarta décadas. Existe evidencia que sugiere que existe una fuerte correlación con la DGM [690] y que la infestación por Demodex puede estar asociada a su desarrollo [691-694]. Existe una fuerte evidencia de que el ácido azelaico tópico, la ivermectina, la brimonidina, la doxiciclina e isotretinoina y las tetraciclinas orales (doxiciclina y minociclina) son tratamientos efectivos para la rosácea [695,696]. Sin embargo, existe una fuerte evidencia que demuestra que la isotretinoina destruye las glándulas de Meibomio humanas e induce la queratinización de los conductos de la glándula de Meibomio [477,697] y, por tanto, su uso tópico para el tratamiento de la superficie ocular puede no ser recomendable.
La tetraciclina y sus análogos han demostrado reducir los síntomas subjetivos y la hiperemia asociada a la rosácea ocular en series pequeñas de casos clínicos [698,699], demostrándose la efectividad de una única dosis diaria de doxiciclina de tan solo 40 mg [700,701]. Un ensayo cruzado parcial, prospectivo, aleatorizado, con doble enmascaramiento y controlado con placebo comparó la capacidad de la oxitetraciclina para proporcionar alivio sintomático de la blefaritis en 43 pacientes con y sin rosácea [702]. Solo el 25 % de los pacientes con blefaritis sin rosácea respondieron al antibiótico, mientras que el 50 % respondió cuando ambas enfermedades estaban presentes. Un estudio intervencionista comparativo y prospectivo con 44 sujetos demostró que los niveles lagrimales elevados de MMP-8 en la superficie ocular de personas con rosácea se redujeron de forma significativa tras entre 4 y 8 semanas de tratamiento con doxiciclina oral [703]. Una revisión sugirió que se necesitan estudios adicionales de nivel 1 para seguir evaluando la eficacia de las tetraciclinas en la gestión de la rosácea ocular [696].
La blefaritis crónica suele estar caracterizada por una inflamación de los párpados y existen numerosos subtipos de esta afección [381]. Las tetraciclinas se usan para tratar la blefaritis crónica debido a sus efectos antimicrobianos y antiinflamatorios, y varios estudios han descrito los efectos beneficiosos de la minociclona y la doxiciclina [681,683,704]. Sin embargo, hasta la fecha no existen ECA aleatorizados, controlados y con doble enmascaramiento que demuestren la eficacia de antibióticos sobre la higiene del párpado u otros tratamientos [705,706].
Los efectos de las tetraciclinas en pacientes con DGM se han notificado en un caso práctico [707]. Un estudio aleatorizado, prospectivo, sin enmascaramiento y controlado comparó distintas dosis de doxiciclina en 150 pacientes que tenían DGM crónica y que no respondieron al tratamiento con higiene del párpado ni tópico durante más de 2 meses [708]. Los sujetos fueron aleatorizados en tres grupos: un grupo de dosis alta (doxiciclina, 200 mg, dos veces al día), un grupo de dosis baja (doxiciclina, 20 mg, dos veces al día) y un grupo de control (placebo). Después de un mes, ambos grupos de doxiciclina, el de dosis alta y el de dosis baja, demostraron mejoras estadísticamente significativas en el TDL y los síntomas.
Se realizó un estudio cruzado, aleatorizado, con doble enmascaramiento y controlado con placebo para investigar la eficacia de la doxiciclina a dosis bajas de 20 mg dos veces al día para tratar síntomas clínicos del síndrome de Sjögren [709]. Solo en 5 de los 16 sujetos que recibían doxiciclina los síntomas mejoraron de forma significativa. Otro ensayo clínico prospectivo, aleatorizado y sin enmascaramiento formado por 60 sujetos con DGM de moderada a grave demostró que la minociclina a una dosis diaria de 50 mg mejoraba de forma significativa los signos clínicos de DGM, incluido el TDL, la tinción conjuntiva y corneal, el aspecto de los párpados y la calidad del meibum en comparación con un grupo de control tratado con lubricantes oculares [710]. Se demostró que los niveles de los mediadores inflamatorios de la superficie ocular, incluidos IL-6, IL-1β, IL-17α, TNF-α e IL-12p70, eran significativamente menores tras dos meses de tratamiento [710].
4.4.1.1. Posología y seguridad.
No se ha establecido la pauta posológica óptima de tetraciclinas para el tratamiento de la EOS, habiéndose propuesto varias pautas posológicas. Estas incluyen 50 o 100 mg de doxiciclina una vez al día [711], 200 mg dos veces al día durante 1 mes seguido de 200 mg al día, o una dosis inicial de 50 mg al día durante las primeras 2 semanas, seguida de 100 mg al día durante un periodo de 2,5 meses de modo intermitente [681-683,707]. Otros han propuesto el uso de una dosis baja de doxiciclina (20 mg) a largo plazo [708].
Además de los efectos secundarios conocidos de las tetraciclinas, que incluyen síntomas gastrointestinales y fotosensibilidad, han surgido problemas de seguridad asociados al tratamiento a largo plazo con antibióticos. Para minimizar los riesgos, un reciente estudio sugería que un ciclo de tres meses de 100 mg de minociclina podría ser suficiente para controlar una meibomianitis significativa, ya que el control continuado se mantuvo durante al menos tres meses después del cese del tratamiento [707]. La doxiciclina (40 mg al día) es la única tetraciclina aprobada por la FDA para su uso durante un máximo de 16 semanas en el tratamiento de la rosácea. El tratamiento a largo plazo con doxiciclina a este nivel no ejerce una presión de selección antibiótica sobre la microbiota, lo que previene el desarrollo de la resistencia al antibiótico [712,713]. Estas recomendaciones pueden moderarse debido a informes que indican que, en mujeres, el riesgo de desarrollar cáncer de mama y la morbilidad de cáncer de mama aumenta de forma acumulativa con la duración del uso de antibióticos, incluidas las tetraciclinas [714,715], aunque otro estudio no respalda estos hallazgos [716]. Se necesitan más estudios para determinar si existen riesgos con el uso de tetraciclina a largo plazo.
4.5. Tratamiento con macrólidos
Existen algunos informes sobre el impacto positivo de la azitromicina sistémica en el tratamiento de la DGM, especialmente en personas que sufren intolerancia u otros antibióticos sistémicos [717 - 720]. Un reciente estudio basado en el laboratorio comparó el efecto de la azitromicina, la doxiciclina, la minociclina y la tetraciclina durante 5 días sobre células humanas epiteliales inmortalizadas de la glándula de Meibomio [688]. La azitromicina aumentó de forma significativa la acumulación celular de colesterol, ésteres de colesterol, fosfolípidos y lisosomas, mientras que otros antibióticos no lo hicieron. Los autores concluyeron que los efectos estimulantes de la azitromicina sobre la función de las células humanas epiteliales de la glándula de Meibomio son únicos y no los replican los demás antibióticos evaluados [688].
La azitromicina puede ser una opción valiosa cuando se da la DGM en asociación con rosácea [721 - 723], y se cree que sus propiedades antiinflamatorias pueden ayudar a controlar la flora bacteriana y la inflamación del párpado [706,724-726]. Los efectos secundarios más frecuentes de la azitromicina son diarrea, náuseas y vómitos.
La posología ideal de la azitromicina sistémica sigue siendo objeto de controversia y no existe un acuerdo universal. Estudios previos han demostrado eficacia con una dosis oral diaria de 250 mg o 500 mg para el tratamiento de la rosácea [721,723,727]. Se ha propuesto un tratamiento de pulsos con azitromicina oral para el acné pustular [728,729], y el mismo concepto parece tener éxito para la gestión de la DGM, utilizando 500 mg al día durante 3 días en 3 ciclos con intervalos de 7 días [720]. Se deben llevar a cabo más ECA con doble enmascaramiento para aclarar la eficacia a largo plazo y la posología ideal.
La Tabla 12 resume varios estudios clínicos que investigan el uso tanto de azitromicina oral como tópica para la gestión de la EOS [720,730-735].
Siempre que esté disponible, la azitromicina tópica al 1 % se tolera bien y parece ser eficaz en la gestión de la DGM y la EOS evaporativa, aunque el bajo número de estudios bien diseñados sigue haciendo que este tratamiento sea algo controvertido. En un reciente estudio a gran escala realizado por Hosseini y colegas en el que se evaluó a 907 sujetos con blefaritis, el uso de una combinación de azitromicina-dexametasona tópica durante 14 días dos veces al día fue seguro y bien tolerado [735]. Este colirio combinado logró la resolución clínica completa de un mayor porcentaje de pacientes (8,2 %) que la azitromicina al 1 % (5,2 %), la dexametasona al 0,1 % (5,7 %) o el vehículo (4,7 %).
Es necesario seguir investigando para determinar si existe beneficio derivado de combinar la azitromicina sistémica y tópica para mejorar el tratamiento de la EOS evaporativa, especialmente en la gestión de casos resistentes o graves.
Hasta la fecha, dos estudios han comparado la eficacia de doxiciclina y azitromicina para la gestión de la DGM [717,736]. Una pauta de azitromicina oral de cinco días se comparó con un mes de doxiciclina (200 mg) en un estudio (evidencia de nivel 2) [717]. Aunque ambos tratamientos mejoraron de forma significativa las puntuaciones clínicas y los síntomas, la azitromicina pareció ser más eficaz en la mejora de los signos clínicos. En el segundo estudio de nivel 2, tanto la azitromicina tópica al 1 % durante cuatro semanas como 100 mg de doxiciclina oral dos veces al día durante dos meses redujeron de forma significativa los signos clínicos de DGM. El tratamiento oral con doxiciclina fue ligeramente menos efectivo en la mejora de la sensación de cuerpos extraños y los signos de taponamiento y secreción que la acitromicina tópica [736].
Cabe mencionar que existe un informe reciente que evaluó el papel de los antibióticos orales para la ESO relacionada con la glándula de Meibomio [737]. Esta revisión concluyó que no existe evidencia de nivel 1, y solo escasa evidencia general, que respalde el uso de antibióticos orales en la gestión de ESO relacionada con la glándula de Meibomio.
5.1. Tarsorrafía
La tarsorrafía se refiere a un procedimiento quirúrgico temporal o permanente en el que los párpados se cierran total o parcialmente utilizando suturas. Además del cierre temporal con suturas, también se puede lograr una tarsorrafía temporal con cinta adhesiva, pegamento o parálisis del músculo elevador mediante inyección de toxina botulínica [738]. Cualquier forma de tarsorrafía reduce la exposición de la superficie ocular, reduce la evaporación de la película lagrimal y, en último término, provoca una reducción del desecado y el secado de la superficie ocular. El procedimiento se realiza principalmente en casos de defectos epiteliales persistentes y se reserva para el ojo seco grave resistente a tratamientos médicos y a la oclusión de los conductos lagrimales [499]. Posiblemente debido al hecho de que normalmente se reserva como el último paso cuando todos los demás tratamientos han fracasado, solo el 20 % de los pacientes refirieron no estar contentos con los efectos estéticos [739].
Hasta la fecha, no existen estudios que comparen la eficacia de la tarsorrafía con otras modalidades de tratamiento en la EOS.
5.2. Tratamiento quirúrgico para la conjunctivocalasia
La conjuntivocalasia se caracteriza por la un exceso de conjuntiva bulbar inferior suelta no edematosa que se encuentra entre el globo ocular y el párpado. Se trata de un trastorno ocular relacionado con la edad, que, a menudo, se pasa por alto y afecta de forma negativa a la calidad de vida [740]. La conjuntivocalasia es un hallazgo frecuente en el ojo seco, con una prevalencia notificada del 54 % en personas con EOS [741], y otro informe sugiere que su presencia tiene un valor predictivo positivo del 93 % en el diagnóstico de EOS [742]. La gravedad de la conjunctivocalasia puede clasificarse registrando la puntuación de los pliegues conjuntivales en paralelo al párpado (lid-parallel conjunctival folds, LIPCOF), con una mayor clasificación correlacionada positivamente con síntomas más graves del ojo seco [743]. El mecanismo que vincula la conjunctivocalasia con los síntomas del ojo seco podrían relacionarse con su impacto en la AML más baja [744,745]. La epifora es también un síntoma de conjunctivocalasia, especialmente cuando tiene localización media, y se puede aliviar corrigiendo la conjuntivocalasia [746,747].
En casos graves de conjunctivocalasia que no responden a lubricantes oculares, ciclosporina tópica u oclusión del conducto lagrimal, se puede considerar la resección del exceso de tejido conjuntival [748]. También se han notificado varios enfoques para reducir los pliegues excesivos conjuntivales, incluida la electrocoagulación o la cauterización térmica [749,750], fijación simple a la esclerótica [751] y conjuntivoplastia con láser de argón [752]. En todos los estudios (evidencia de nivel 3), se ha notificado cierto nivel de mejora de los síntomas en más del 75 % de los pacientes.
5.3. Tratamiento del blefarospasmo esencial con neurotoxina botulínica
El blefarospasmo esencial (BE) es una distonía craneal focal que afecta al párpado y a los músculos de la frente. Se ha notificado que entre el 40 % y el 60 % de los pacientes con BE presentan síntomas de ojo seco y una reducción de las puntuaciones Schirmer [753 - 756]. Con carácter adicional, los niveles de citocina proinflamatoria del líquido lagrimal también aumentaron en pacientes con ojo seco con BE en comparación con los que solo presentaban EOS [757].
La inyección de toxina botulínica A para la gestión del BE causa la denervación farmacológica temporal del músculo orbicular del párpado. Varios estudios de casos y controles (evidencia de nivel 2) informan de una mejora de los síntomas del ojo seco y un aumento de la AML, del TDLT y del tiempo de aclaramiento lagrimal después de la inyección de toxina botulínica A [757 - 759]. Sin embargo, estos efectos duran tan solo 3 meses [760]. Por el contrario, la producción de lágrimas puede verse alterada por inyecciones de toxina botulínica A que se administran demasiado cerca de la glándula lagrimal [753,761,762].
5.4. Correcciones de los párpados
5.4.1. Dermatocalasia
La dermatocalasia es un término utilizado para describir la presencia de piel del párpado suelta e innecesaria, y es un signo frecuente de envejecimiento. Basándose en evidencias de nivel 2 y 3, el 46-51 % de los pacientes con dermatocalasia presentan quejas por ojo seco y el 55-86 % de los pacientes logran una mejora subjetiva de los síntomas después de la blefaroplastia del párpado superior [763,764]. Sin embargo, no se ha demostrado que los parámetros objetivos cambien de forma significativa tras la blefaroplastia [764], y las mejoras notificadas pueden ser puramente psicológicas.
5.4.2. Blefaroptosis (ptosis)
La enfermedad del ojo seco puede ser un factor de riesgo para la blefaroptosis, ya que causa un aumento de la fricción entre el párpado superior y la superficie ocular, que puede contribuir a la desinserción o el debilitamiento del músculo elevador levator aponeurosis. Un estudio prospectivo de casos y controles (evidencia de nivel 2) mostró que una baja puntuación Schirmer se da con más frecuencia en pacientes con ptosis aponeurogénica adquirida que en controles [765].
A pesar de la corrección quirúrgica de la ptosis, la calidad de la lágrima puede seguir deteriorándose. En una serie de casos intervencionistas, las puntuaciones Schirmer y el TDL revelaron una reducción de la cantidad y la calidad de la lágrima después de la cirugía [766]. El volumen lagrimal también puede disminuir después de la cirugía para la ptosis [767,768].
5.4.3. Blefaroplastia del párpado inferior
La laxitud del párpado inferior y el ectropión son ocurrencias frecuentes a medida que avanza la edad, y se tratan muy frecuentemente con blefaroplastia transcutánea del párpado inferior. Sin embargo, incluso después de una cirugía aparentemente exitosa, los pacientes a menudo refieren sequedad, epifora y quemosis durante el posoperatorio [769 - 771].
La enfermedad del ojo seco es una de las complicaciones más frecuentes después de cualquier tipo de cirugía de párpado [102], con la excepción de la tarsorrafía [772]. Las causas frecuentes del ojo seco posoperatorio incluyen quemosis, aumento de la exposición de la superficie ocular, lagoftalmos, posicionamiento incorrecto del párpado inferior y reducción del reflejo de parpadeo como consecuencia de la anestesia quirúrgica o de un edema [102,483]. Estas causas se describen con más detalle en los informes de fisiopatología y de ojo seco iatrogénico de TFOS DEWS II.
5.5. Cirugía conjuntival e injertos de la membrana amniótica
Las personas con trastornos conjuntivales como pterigión, pinguécula, síndrome de Stevens-Johnson y penfigoide de la membrana mucosa a menudo desarrollan EOS. El pterigión avanzado causa la distribución desigual y la evaporación focal de las lágrimas sobre la superficie ocular, lo que agrava los síntomas de ojo seco. Los pacientes de ojo seco con inflamación grave de la superficie ocular y cicatrización podrían beneficiarse del tratamiento quirúrgico con reconstrucción conjuntival, así como de la eliminación de los tejidos inflamados y los fibroblastos activados [773 - 775]. Sin embargo, en pacientes con penfigoide de la membrana mucosa, cualquier cirugía de la superficie ocular y del párpado se debe llevar a cabo una vez que la enfermedad esté debidamente controlada mediante inmunosupresión sistémica para evitar la exacerbación de la enfermedad. El autoinjerto de la conjuntiva o el limbo reduce la recurrencia de pterigión en comparación con la escisión de la esclera desnuda y el trasplante de la membrana amniótica, y se ha convertido en un tratamiento de referencia [776]. La aplicación concurrente de mitomicina C reduce aún más el riesgo de recurrencia, aunque está asociada a complicaciones potencialmente graves, como debilitamiento escleral, ulceración y epitelialización retardada de la conjuntiva [777].
La EOS grave puede provocar defectos epiteliales persistentes, ulceración corneal y cicatrización corneal. Los injertos de la membrana amniótica podrían considerarse para tratar defectos epiteliales persistentes en casos de penfingoide cicatricial ocular, síndrome de Stevens-Johnson y otras ESO [499,775,778-782]. Estas membranas contienen una amplia variedad de neuropéptidos y neurotransmisores, incluidas la acetilcolina y la catecolamina [783 - 787].
Una forma particular de trasplante de la membrana amniótica es PROKERA® y PROKERA® SLIM (Bio-TissueDoral, FL, EE. UU.), más fina que la anterior. Estos dispositivos contienen membrana humana amniótica procesada con una forma de crioconservación que conserva la actividad biológica del tejido. La membrana queda contenida dentro del anillo termoplástico, lo que permite introducir el dispositivo de un modo similar a las lentes esclerales y sujeta el tejido firmemente en su sitio. Los injertos normalmente se disuelven en aproximadamente una semana y, a continuación, puede retirarse el anillo conformador [788]. Hasta la fecha, solo se han publicado unos pocos estudios de casos sobre su uso [782,789,790]. Un estudio mostró una mejora sostenida de los síntomas durante cuatro meses en sujetos con ojo seco que llevaron PROKERA® SLIM durante una media de aproximadamente cinco días [782]. Los autores también notificaron una reducción de la tinción corneal y conjuntival, así como una mejora de la agudeza visual.
5.6. Dacriorreservorios mecánicos
En la EOS grave, las personas con puntuaciones Schirmer de ≤1 mm pueden requerir la aplicación de gotas lubricantes cada pocos minutos, lo que altera seriamente las acitividades diarias y provoca una marcada reducción de la calidad de vida. En estos casos, se han utilizado dispositivos mecánicos que suministran gotas lubricantes de un reservorio a través de un catéter para lubricar de forma continua la superficie ocular. Un estudio en conejos demostró que una bomba de microinfusión, originalmente desarrollada para el tratamiento de insulina en diabéticos, pudo administrar una dosis de lágrimas artificiales similar a la encontrada en los ojos normales [791]. Además, los ojos tratados con corticosteroides mediante esta bomba se recuperaron más rápido que los tratados con corticosteroides tópicos.
En un ensayo prospectivo no aleatorizado de 21 sujetos con una puntuación Schirmer de ≤1 mm, se implantó un reservorio de 60 ml bajo los tejidos subcutáneos de la pared abdominal anterior y se conectó a un catéter de silicona que ascendía de forma subcutánea a lo largo del pecho, el cuello y la sien hasta el fondo de saco conjuntival superior [792,793]. Todos los sujetos refirieron una mejoría de los síntomas y mostraron un TDL prolongado con una reducción de la tinción corneal y de la hiperemia conjuntival. Las infecciones del reservorio o del catéter, aunque no se describieron en este estudio, pueden darse y pueden requerir la explantación del dispositivo.
Aunque raros, queda claro que los dacriorreservoirios mecánicos pueden ser una opción valiosa en casos de déficit lagrimal acuoso grave en los que todas las demás medidas menos invasivas han fracasado a la hora de proporcionar un alivio subjetivo suficiente.
5.7. Trasplante de la glándula salival mayor
El objetivo del trasplante de la glándula salival es proporcionar algo de tejido exocrino viable a un ojo gravemente seco. Las posibles indicaciones pueden incluir alacrimia primaria (congénita) o déficit acuoso grave secundario a la conjuntivitis cicatrizal (debido al penfigoide de la membrana mucosa, síndrome de Stevens-Johnson, quemaduras químicas), daño quirúrgico o radioablación del tejido lagrimal (como la que se encuentra en la enfermedad neoplásica de la cabeza). Disponer de una glándula salival viable, además de ser una fuente de lubricación constante, también proporciona factores epiteliotróficos que también están presentes y son funcionalmente relevantes en las lágrimas [794].
Las tres principales glándulas salivales, la parótida, la submandibular y la glándula sublingual, se han utilizado para lubricar la superficie ocular, aunque el enfoque de trasplantar una glándula sublingual al espacio subconjuntival no ha tenido éxito debido a la isquemia del tejido injertado [795]. Para la glándula parótida y la glándula submandibular, los enfoques quirúrgicos son totalmente distintos y ambos requieren el conocimiento de un cirujano oral experimentado.
5.7.1. Transposición del conducto parotídeo
En este procedimiento, el conducto secretor de la glándula parotídea se mueve de su posición premolar original en la boca al fondo de saco conjuntival inferior [796]. Dado que se mantiene la inervación de la glándula, el resultado es una epífora refleja gustativa de una secreción puramente serosa. Las evidencias de su éxito se limitan a informes de casos retrospectivos o series sin datos de seguimiento cuantitativos. Las complicaciones incluyen blefaritis y queratitis por secreción excesiva, para las que se determinó que medidas como los anticolinérgicos sistémicos o la denervación parasimpática de la glándula eran impracticables o ineficaces, y parece que esta técnica se ha abandonado [797].
5.7.2. Trasplante de la glándula submandibular microvascular
Una glándula submandibular libre parcial o total con un pedículo vascular y el conducto secretor se transfiere a la sien. Se crea una anastomosis microvascular con los vasos faciales y el conducto se sutura en el fondo de saco conjuntival [798,799]. Pese a que el procedimiento requiere varias horas de anestesia general, ofrece algunas ventajas importantes respecto a otros procedimientos que utilizan tejido de la glándula salival, entre ellas (i) un riego sanguíneo establecido para garantizar la viabilidad de las glándulas, (ii) una secreción capaz de sustituir el componente de la mucosa o el suero de la película lagrimal, (iii) la ausencia de salivación refleja debido a la denervación simpática intraoperatoria del injerto y (iv) una secreción inicial mantenida debido a las células ganglionares intraglandulares parasimpáticas supervivientes [800].
En ratas y conejos, las glándulas submandibulares trasplantadas siguieron siendo viables y activas durante al menos seis meses después del trasplante [801,802]. Varios grupos han publicado resultados clínicos en sujetos con déficit acuoso grave [798,799,803-807]. A pesar del potencial de complicaciones microvasculares, se notificó que un 66-100 % siguió siendo viable durante al menos cinco años, de acuerdo con la exploración oftalmológica clínica o la escintigrafía [808]. Los injertos alogénicos requieren inmunosupresión a largo plazo [809]. La mayoría de informes proceden de cirujanos maxilofaciales o de oído, nariz y garganta, y a menudo solo cuentan con datos limitados sobre hallazgos de la superficie ocular. La evaluación más sistemática hasta la fecha es una serie prospectiva de casos controlados con un seguimiento durante más de 40 meses [805,807]. Los resultados mostraron una mejora sustancial de la puntuación Schirmer, del TDL, del uso de sustitutos lagrimales y de los síntomas en comparación con los controles (los ojos contralaterales sin un injerto de la glándula mandibular viable) desde los tres meses hasta el final del seguimiento. Ni la agudeza visual (probablemente debido a cicatrices corneales preexistentes y otras comorbilidades) ni la inflamación conjuntival o la metaplasia escamosa mejoraron [807].
Al comparar el trasplante total de glándulas submandibulares frente al parcial, Qin y sus colaboradores refirieron epífora grave en 19 de los 22 pacientes con un injerto de glándula submandibular total frente a 6 de los 20 ojos con trasplante parcial [799]. La secreción de la glándula se estimuló con calor o actividad física y se pudo bloquear mediante anticolinérgicos [799,805,810,811]. La hipersecreción también se puede controlar quirúrgicamente reduciendo el tamaño de la glándula o mediante la ligadura parcial del conducto [805,812].
Aunque la lubricación resultante contiene muchas proteínas y otros componentes abundantes en las lágrimas, es muy hipoosmolar en comparación con las lágrimas y esta hipoosmolaridad puede inducir el edema epitelial microquístico en casos de trasplantes con sobresecreción [190,794,807,813]. Como consecuencia, el 100 % de los cinco trasplantes corneales realizados después del trasplante de la glándula submandibular fracasaron debido a rechazo, infección o edema epitelial asociado a epífora, con subsiguiente perforación corneal [807].
En resumen, la glándula submandibular es la única glándula salival mayor que se está utilizando actualmente para proporcionar lubricación al ojo por medio de trasplante. Solo está indicado en pacientes con un déficit absoluto de lágrima acuosa con malestar grave persistente y cuando todos los demás medios han fallado. Estos pacientes se benefician de un alivio sustancial de los síntomas graves y de algunos signos de ojos seco, pero el procedimiento no permite una rehabilitación visual exitosa.
5.8. Autotrasplante de la glándula salival menor
La mucosa oral y nasal se pueden usar para reconstruir los fondos de saco y para suministrar mucina a la superficie ocular, pero este procedimiento no es capaz de proporcionar suficiente lubricación para mantener un injerto corneal sano [814,815]. La mucosa labial (que recubre los labios) se ha utilizado como un injerto completo para los fondos de saco conjuntivales en ojos secos graves, con un éxito excelente en términos de viabilidad del injerto [795,797]. La secreción de las glándulas salivales menores es predominantemente mucinosa, y las glándulas salivales bucales muestran la tasa de flujo más elevada [816]. El trasplante provocó un aumento de la puntuación en la prueba de Schirmer y el TDL, y también proporcionó un alivio sintomático [817].
Marinho notificó resultados de 14 pacientes y Sant’ Anna de 19 pacientes con EOS grave secundaria al síndrome de Stevens-Johnson que se sometieron a un trasplante de la glándula salival labial [817,818]. Hasta 14 meses después de la operación, el volumen lagrimal mejoró en más del 70 % de los pacientes. La transparencia corneal y la agudeza visual mejoraron en el 72 % y los síntomas se redujeron en el 54 % y el 100 %, respectivamente. Las complicaciones potenciales incluyen hipoestesia labial temporal o necrosis del injerto, sensación de ojos “acuosos” o voluminosidad y laxitud de los párpados que provoca entropión, así como la morbilidad del sitio donante.
6. Modificaciones en la dieta volver arriba
Existen cada vez más evidencias de que la dieta y la suplementación nutricional desempeñan un papel en la EOS. Las contribuciones al estado de hidratación general y otras intervenciones, como la lactoferina y la suplementación antioxidante, también eran dignas de consideración.
6.1. Estado de hidratación general
Se ha propuesto que el estado de hidratación de todo el cuerpo desempeña un papel potencial en el control de la EOS. Los niveles de osmolaridad lagrimal en adultos sanos aumentan como consecuencia de una modesta deshidratación de todo el cuerpo (pérdida del 2-3 % de la masa corporal) durante el ejercicio [819,820], un efecto que es modificable con la ingesta de líquidos [819]. Los datos observacionales sugieren que el estado de hidratación de todo el cuerpo también puede influir en la expresión clínica de la EOS. En un estudio transversal de 111 participantes de al menos 60 años de edad, las personas clasificadas como que padecían EOS resultaron tener una osmolaridad plasmática superior, lo que indica una hidratación subóptima, en comparación con las personas sin EOS [821]. Aún se debe estudiar más en profundidad si una mejora de la hidratación de todo el cuerpo con intervención fluídica confiere un beneficio terapéutico en personas con EOS. Concretamente, sigue existiendo la necesidad de ensayos de intervención controlados para evaluar la eficacia y la seguridad de la optimización del estado de hidratación como un tratamiento no farmacológico de la EOS.
6.2. Ácidos grasos esenciales
Los ácidos grasos esenciales (AGE) se denominan “esenciales” porque son necesarios para que tengan lugar procesos metabólicos sanos [822]. Los humanos no son capaces de formar AGE in vivo y deben ingerirlos a través de fuentes alimenticias. Dos AGE clave son los ácidos grasos de 18 átomos de carbono omega-3 (ω-3) y omega-6 (ω-6). Los AGE ω-3 existen en subtipos tanto de cadena corta (ácido alfalinolénico, AAL) como de cadena larga (ácido eicosapentaenoico, AEP, y ácido docosahexaenoico, ADH). Ambos subtipos se pueden consumir con los alimentos, de modo que las formas de cadena larga también se pueden producir a partir de formas de cadena corta en el organismo, por medio de la desaturación/elongación de AGE de cadena corta. Fuentes alimentarias frecuentes de AAL incluyen semillas de lino, nueces, semillas de chía y aceite de soja. Los ácidos grasos poliinsaturados (AGPI) ω-3 de cadena larga, AEP y ADH están presentes en elevadas concentraciones en el pescado graso (como el atún, el salmón, la trucha, las sardinas y la caballa), así como, en menor medida, en algún marisco (como los langostinos, las ostras y los mejillones). Los AGE ω-6 suelen derivarse de aceites vegetales, como aceite de cártamo y aceite de maíz, en forma de ácido linolénico (AL) que, una vez ingerido, se desatura y elonga para formar ácido gamma-linolénico (AGL) y ácido araquidónico (AA) [823].
En el organismo, los AGE ω-3 y ω-6 compiten por las enzimas que regulan su metabolismo para producir eicosanoides que modulan la inflamación sistémica. Los eicosanoides derivados de ω- 6, la vía dependiente de AA, incluida la prostaglandina-E2 (PGE2), el tromboxano-A2 y el leucotrieno-B4, favorecen la inflamación. Mientras que la mayoría de eicosanoides ω-6 fomentan la inflamación [824], el metabolismo de AGL puede provocar la producción de prostaglandina-E1 (PGE1) y tromboxano-A1, que son mediadores antiinflamatorios [824]. Los efectos potenciales de los AGE ω-6 sobre la inflamación son, por tanto, complejos. Los AGE ω-3 de cadena larga producen un sesgo del metabolismo de la prostaglandina hacia la producción de eicosanoides proinflamatorios, incluidas las resolvinas y las protectinas, que son esenciales para limitar y resolver la inflamación [825]. Como tal, la proporción relativa de AGE ω-3 a ω-6 consumidos influye en el estado inflamatorio general del organismo [824].
En los tiempos modernos, el equilibrio en la ingesta de ácidos grasos esenciales (AGE) de ω-3 a ω-6 con la dieta ha cambiado, alterando así el equilibrio de las citocinas inflamatorias [826]. En las dietas occidentales actuales, la proporción de ingesta ω-6:ω-3 es normalmente 15:1, mientras que una proporción ideal se considera, por lo general, 4:1 [827]. Como resultado, ha existido interés científico en entender si los crecientes niveles sistémicos de AGE ω-3 por medio de la intervención nutricional para reducir la proporción de ω-6:ω-3 puede provocar efectos antinflamatorios sistémicos que son beneficiosos para afecciones con inflamación superpuesta, incluida la EOS.
6.2.1. Estudios de investigación fundamental
Se reconoce que los AGE omega-3 tienen una amplia gama de efectos antiinflamatorios sistémicos, incluida la inhibición de la producción de varias citocinas proinflamatorias clave (como IL-1, IL-2 y TNF- α) [828 - 830] y la prevención de la proliferación de linfocitos T [831,832], procesos que se han involucrado en la patogénesis de la EOS.
Varios estudios de laboratorio han demostrado que el enriquecimiento con ácidos grasos puede provocar cambios en las glándulas lagrimales y alterar la respuesta de la superficie ocular en modelos de EOS inducida farmacológicamente [833 - 838]. Dos estudios recientes en laboratorio han evaluado el impacto de los AGE en la función de las células humanas epiteliales de la glándula de Meibomio [833,834]. El estudio realizado por Liu et al. mostró que los AGE influyeron en la calidad y la cantidad de lípidos intracelulares, lo que dio como resultado un aumento de 2,4 a 3,7 veces en el contenido celular de triglicéridos después del tratamiento con ω-3 y ω-6, respectivamente. En ratas, la suplementación alimenticia con ω-3 (AEP + ADH) durante tres meses se asoció a su incorporación a los tejidos de la glándula lagrimal [835]. Un enriquecimiento nutricional durante dos meses combinado con AGPI ω-3 (AEP + ADH) y ω-6 (GLA) redujo la queratitis corneal, minimizó la sobreexpresión del complejo mayor de histocompatibilidad (major histocompatibility complex, MHC) II e inhibió la regulación al alza de la prostaglandina (PG) E1 y PGE2 en la glándula lagrimal, después de 28 días de intervención con escopolamina [836]. En modelos murinos de EOS, las fórmulas tópicas de AGE ω-3 han demostrado reducir los niveles de tinción corneal con ?uoresceína [837,838] y reducir tanto los números de células CD11b (+) como la expresión conjuntival de IL-1a y TNF-α [837]. Los AGE ω-3 tópicos, con y sin la adición de AH al 0,1 %, también han demostrado mejorar la irregularidad corneal y reducir la alteración de la barrera epitelial [838].
La evidencia experimental respalda el potencial terapéutico de una clase de inmunomoduladores endógenos derivados de los lípidos, las resolvinas, derivadas del AEP (resolvina E1) y ADH (resolvina D1), como tratamiento antiinflamatorio de la EOS [14,839,840]. Las resolvinas E1 y D1 fomentan la resolución de la inflamación en células calciformes conjuntivas cultivadas mediante la reducción de los cisteinil leucotrienos [839,840]. En modelos murinos de EOS, se ha notificado que la resolvina E1 aumentó la producción lagrimal, mejoró la regularidad corneal y redujo la infiltración de macrófagos [841], además de reducir la alteración de la barrera epitelial corneal y atenuar la pérdida de células calciformes de la conjuntiva [842]. La aplicación tópica de un profármaco de resolvina E1, RX-10045 (0,1 %), que se hidroliza rápidamente a su forma activa en matrices biológicas, puede reducir la neblina estromal corneal después de la lesión corneal en conejos [843]. En un reciente estudio clínico, RX-10045 no cumplió un criterio de valoración principal relacionado con la tinción corneal [329]. Aunque las investigaciones relacionadas con la resolvina D1 son menos frecuentes, es importante destacar que estos agentes tienen un papel en la salud corneal. Por ejemplo, un derivado del ADH, el NPD1, es importante en la regeneración nerviosa y la sensibilidad corneal [844,845].
6.2.2. Datos observacionales en humanos
El Estudio de Salud de la Mujer, que incluyó a más de 32 000 mujeres, describió una asociación entre una baja ingesta de AGE ω-3 en la dieta y la EOS en mujeres [846]. Este estudio informó de una reducción del 30 % en el riesgo de EOS con cada gramo adicional de AGE ω-3 consumido al día. Una mayor proporción de ω-6:ω-3s en la dieta también estuvo asociada a un elevado riesgo de EOS (para ≥15:1 frente a <4:1, razón de probabilidades: 2,51; IC del 95 %: 1,13, 5,58, p = 0,01). Además, recientemente se ha demostrado que la proporción de lípidos lagrimales ω-6:ω-3 es elevada en personas con EOS y que esto ocurre en proporción al grado de la disfunción de la película lagrimal y la tinción corneal [847]. El nivel de ingesta de AGE ω-3 en la dieta también está asociado a diferencias en el patrón lipídico polar de secreciones de la glándula de Meibomio en mujeres con síndrome de Sjögren [848].
6.2.3. Ensayos clínicos de suplementos de AGE
Se han realizado ensayos clínicos para evaluar el beneficio potencial de la suplementación oral con AGE ω-3 y ω-6, tanto solos como en combinación, para el tratamiento de la EOS. La mayoría de estos ensayos intervencionistas se han realizado en centros únicos y con números de participantes relativamente pequeños (tamaño de la muestra <70). Los ensayos clínicos han tenido grados diversos de enmascaramiento, tanto para los participantes como para los evaluadores de los resultados, y pocos de ellos presentaron doble enmascaramiento.
Todos los ensayos clínicos que evalúan solo los AGE ω-3 (Tabla 13) [849 - 859] se han realizado durante tres meses como máximo, con la excepción de un estudio piloto que investigó la eficacia de los AGE ω-3 de cadena corta (AAL) para el tratamiento de la DGM y la blefaritis durante 12 meses [849]. Las intervenciones con AGE ω-3 han variado tanto en términos de subtipo (formulaciones de cadena corta y/o de cadena larga) como de dosis. Hasta la fecha, solo un estudio ha evaluado la eficacia relativa de distintas formas de AGE ω-3 de cadena larga para el tratamiento de la EOS, comparando el aceite de krill, principalmente en forma de fosfolípido, con el aceite de pescado en forma de triglicérido [858]. Este ensayo clínico aleatorizado y controlado con placebo sugería que los AGE ω-3 en forma de fosfolípidos (aceite de krill) podrían conferir un beneficio terapéutico adicional en la EOS, siendo necesarias más investigaciones clínicas para evaluar este potencial. Se han examinado distintas medidas de los resultados, que implicaron principalmente la cuantificación de los cambios en la sintomatología de los pacientes y medidas clínicas objetivas relativas a la estabilidad y/o la producción de lágrimas. Más recientemente, también se han demostrado los efectos beneficiosos de los suplementos de AGE ω-3 orales en la EOS, con la especificación de la osmolaridad lagrimal como una medida principal de los resultados [858,859]. Un reciente estudio piloto ha demostrado adicionalmente los efectos neuroprotectores de la zona corneal central con una suplementación trimestral de una dosis moderada de ω-3 (1000 mg/día de AEP + 500 mg/día de ADH) en EOS [860]. En un intento por resumir la mejor evidencia disponible, un metanálisis concluyó que la suplementación con AGE ω-3 mejora el TDL y las puntuaciones Schirmer en personas con EOS, sin alterar de forma significativa las puntuaciones del IESO [861].
Aunque muchos pacientes se automedican con suplementos de AGE ω-3 bajo la premisa de sus difundidos beneficios para la salud, el uso de estos suplementos requiere ciertas precauciones. Existen diversas contraindicaciones sistémicas importantes, incluida la lesión hepática, la fibrilación auricular y trastornos hemorrágicos; en estos casos, se debe buscar asistencia médica antes de comenzar la suplementación. Pueden existir riesgos potenciales para la salud con la ingesta de altas dosis de AGE ω-3 (>2000 mg/día combinados de AEP + ADH), en términos de un riesgo destacado de hemorragia [862], y las personas con trastornos hematológicos deben buscar atención médica antes de consumir suplementos de AGE ω-3 [863]. También se ha sugerido la posibilidad de que los hombres con elevadas concentraciones séricas de AGPI ω-3 de cadena larga presenten un mayor riesgo de cáncer de próstata [864], pero esto sigue siendo controvertido [865,866]. Tanto la FDA como el Consejo Nacional de Sanidad e Investigación Médica (National Health and Medical Research Council, NHMRC) de Australia recomendaron un límite superior diario para el consumo de ácidos grasos omega-3 de 3 g (3000 mg); esto incluye los ácidos grasos omega-3 derivados tanto de alimentos como de suplementos. Es importante advertir que esta dosificación está relacionada con la cantidad de contenido en ácidos grasos omega-3, en lugar del tamaño de la cápsula del suplemento per se. Por ejemplo, muchas cápsulas de aceite de pescado de 1 g (1000 mg) contienen 180 mg de AEP + 120 mg ADH; por tanto, solo en torno al 30 % del contenido de la cápsula de suplemento de aceite de pescado serán ácidos grasos omega-3 de cadena larga.
Los ensayos clínicos intervencionistas que han evaluado formulaciones de AGE ω-6 para el tratamiento de la EOS se han realizado en centros únicos, han variado en su duración de tres semanas a seis meses, y presentaban variaciones considerables en las dosis diarias (Tabla 14) [867-871]. La mayoría de estudios se dirigían a poblaciones de estudio con síndrome de Sjögren, con resultados variables notificados en relación con los cambios en los síntomas del ojo seco, los marcadores de inflamación ocular y otros signos clínicos (como la tinción de la superficie ocular, el TDL y la puntuación Schirmer).
Los ensayos clínicos que investigaron la suplementación con una combinación de AGE ω-3 y ω-6 han variado en duración de tres a seis meses, e incluyen tanto estudios de un solo centro como estudios multicéntricos (Tabla 15) [872 - 877]. Un metanálisis de 2014 que consideró la eficacia general de la suplementación con AGPI para el tratamiento de la EOS concluyó que, en comparación con el placebo, estas intervenciones provocaron una reducción significativa en la puntuación de los síntomas (cuantificada utilizando el IESO) y en la tasa de células positivas para HLA-DR [878].
También se publicó en 2014 un protocolo de revisión sistemática de Cochrane sobre este tema y está actualmente en curso [879].
6.2.4. Resumen de ácidos grasos esenciales
El papel de la suplementación con AGE ω-3 y/o ω-6 para tratar la EOS aún no se ha entendido completamente. Aunque se ha realizado un número considerable de ensayos clínicos (Tablas 13 - 15), la mayoría han sido de duración breve y muestran hallazgos contradictorios. Existen pocos ensayos clínicos controlados y aleatorizados de gran calidad para servir de fundamento a la práctica clínica. Como consecuencia, actualmente no existe consenso acerca del protocolo óptimo, en particular en lo que se refiere a la dosis, la composición o la duración del tratamiento. Además, la mayoría de estudios clínicos no han medido el cumplimiento con las intervenciones del estudio mediante análisis de ácidos grasos en el suero sanguíneo. Esto se considera esencial para evaluar con precisión los efectos que tiene sobre la salud la suplementación, en particular debido a que las fuentes frecuentes de AGE ω-3 (como los suplementos de aceite de pescado) tienen el potencial de provocar efectos secundarios gastrointestinales que incluyen regusto a pescado y diarrea, que pueden afectar de forma negativa al cumplimiento [880]. Actualmente se está realizando un ensayo controlado con placebo, multicéntrico y aleatorizado a gran escala (estudio DREAM) para evaluar la eficacia y la seguridad de los AGPI ω-3 (con dosis a 2000 mg AEP + 1000 mg ADH/día) durante 24 meses, financiado por el Instituto Nacional de Salud [National Institute of Health] (https://clinicaltrials.gov/ ct2/show/NCT02128763). Se prevé que este estudio informe de las recomendaciones de tratamiento para el uso de AGPI ω-3 de dosis alta para tratar la EOS.
6.3. Lactoferrina
La lactoferrina es una glicoproteína lagrimal multifuncional con propiedades antibacterianas, antiinflamatorias y antiangiogénicas. Los niveles lagrimales de lactoferrina se consideran un indicador de la función secretora lagrimal [881]. Se han notificado niveles reducidos de lactoferrina lagrimal en diversas poblaciones clínicas con EOS [881 - 886], que proporcionan una justificación científica para evaluar el posible beneficio de la suplementación alimenticia con lactoferrina como una intervención para el ojo seco. La lactoferrina oral preserva la función de la glándula lagrimal en ratones viejos reduciendo el daño oxidativo y suprimiendo la inflamación glandular [887]. En un estudio piloto de siete individuos con síndrome de Sjögren, la suplementación oral con lactoferrina (270 mg/día) durante un mes mejoró los síntomas de ojo seco, el TDL, las puntuaciones de la tinción vital de la superficie ocular, las puntuaciones de sensibilidad corneal y de la citología de impresión, con anulación de la mejora tras el cese del tratamiento [888]. Un reciente ensayo clínico prospectivo controlado aleatorizado de un único centro informó de la mejora de los síntomas de ojo seco, TDL y puntuaciones de Schirmer con respecto a placebo con lactoferrina oral diaria posoperatoria durante dos meses (350 mg/día) tras cirugía de cataratas con incisión pequeña [889]. Se necesitan investigaciones adicionales para aclarar la función del suplemento con lactoferrina para tratar la EOS.
6.4. Otras consideraciones nutricionales
El estrés oxidativo, que genera especies de oxígeno reactivo perjudiciales para las células, puede participar en la lesión celular que conduce a la ESO, incluido el ojo seco [890]. En un ensayo cruzado, aleatorizado y controlado con placebo que implicaba un suplemento antioxidante administrado por vía oral (con beta-caroteno, vitaminas E, C, B, B6, D, zinc y cobre) en personas con EOS marginal, se demostraron mejoras relativas en la estabilidad lagrimal, la densidad de las células calciformes y la metaplasia escamosa en el criterio de valoración del estudio a un mes [891]. Otro pequeño ensayo clínico controlado y aleatorizado de un suplemento oral combinado de antioxidante y mineral (zinc) informó de mejoras en el TDL y en las puntuaciones Schirmer, así como una reducción de los síntomas oculares en personas con EOS, en comparación con placebo durante 12 semanas [892]. Un ensayo preliminar abierto no controlado en el que participaron 13 personas con EOS demostraron que la suplementación antioxidante oral diaria, con extracto de baya de Aristotelia chilensis (30 mg), provocaron una mejora relativa de los síntomas de ojo seco y puntuaciones Schirmer, en comparación con el inicio, durante dos meses [893].
El ácido alfa lipoico, un compuesto disulfuro de origen natural, también tiene capacidad antioxidante [894]. En un modelo animal de ojo seco posmenopáusico, se observó que la suplementación alimenticia con ácido alfa lipoico durante 16 semanas aumentaba la actividad de la peroxidasa lagrimal y mejoraba la producción lagrimal [895]. Aún se debe investigar si el ácido alfa lipoico tiene aplicación clínica para la EOS en humanos.
Kawashima y colegas demostraron que la restricción calórica preserva la función de la glándula lagrimal atenuando el daño oxidativo en la glándula lagrimal, lo que sugiere que los cambios en la dieta y una reducción en la ingesta calorífica pueden ser beneficiosos en la gestión del ojo seco [896]. El trabajo más reciente del mismo grupo en un modelo de ojo seco en ratas y en un ensayo clínico en humanos ha demostrado el valor a corto plazo de los cambios en la dieta para los signos y síntomas de ojo seco [897]. Un reciente estudio cruzado de una sola visita también respaldó la idea de que el aumento de la grasa corporal puede provocar un aumento de los síntomas de ojo seco [898]. La ingesta de alcohol induce ojo seco temporal en individuos sanos [899], lo que sugiere que su consumo puede agravar los síntomas y signos de ojo seco.
Recientemente, se describió que el uso de gafas con extractos de cuatro plantas medicinales conocidas por sus propiedades antioxidantes y antiinflamatorias, tres veces al día durante ocho semanas mejoraba tanto signos objetivos como subjetivos del ojo seco, en comparación con una intervención con placebo, en personas con EOS leve [900]. Los hallazgos de estas investigaciones preliminares requieren confirmación mediante ensayos clínicos multicéntricos lo bastante grandes y debidamente controlados.
7. Consideraciones del ambiente local volver arriba
Se ha implicado a varios factores “ambientales” en la EOS, incluidas las medicaciones sistémicas y tópicas, las afecciones desecantes, el uso de dispositivos digitales y el uso de lentes de contacto [102]. Es importante considerar estos factores de riesgo, ya que esta información puede proporcionar información adicional sobre la respuesta individual de un paciente en respuesta al tratamiento prescrito.
La modificación de cualquier problema ambiental relevante es potencialmente útil para las opciones de gestión temprana, ya que cualquier cambio inicial en la superficie ocular que culmine en EOS puede prevenirse o potencialmente invertirse eliminando los factores de riesgo ambiental asociados.
7.1. Medicamentos tópicos crónicos
Diversos estudios han demostrado que los conservantes pueden estar asociados a reacciones alérgicas, tóxicas o inflamatorias, en particular en pacientes que utilizan medicamentos tópicos a largo plazo. Los conservantes como el CAB irritan la superficie ocular [98] y tanto los síntomas (como quemazón, sequedad y sensación de cuerpo extraño) como los signos son significativamente más frecuentes en pacientes que utilizan medicamentos con conservantes para el glaucoma [901,902]. Varios estudios han sugerido que los medicamentos para el glaucoma pueden contribuir a la ESO y al desarrollo de ojo seco [903,904], y la gravedad de la ESO se ha correlacionado con el número de medicamentos con conservantes en uso y con la gravedad de la enfermedad del glaucoma [905 - 907].
Dos grandes ensayos clínicos multicéntricos realizados en Europa demostraron que cambiar a medicamentos sin conservantes (preservative-free, PF) para el glaucoma provocó que los pacientes experimentaran significativamente menos signos y síntomas de ESO [901,902]. Los medicamentos PF disponibles para el tratamiento del glaucoma incluyen los análogos de la prostaglandina (APG), ta?uprost PF, betabloqueantes, maleato de timolol PF y una combinación de dosis fija en forma de dorzolamida/timolol PF. El timolol sin conservantes ha estado disponible durante varios años en EE. UU. y Europa, y tiene menos efectos negativos sobre los síntomas y signos de ESO y sobre las pruebas de la función lagrimal [908]. Ciancaglini et al. realizaron una microscopía confocal de la conjuntiva y realizaron una citología de impresión para demostrar que el uso de levobunolol sin conservante se asoció a menores cambios en la conjuntiva [909]. Renieri et al. informaron de un ensayo clínico cruzado de 2298 sujetos que cambiaron de diversos tratamientos conservados con CAB a dorzolamida/timolol sin conservante, y demostraron una mejor tolerabilidad local en un 80 % de los pacientes [910]. Uusitalo et al. cambiaron a 158 pacientes de latanoprost conservado con CAB a ta?uprost sin conservante durante 3 meses [911]. Detectaron reducciones significativas de los síntomas, tinción corneal con ?uoresceína, hiperemia conjuntival y células conjuntivas anómalas (según HLA-DR y MUC5AC), así como mejoras en el TDL y en las puntuaciones Schirmer.
Además de la disponibilidad de fármacos PF, se han desarrollado conservantes adicionales para minimizar el efecto tóxico del CAB [912]. El polyquaternium 1 (Polyquad®) es un conservante de amonio cuaternario que se considera menos tóxico para la superficie ocular, basándose en estudios que examinan la toxicidad para las células epiteliales corneales y conjuntivales. Labbe et al. [913] demostró que el Polyquad inducía considerablemente menos toxicidad que CAB in vivo y que produjo resultados similares que los del control en la prueba de Schirmer, lámpara de hendidura, tinción corneal con ?uoresceína e histología [913]. SofZia™ es un sistema de conservación oxidativa utilizado en un preparado de travoprost, y diversos estudios han demostrado una mejora de los síntomas y los signos de ESO después de cambiar de medicamentos conservados con CAB a colirios conservados con sofZia [914 - 916].
Puede encontrar información adicional sobre las interacciones de los conservantes con la superficie ocular en el informe del ojo seco iatrogénico de TFOS DEWS II [102].
7.2. Medicación sistémica
Muchos fármacos utilizados para tratar enfermedades crónicas pueden contribuir a la EOS. Se ha notificado una mayor incidencia de ojo seco en personas que utilizan antihistamínicos, betabloqueantes, antidepresivos, diuréticos, ansiolíticos, antipsicóticos, fármacos contra el Parkinson, isotretinoína, tratamiento con estrógenos y quimioterapia sistémica [102,917]. Las estrategias para reducir o eliminar los efectos secundarios sistémicos inducidos por el fármaco incluyen el cambio en la vía de administración de oral a tópica, la interrupción de los fármacos, los ajustes de las dosis, el cambio a otro medicamento o una gestión más agresiva del ojo seco inducido [102].
7.3. Reducción de la frecuencia de parpadeo
El parpadeo es esencial para mantener la homeostasis de la película lagrimal preocular en la superficie ocular [918]. Una reducción de la frecuencia de parpadeo o un parpadeo incompleto afectan a la dinámica de las lágrimas, prolongando el periodo durante el que la superficie ocular queda expuesta a la pérdida de agua antes del siguiente parpadeo, contribuyendo así al desarrollo de la EOS [919,920]. Un factor principal que afecta a la frecuencia de parpadeo es el uso de terminales de pantallas de vídeo (TPV) y otros dispositivos digitales, leer y otras diversas tareas visuales y funciones cognitivas. Con el aumento exponencial del uso de ordenadores en el lugar de trabajo, se ha notificado un aumento proporcional del número de informes de epidemiología y patología de esta afección [921,922]. El porcentaje de oficinistas japoneses que utilizan TPV y que han sido diagnosticados con ojo seco aumentó hasta el 10 % en hombres y el 20 % en mujeres [923]. Los principales mecanismos por los que los TPV pueden inducir signos o síntomas de ojo seco incluyen un aumento de la tasa de evaporación de la película lagrimal, el desarrollo de DGM a una edad más temprana, una reducción del volumen lagrimal [924,925], una reducción de la concentración de MUC5AC en las lágrimas [926] y un aumento del estrés oxidativo [927].
El principal tratamiento para personas que muestran estos cambios en la superficie ocular es la prevención de la desecación, y el uso frecuente de lubricantes oculares sin conservante suele ser el tratamiento inicial elegido. Sin embargo, los dispositivos o el software informático que estimulan el parpadeo con más frecuencia presentan un mecanismo potencial para la minimización del efecto de los TPV. Miura et al. demostró que un novedoso dispositivo de diodos luminosos (LED) aumentó la frecuencia de parpadeo para los grupos de ojo seco y de control [928]. Cardona et al. presentaron una estrategia en la que el parpadeo reflejo fue provocado por una repentina distorsión del texto de la pantalla para aumentar la frecuencia de parpadeo espontánea [929]. Se recomienda hacer pausas frecuentes y la formación en la concienciación del parpadeo para los usuarios de TPV que requieren periodos prolongados de demanda visual. Los factores ergonómicos, como bajar la pantalla, permiten al usuario del dispositivo digital mirar hacia abajo, exponiendo así menos área de la superficie ocular al aire del ambiente, reduciendo la pérdida de película lagrimal y reduciendo los síntomas del ojo seco [930].
7.4. Afecciones desecantes y contaminantes medioambientales
La superficie ocular es la superficie mucosa del organismo más expuesta desde el punto de vista medioambiental, que se enfrenta a factores como la exposición al viento, baja humedad relativa, temperaturas extremas, radiación UV, agentes irritantes, agentes contaminantes y humo del tabaco. La exposición a condiciones ambientales adversas, como la baja humedad y/o el aumento/la reducción de la temperatura del aire y/o el movimiento del aire, conduce a un aumento de la inestabilidad y la evaporación lagrimales [931]. Estas afecciones fomentan el desarrollo de síntomas de ojo seco en personas normales y también peores síntomas y signos en aquellos con EOS [932 - 935]. La sequedad crónica de la superficie ocular provoca una cascada descendente de acontecimientos que favorecen la inflamación, la apoptosis epitelial, la pérdida de células calciformes y cambios en las glándulas de Meibomio. Los estudios han demostrado la eficacia de determinados tratamientos en respuesta a afecciones medioambientales desfavorables. Estos incluyen el uso de lágrimas artificiales [43,936,937], medicamentos que suprimen las respuestas inflamatorias [584,842,938-940], fármacos que inducen la secreción mucosa [941] y fármacos que reducen la apoptosis [942].
Mientras que evitar la exposición a condiciones adversas puede aumentar la inestabilidad y la evaporación lagrimales representa la táctica inicial, crear condiciones que imiten un entorno adecuado para la superficie ocular también es un enfoque válido. Estos incluyen el uso de humidificadores [317,943] y la retención de líquido lagrimal utilizando gafas de cámara de humedad, lentes de contacto y tapones lagrimales [307,944-946].
El aumento de la contaminación del aire está asociado al ojo seco [947] y factores como el humo de los cigarrillos pueden provocar una película lagrimal disfuncional [948 - 950]. El humo de tabaco contiene numerosas sustancias oxidantes y tóxicas, que exponen a quienes las inhalan a una enorme carga de radicales libres. Matsumoto et al. confirmaron el efecto nocivo que tiene una exposición crónica acumulada al humo del tabaco sobre la película lagrimal, lo que provoca un aumento de los niveles de hexanoil-lisina lagrimal, un marcador del estrés oxidativo para la peroxidación lipídica [951]. Rummenie et al. observaron hallazgos similares tras la exposición pasiva al humo del tabaco [952]. Los efectos adversos del humo de tabaco para el fumador pasivo sobre la película lagrimal queda evidenciado por un aumento de las citocinas inflamatorias lagrimales, los productos de la peroxidación lipídica y una reducción de la defensa mucosa, que provoca inestabilidad y daño en el epitelio de la superficie ocular [948,951]. La inhibición del estrés oxidativo podría actuar terapéuticamente para “romper el ciclo” de citotoxicidad, inflamación y muerte celular.
7.5. Uso de lentes de contacto
Existen numerosos factores que contribuyen a las molestias relacionadas con las lentes de contacto y a la EOS, incluidos problemas relacionados con las lentes de contacto (entre ellos el material de las lentes, su diseño, ajuste, periodo de recambio y sistema de cuidado) [953] y con la superficie ocular [954]. Un informe previo de TFOS abordó las estrategias para reducir las molestias de las lentes de contacto [500]. Estas estrategias incluían ajustar la frecuencia de sustitución de las lentes de contacto, eliminar o cambiar el sistema de cuidado, alterar el diseño de las lentes, añadir suplementación lagrimal y realizar la oclusión de los conductos lagrimales [500].
En conclusión, existen numerosos factores medioambientales que los médicos deben considerar al tratar a personas con EOS, y las estrategias de gestión adecuada serán a menudo un complemento útil para cualquier tratamiento prescrito.
8. Medicamentos complementarios volver arriba
Debido a diversos problemas económicos, culturales y regulatorios, muchos países presentan una escasez de fármacos aprobados para la EOS. Se han utilizado diversos medicamentos complementarios como estrategias alternativas para la gestión de la EOS.
8.1. Productos naturales y a base de plantas
Los productos naturales y a base de plantas, tanto tópicos como orales, se han utilizado con frecuencia en muchos países durante siglos. Sin embargo, relativamente pocos ECA han comparado la medicina a base de hierbas con tratamientos convencionales debido a las dificultades inherentes a la forma en que se prescriben las hierbas. Muchos de estos tratamientos están basados en la teoría tradicional del “yin” y “yang” de la medicina china y, por lo tanto, requieren que los facultativos traten a los pacientes de ojo seco con una combinación de distintas hierbas chinas [955]. Mientras que esto potencialmente permite “personalizar” los tratamientos a las personas, también impide que se estandaricen y, por tanto, es más difícil estudiar la eficacia de estos productos utilizando el enfoque ECA de referencia. Algunos estudios de nivel 1 basados en el laboratorio han sugerido que las medicinas chinas pueden desempeñar un papel en la regulación del equilibrio inmunológico de células Th1 a Th2 en suero, así como la expresión de acuaporina-1 y acuaporina-5 [956,957]. Sin embargo, el mecanismo de acción de estos productos sigue siendo poco conocido y hace falta más trabajo para demostrar la efectividad de las hierbas en el tratamiento de la EOS. También se han notificado varios efectos secundarios, incluidos náuseas, dolor abdominal, diarrea, síntomas gastrointestinales menores, disfunción hepática y disfunción renal leves, que se deben considerar al adoptar estas opciones de tratamiento [958].
En un estudio de nivel 1 con 80 participantes, se demostró que Chi-Ju-Di-Huang-Wan, una hierba que se receta con frecuencia, mejora de forma significativa el TDL de sujetos con ojo seco tras 4 semanas [959]. Varios estudios de nivel 2 y 3 han investigado la combinación óptima de hierbas necesarias para tratar el síndrome de Sjögren [444,955,958]. Un ECA de nivel 1 con doble enmascaramiento con 240 sujetos mostró que un ciclo de seis semanas de gránulos de ShengJinRun ZaoYangXue para el síndrome de Sjögren primerio mejoró los síntomas de la boca seca, el ojo seco y bajos flujos lagrimales, aunque no se produjo una mejora de los signos clínicos [960].
8.2. Miel
Durante siglos, algunas culturas han considerado que los productos apícolas, como la jalea real y la miel, tienen propiedades medicinales. En diversos estudios clínicos y de laboratorio de nivel 2 y 3 se ha notificado que tienen propiedades antibacterianas, antiinflamatorias, antioxidantes y de curación de heridas [961 - 964]. La administración oral de jalea real puede restablecer la capacidad de secreción lagrimal en un modelo de ojo seco con supresión del parpadeo [965]. La aplicación tópica de colirio de miel de Manuka puede reducir el número de bacterias aisladas del margen del párpado y la conjuntiva en pacientes con EOS [966]. Una crema de microemulsión para ojos de miel de Manuka Cyclopower con actividad antimicrobiana confirmada en pruebas preclínicas [967] ha demostrado ser segura en un ensayo de tolerabilidad en humanos de fase I [968]. Aunque es prometedor, se necesitan más ensayos clínicos para evaluar el papel terapéutico de esta formulación y otros productos apícolas.
8.3. Leche
La leche materna es un medicamento tradicional relativamente frecuente para el tratamiento de distintas afecciones oculares en algunos países [969,970]. La instilación tópica de leche materna, especialmente el calostro, ha demostrado ser eficaz en el tratamiento de la epífora infantil en un estudio de nivel 3 [971] y en la prevención de la conjuntivitis neonatal en un estudio de nivel 1 [972] mediante la inhibición de distintos patógenos oculares comunes [973 - 975].
En un pequeño estudio de nivel 3, 10 de los 11 pacientes notificaron una mejora en los síntomas de sequedad y demostraron cierta mejoría en los signos clínicos después de haber sido tratados con suero de calostro bovino [976]. Un estudio en conejos mostró que la fucosil lactosa, un oligosacárido natural en el calostro humano, puede mejorar de forma significativa el volumen lagrimal y el TDL en un modelo de ojo seco inducido por atropina [977]. La leche materna también contiene abundante lactoferrina (véase la sección 6.3), lo que la convierte en un buen candidato a remedio natural para el tratamiento del ojo seco.
8.4. Acupuntura
La acupuntura es una intervención tradicional en los países de Asia oriental para tratar diversas afecciones. Sin embargo, no existen métodos comunes a toda la acupuntura, lo que hace que estudiarla de forma sistemática sea todo un desafío. Se ha sugerido que la estimulación del sistema nervioso periférico con un efecto central concomitante podría ser el mecanismo de alivio del dolor, que posteriormente podría afectar a la percepción del dolor, alterar la inflamación o las sensaciones periféricas, o “reconvertir” los nervios periféricos ante la sensación de dolor [978].
Se ha notificado que la acupuntura mejora el TDL, las puntuaciones Schirmer y la tinción corneal en un grado superior al de las lágrimas artificiales en estudios de nivel 1 [979,980], un estudio de nivel 2 [981] y un informe de metanálisis [982]. Otro estudio de nivel 1 demostró que el volumen lagrimal, evaluado mediante los cambios en los parámetros del menisco lagrimal, mejoró de forma significativa después de un tratamiento de cuatro semanas con acupuntura [983]. Algunos estudios han evaluado los efectos de procedimientos relacionados en la gestión de la EOS. Dos estudios clínicos bien controlados mostraron que tanto la acupuntura láser como la electroterapia SSP sin aguja (silver spike point) fueron igual de eficaces que la acupuntura tradicional en el alivio de los síntomas y el aumento de la secreción lagrimal en sujetos con ojo seco [984,985].
Una carencia de muchos de estos estudios es que el control utilizado para evaluar la eficacia relativa de la acupuntura fue la lágrima artificial, en lugar de utilizar acupuntura simulada. En un ECA, 42 participantes con EOS se inscribieron para aceptar la acupuntura “real” o simulada [986]. Tras cuatro semanas, los sujetos de ambos grupos notificaron una mejora significativa de los síntomas, sin diferencias significativas entre los dos grupos. Esto condujo a que los autores concluyeran que la acupuntura simulada y la real eran igual de efectivos para el tratamiento de los síntomas de EOS.
9. Gestión de los aspectos psicológicos de la EOS volver arriba
La EOS ha demostrado estar asociada a factores psicológicos, como depresión y estrés [987 - 989]. Se ha demostrado que la prevalencia de los trastornos del sueño y del ánimo es significativamente superior en personas con EOS [990]. Reconociendo la importancia de la psicología positiva, la Organización Mundial de la Salud considera que la “felicidad” es un componente importante del estado de salud general [991]. Se considera que una psicología positiva, incluido un estado de felicidad, mejora la función humana y fomenta que las personas tengan vidas más exitosas [992]. Estos hallazgos han conducido al interés de la investigación en la influencia de la “felicidad” en la expresión clínica de EOS.
Un reciente estudio japonés informó de que las personas con niveles elevados de felicidad subjetiva también presentaban menos síntomas autonotificados de ojo seco; esta asociación no fue evidente para los indicadores objetivos de EOS [993]. Además, los participantes con menores puntuaciones de felicidad informaron de síntomas significativos de EOS, pero no mostraron marcadores clínicos objetivos de EOS. Los autores concluyeron que existe una necesidad de nuevos estudios que investiguen si las intervenciones psicológicas positivas pueden ser beneficiosas en la gestión de la EOS.
Los hallazgos de un estudio transversal basado en encuestas, en el que se describe una asociación entre la EOS y los bajos niveles de actividad física y un comportamiento sedentario [994], también han planteado la pregunta relativa a si la actividad física puede influir en la calidad de la película lagrimal. Aunque se ha propuesto que el ejercicio es un complemento potencialmente útil para la gestión de la EOS [994], actualmente se carece de evidencia clínica que respalde este enfoque. Para respaldar ampliamente esta hipótesis, se determinó que el ejercicio de entrenamiento durante ocho semanas en un modelo murino de diabetes tipo II aumentaba la secreción lagrimal [995].
10. Algoritmo gradual de gestión volver arriba
La gestión de la EOS es complicada debido a su etiología multifactorial. Desarrollar la simple doctrina de que “el diagnóstico precede al tratamiento” significa que los médicos deben hacer lo posible por identificar el grado en el que la ESO (probablemente relacionada con la DGM), el OSDA y/u otras afecciones de la superficie ocular contribuyen a la presentación de los pacientes. Este aspecto de determinar los principales factores causantes tras la EOS es crítico para una gestión apropiada.
La Fig. 1 presenta, esquemáticamente, un enfoque para la gestión de la EOS. Antes de seleccionar la gestión apropiada que se debe llevar a cabo, se debe preguntar y realizar las pruebas diagnósticas con el fin de determinar que el paciente realmente tiene EOS y si muestra de forma general más signos de ESO o de OSDA. Pueden encontrarse más detalles sobre las pruebas apropiadas para confirmar un diagnóstico de EOS y los principales factores etiológicos en el informe sobre metodología diagnóstica de TFOS DEWS II [10]. Después de confirmar un diagnóstico de EOS, la gravedad de la enfermedad, junto con la determinación del subtipo etiológico, permitirán desarrollar un plan de tratamiento adecuado.
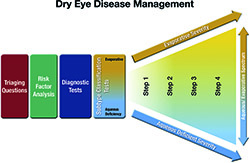
Fig. 1 Diagrammatic representation of the process associated with the management of DED.
La mayoría de los pacientes con EOS muestran alguna relación entre la gravedad de los síntomas y los signos. Sin embargo, es bien sabido que una parte de los pacientes muestran signos y síntomas contradictorios [996 - 998]. En situaciones en las que existen síntomas crónicos, pero signos limitados que son resistentes al tratamiento, se debe considerar el dolor neuropático en lugar de la EOS. Esto se describe más en detalle en el informe sobre dolor y sensación de TFOS DEWS II [539]. Por contra, en pacientes con pocos síntomas, pero signos claros de EOS, la reducción de la sensibilidad corneal, que sugiere queratopatía neurotrófica, es una posibilidad [999 - 1001], y el tratamiento con receta puede ser especialmente importante para evitar el daño continuo.
El último objetivo de la gestión de la EOS consiste en restablecer la homeostasis de la superficie ocular, rompiendo el círculo vicioso de la enfermedad y ofreciendo opciones a largo plazo para evitar un regreso a este círculo vicioso y una reaparición de los síntomas. Mientras que existen tratamientos que pueden estar específicamente indicados para un aspecto concreto de una afección de la superficie ocular de un paciente individual, podrían recomendarse de forma apropiada diversos tratamientos para múltiples aspectos de una presentación de EOS.
La gestión de la EOS normalmente implica tratar secuelas crónicas que requieren gestión continua, en lugar de un tratamiento a corto plazo, para eliminar los problemas de ojo seco. El algoritmo de gestión que se presenta en este informe no representa un enfoque gradual rígido, sino que se debe ver como una herramienta organizativa que se debe usar al iniciar el tratamiento de la EOS para seleccionar las intervenciones que probablemente sean más beneficiosas. El algoritmo tiene en cuenta tanto la etiología como la gravedad de la enfermedad, progresando desde tratamientos más generalizados para la enfermedad de etiología mixta a tratamientos más avanzados y específicos dirigidos a aspectos concretos de la fisiopatología de la enfermedad. La relación riesgo/bene?cio y las consideraciones de los costes también contribuirán necesariamente a las elecciones realizadas entre las opciones de tratamiento [5 - 9,17].
Los algoritmos de gestión a menudo se construyen para recomendar una secuencia de tratamientos de acuerdo con el estadio de la enfermedad, pero esto no es posible para la EOS, ya que se trata de una afección compleja que varía de un paciente a otro tanto en gravedad como en carácter. Sin embargo, con la intención de ayudar a los facultativos de oftalmología a crear un enfoque de tratamiento lógico y basado en evidencias, se propone el siguiente algoritmo de gestión (Tabla 16). Para pacientes que no responden a un determinado nivel de gestión o que muestran una EOS más grave, se recomienda el siguiente nivel de gestión y, en algunos casos, el tratamiento previo puede continuar, además de cualquier nuevo tratamiento (Fig. 1 y Tabla 16). En general, los enfoques de gestión comienzan con tratamientos convencionales de bajo riesgo y normalmente disponibles, como lubricantes de venta sin receta para las fases tempranas de la enfermedad, y progresan hacia tratamientos más avanzados para formas más graves de EOS [1002].
Sin embargo, se reconoce que la notable heterogeneidad que existe en la población de pacientes de EOS impide un enfoque excesivamente formulista y se prevería que estas recomendaciones se adaptasen, por medio de los oftalmólogos, para adecuarse mejor a cada paciente.
Es importante, después de iniciar cualquiera de estas estrategias, que se produzca un cuidadoso seguimiento para garantizar que los pacientes ponen en práctica con éxito las opciones de gestión recomendadas y establecer mejoras de los síntomas y/o signos. El intervalo de tiempo durante el que se debe aplicar el tratamiento antes de que se pueda concluir que no se va a producir ninguna mejora está relacionado tanto con la respuesta del individuo como con el tratamiento que se está considerando. Una revisión de la literatura sugiere que la mayoría de los estudios tienen una duración de 1-3 meses (con la excepción de la ciclosporina, ya que la acción terapéutica puede tardar varios meses en producirse y los periodos del estudio suelen ser superiores a los 3 meses) [595 - 597] y, por tanto, los cambios más allá de este periodo de tiempo para la mayoría de tratamientos no parecerían probables.
Si hay evidencia clínica de complicaciones más graves asociadas a la presencia de ojo seco, como afectación avanzada del párpado (chalazión, triquiasis), neovascularización corneal o signos clínicos de infección microbiana, el médico debe considerar enfoques adicionales. Algunos ejemplos podrían incluir potencialmente esteroides intralesionales o la escisión de un chalazión, depilación de las pestañas o crioterapia para triquiasis, y fármacos antiangiogénicos para neovascularización. Queda fuera del ámbito de este informe la descripción exhaustiva de estas estrategias de gestión.
En resumen, la gestión de la EOS sigue siendo todo un arte que no se presta fácilmente a un algoritmo rígido y basado en evidencias que se adapte a todos los pacientes con síntomas y signos de ojo seco. Todos los oftalmólogos que tratan la EOS deben aplicar su criterio médico para juzgar la importancia de cada uno de los variados procesos patogénicos (déficit acuoso, DGM, inflamación, etc.) que pueden manifestarse como quejas subjetivas similares y signos similares de alteración de la homeostasis de la superficie ocular. La investigación continuada seguirá mejorando la comprensión de la eficacia relativa del tratamiento de distintas intervenciones para causas individuales de la EOS y determinará las acciones terapéuticas sinergísticas.
11. Direcciones futuras de la investigación volver arriba
Desde la publicación del informe de TFOS DEWS original [1], las opciones disponibles para tratar la EOS han aumentado drásticamente. La última década ha sido testigo de nuevos desarrollos de lubricantes tópicos (en particular colirios con lípidos), opciones de suero autólogo y diseños de tapones lagrimales. Han surgido numerosos desarrollos nuevos para ayudar en la higiene del párpado, así como nuevos tratamientos disponibles para la infestación por Demodex, dispositivos para gestionar la DGM y lentes de contacto esclerales rígidas permeables a gases. Además de las distintas opciones para gestionar los procesos inflamatorios asociados a la EOS que han salido al mercado, el impacto de las modificaciones en la dieta (en particular el valor de suplementos de AGE) se conoce mejor y se está debatiendo el valor potencial de diversos medicamentos complementarios.
Sin embargo, la revisión de la literatura hasta la fecha indica que se necesitan muchas más investigaciones para confirmar el valor de muchas de estas opciones de tratamiento. El dogma clínico relativo a la prescripción de muchas opciones de gestión suele tener un pobre respaldo de los estudios de nivel 1. Se han realizado muchos estudios en pequeños números de muestras de pacientes que, a menudo, están mal categorizadas. Existen muchas oportunidades para que los médicos e investigadores realicen estudios que se añadiesen al cuerpo de conocimiento existente, lo que ayudaría a guiar la gestión futura de los pacientes con EOS.
Mientras que prescribir lubricantes sin receta sigue siendo el elemento principal del tratamiento precoz para la EOS, muy pocos ECA han comparado la superioridad entre productos. Con la amplia variedad de composiciones que hay actualmente disponibles, se requieren más trabajos en esta área. Sería especialmente valioso realizar estudios que compararan la eficacia de los productos con y sin lípidos en la EOS evaporativa y con déficit acuoso. También merecen consideración los estudios para determinar el impacto de varias formulaciones sobre la osmolaridad de la película lagrimal y la duración del tratamiento requerida para que se produzcan cambios, en especial para lubricantes que se espera que influyan en la estabilidad de la película lagrimal. También hay ausencia en la literatura de comparaciones de compatibilidad con la superficie ocular entre las formulaciones de dosis unitaria sin conservante y las formulaciones que contienen nuevos conservantes “más suaves” que se administran en frascos multidosis con válvulas unidireccionales. Finalmente, sería valioso contar con estudios que se centren en el potencial de los antioxidantes tópicos para influir en los signos y síntomas de la EOS.
El enfoque para la conservación de la lágrima utilizado con más frecuencia es el uso de tapones lagrimales. Sin embargo, dada la aceptación de la importancia de la inflamación en el ciclo continuo de la EOS, se ha publicado poco sobre el potencial de esta opción de gestión para influir en la inflamación de la superficie ocular, y esto requiere cierta consideración. Otros métodos para mejorar la conservación lagrimal incluyen gafas con cámara de humedad y humidificadores locales, cuya popularidad está aumentando. Sin embargo, muy pocos estudios han investigado su eficacia de un modo controlado.
La estimulación lagrimal por medio de fármacos o dispositivos también suscita un interés creciente. Los secretagogos tópicos están disponibles en algunos mercados, y la FDA ha aprobado recientemente un nuevo dispositivo neuroestimulador lagrimal intranasal para la producción aguda de lágrimas. Ambos enfoques parecen tener un valor potencial, pero se necesitan más estudios de nivel 1 para confirmar su eficacia.
Está generalmente aceptado el valor de la higiene del párpado para una gestión exitosa de la EOS. Sin embargo, una detenida revisión de la literatura muestra que existen muy pocos estudios de nivel 1. ¿Qué efecto provoca el uso de estropajos comerciales para la limpieza del párpado sobre la microbiota de los párpados? ¿Qué bacterias se ven afectadas? ¿Con qué frecuencia y durante cuánto tiempo se deben realizar los frotados del párpado? ¿Cómo debe ser el régimen de mantenimiento? ¿Qué formato de limpiador para el párpado afecta de forma positiva a la osmolaridad lagrimal, los marcadores inflamatorios de la película lagrimal o la estabilidad de la película lagrimal? ¿Existe una combinación óptima de limpiadores para el párpado que se pueda usar con otras opciones de gestión simples, como la suplementación de AGE orales y los colirios tópicos? ¿Tiene la aplicación de antibióticos tópicos en los párpados en combinación con limpiadores para párpados un impacto positivo en la EOS? ¿Cuál es el impacto del aceite del árbol del té según los limpiadores para el párpado en la inflamación de la superficie ocular? Este área íntegra es rica en oportunidades para estudios futuros.
Desde que se publicó el informe de TFOS MGD [2], el interés en la gestión de la DGM ha crecido sobremanera. Está generalmente aceptado el valor de las compresas calientes junto con la evacuación física de las glándulas bloqueadas. Sin embargo, la efectividad de los distintos dispositivos de calentamiento parece variar, y queda pendiente esclarecer cuáles son las características clave. ¿Se debe combinar el calor con el masaje? ¿Cómo se debe combinar la gestión en la consulta y en el domicilio para lograr un efecto óptimo? Además, se necesita más trabajo en este área para determinar si el tratamiento con antibióticos orales es valioso incluso en casos de menor gravedad, en qué medida se requiere un régimen de mantenimiento y si las modificaciones en la dieta pueden ayudar en la gestión de la DGM. Cabría esperar entender más plenamente el papel que pueden desempeñar los lubricantes basados en lípidos en combinación con los tratamientos físicos, el proceso fisiopatológico subyacente que explica por qué la LPI puede resultar útil, si la palpación intraductal es perjudicial a largo plazo y con qué frecuencia se puede realizar, y cuánto dura la escalada de desbridamiento en los orificios de la glándula de Meibomio antes de que se deba repetir. Estos y muchos otros estudios mejorarían nuestra capacidad para gestionar la DGM en pacientes con EOS.
A pesar de reconocer el papel de la inflamación en la EOS, sigue habiendo escasez de estudios de nivel 1 que investiguen el papel a largo plazo de los nuevos esteroides tópicos y de los AINE en la gestión de la EOS. También se requiere trabajo adicional para investigar el potencial de los esteroides o los AINE en forma de dosis de pulsos para romper el ciclo de la EOS y aclarar las pautas posológicas apropiadas.
La creciente disponibilidad de una gran variedad de productos biológicos tópicos y la comercialización de un nuevo antagonista de LFA-1 abre muchas oportunidades nuevas para investigar el papel de estos nuevos agentes en la mejora de una gran variedad de síntomas y signos en pacientes con EOS.
El papel de los antibióticos sistémicos (tetraciclinas y macrólidos) en la gestión de la EOS se conoce relativamente poco, y las pautas posológicas óptimas siguen bajo un intenso debate, con numerosas sugerencias publicadas. Se necesitan más trabajos para entender su papel a la hora de predecir qué pacientes es más probable que se beneficien de su uso.
Existe una creciente evidencia de que las modificaciones en la dieta, el aumento notable de la ingesta de agua y la suplementación de AGE puedan afectar a la EOS. Sin embargo, la selección de los AGE apropiados para ingerir, sus proporciones relativas, la pauta posológica diaria, el impacto en los marcadores inflamatorios de la película lagrimal, la densidad de las células calciformes, la estabilidad lagrimal y la osmolaridad precisan de más estudio.
Finalmente, cada vez se está utilizando una cantidad mayor de una serie de productos naturales y remedios a base de plantas para gestionar a los pacientes con EOS, entre los cuales la miel y distintas hierbas parecen ser prometedoras. Estos agentes tópicos y sistémicos, junto con la acupuntura, requieren más estudios de nivel 1 para lograr una aceptación generalizada como opciones de gestión potencial para la EOS.
Como reflejo de toda la evidencia disponible hasta la fecha, se derivó un algoritmo gradual de gestión (Tabla 16) que presenta un enfoque escalonado para implementar las distintas opciones de gestión y terapéuticas conforme a la gravedad de la enfermedad. Pese a que este ejercicio indicaba que era importante diferenciar entre el déficit acuoso y la enfermedad del ojo seco evaporativa a la hora de seleccionar la estrategia de gestión más apropiada, esto también puso de manifiesto las dificultades, basándose en la limitada evidencia actualmente disponible, para predecir los beneficios relativos de las opciones de gestión específicas de cara a la gestión de los dos subtipos de EOS. A medida que mejoran las pruebas diagnósticas de los signos y síntomas y se logra una mejor diferenciación de los pacientes por subtipo de EOS, existe una creciente necesidad de entender los beneficios relativos de las numerosas opciones disponibles para tratar el OSDA y la ESO.
Pese a que se necesita más investigación para dar la respuesta a las preguntas que se planteaban más arriba, el creciente rango de posibles soluciones y el continuo respaldo del sector y las agencias de financiación mediante subvenciones proporciona una perspectiva positiva para los pacientes afectados en un futuro.
12. Declaraciones financieras volver arriba
Gestión y tratamiento
L. Jones, Presidente: Advanced Vision Research, Alcon, Allergan, Contamac, CooperVision, Essilor, In?amax, Johnson & Johnson Vision Care, Ocular Dynamics, Oculus, Sa?lens, TearLab, TearScience (F); Alcon, CooperVision, Johnson & Johnson Vision Care (C) (R).
J. Benítez de Castillo Sánchez: Abbvie, Alcon, Allergan, Angelini, Bausch + Lomb, Dompé, Esteve, Horus, Laboratoires Théa, Novartis, Santen (F) (C).
R. Dana: Eleven Biotherapeutics (I); Alcon, Allergan, Cambium, Eleven Biotherapeutics, NovaBay, Rigel, Shire (C).
S. Deng: Chiesi Farmaceutici S.P.A. (C).
P. N. Dong: Ninguna.
L. Downie: Alcon, Allergan, CooperVision (F).
G. Geerling; TearLab, TearScience (F); TearLab (I); Allergan, Bausch + Lomb, Laboratoires Théa, Oculus, Santen, TearLab, TearScience (C).
R. Y. Hida: Ninguna.
D. Jacobs: BostonSight (E); TECLens (C).
D. Korb: Inventor en relación con el ojo seco (P).
Y. Liu: Copropietario de la patente junto con el Schepens Eye Research Institute (P).
K. Y. Seo: Ninguna.
J. Tauber: Eleven Biotherapeutics, Kala, Shire (F); Shire (C); Allergan, Eleven Biotherapeutics, Shire (R).
T. Wakamatsu: Ninguna.
J. Xu: Ninguna.
J. P. Craig, miembro de armonización y vicepresidente: Oculeve, Allergan, Manuka Health NZ, E-Swin, CooperVision, Alcon, Optima Pharmaceuticals, OPSM NZ, Akorn, Medmont (F); Carl Zeiss Meditec, Eye Institute Auckland (C).
F (Soporte financiero), I (Interés financiero personal), E (Empleo), C (Consultor), P (Patente), R (Receptor), N (Relación no comercial), S (No remunerado).
A los autores les gustaría expresar su agradecimiento a los miembros de TFOS y, en particular, a las siguientes personas por su ayuda en las distintas secciones de este informe: Francisco Amparo, Penny Asbell, Caroline Blackie, Stephanie Cox, Teresa Douglass, Anat Galor, Pedram Hamrah, Jiaxu Hong, Deborah Jacobs, Ahmad Kheirkhah, Nino Longo, Amy Nau, Mark Rosenblatt, Benjamin Sullivan, Kunal Suri, Stephanie Wong, Sabrina Zappia.
14. Referencias bibliográficas volver arriba
[1] Management and therapy of dry eye disease: report of the management and therapy subcommittee of the international dry eye WorkShop. Ocul Surf 2007;2007(5):163–178.
[2] Nelson JD, Shimazaki J, Benitez-del-Castillo JM, Craig JP, McCulley JP, Den S, et al. The international workshop on meibomian gland dysfunction: report of the definition and classification subcommittee. Invest Ophthalmol Vis Sci 2011;52(4):1930–1937.
[3] Craig JP, Nichols KK, Akpek EK, Caffery B, Dua HS, Joo CK, et al. TFOS DEWS II Definition and Classification report. Ocul Surf 2017;15:276–283.
[4] Lemp MA, Crews LA, Bron AJ, Foulks GN, Sullivan BD. Cornea 2012;31(5):472–478.
[5] Williamson JF, Huynh K, Weaver MA, Davis RM. Perceptions of dry eye disease management in current clinical practice. Eye Contact Lens 2014;40(2):111–115.
[6] Song JS, Hyon JY, Lee D, Chung E, Choi C, Lee J, et al. Current practice pattern for dry eye patients in South Korea: a multicenter study. Korean J Ophthalmol 2014;28(2):115–121.
[7] Sy A, O'Brien KS, Liu MP, Cuddapah PA, Acharya NR, Lietman TM, et al. Expert opinion in the management of aqueous deficient dry eye disease (DED). BMC Ophthalmol 2015;15:133.
[8] Downie LE, Keller PR, Vingrys AJ. An evidence-based analysis of Australian optometrists' dry eye practices. Optom Vis Sci 2013;90(12):1385–1395.
[9] Downie LE, Rumney N, Gad A, Keller PR, Purslow C, Vingrys AJ. Comparing self-reported optometric dry eye clinical practices in Australia and the United Kingdom: is there scope for practice improvement? Ophthalmic Physiol Opt 2016;36(2):140–151.
[10] Wolffsohn JS, Arita R, Chalmers R, Djalilian A, Dogru M, Dumbleton K, et al. TFOS DEWS II Diagnostic Methodology report. Ocul Surf 2017;15:539–574.
[11] Tong L, Petznick A, Lee S, Tan J. Choice of artificial tear formulation for patients with dry eye: where do we start? Cornea 2012;31(Suppl 1):S32–S36.
[12] Murube J, Paterson A, Murube E. Classification of artificial tears. I: composition and properties. Adv Exp Med Biol 1998;438:693–704.
[13] Murube J, Murube A, Zhuo C. Classification of artificial tears. II: additives and commercial formulas. Adv Exp Med Biol 1998;438:705–715.
[14] Dogru M, Nakamura M, Shimazaki J, Tsubota K. Changing trends in the treatment of dry-eye disease. Expert Opin Invest Drugs 2013;22(12):1581–1601.
[15] Dogru M, Tsubota K. Pharmacotherapy of dry eye. Expert Opin Pharmacother 2011;12(3):325–334.
[16] Pucker AD, Ng SM, Nichols JJ. Over the counter (OTC) artificial tear drops for dry eye syndrome. Cochrane Database Syst Rev 2016;2:CD009729.
[17] Downie LE, Keller PR. A pragmatic approach to dry eye diagnosis: evidence into practice. Optom Vis Sci 2015;92(12):1189–1197.
[18] Wegener AR, Meyer LM, Schönfeld CL. Effect of viscous agents on corneal density in dry eye disease. J Ocul Pharmacol Ther 2015;31(8):504–508.
[19] Yu F, Liu X, Zhong Y, Guo X, Li M, Mao Z, et al. Sodium hyaluronate decreases ocular surface toxicity induced by benzalkonium chloride-preserved latanoprost: an in vivo study. Invest Ophthalmol Vis Sci 2013;54:3385–3393.
[20] Doughty MJ, Glavin S. Efficacy of different dry eye treatments with artificial tears or ocular lubricants: a systematic review. Ophthalmic Physiol Opt 2009;29(6):573–583.
[21] Kamel S, Ali N, Jahangir K, Shah SM, El-Gendy AA. Pharmaceutical significance of cellulose: a review. Express Polym Lett 2008;2(11):758–778.
[22] Garrett Q, Simmons PA, Xu S, Vehige J, Zhao Z, Ehrmann K, et al. Carboxymethylcellulose binds to human corneal epithelial cells and is a modulator of corneal epithelial wound healing. Invest Ophthalmol Vis Sci 2007;48(4):1559–1567.
[23] Garrett Q, Xu S, Simmons PA, Vehige J, Xie RZ, Kumar A, et al. Carboxymethyl cellulose stimulates rabbit corneal epithelial wound healing. Curr Eye Res 2008;33(7):567–573.
[24] Bruix A, Adan A, Casaroli-Marano RP. Efficacy of sodium carboxymethylcellulose in the treatment of dry eye syndrome. Arch Soc Esp Oftalmol 2006;81:85–92.
[25] Noecker RJ. Comparison of initial treatment response to two enhanced-viscosity artificial tears. Eye Contact Lens 2006;32(3):148–152.
[26] Lee JH, Ahn HS, Kim EK, Kim TI. Efficacy of sodium hyaluronate and carboxymethylcellulose in treating mild to moderate dry eye disease. Cornea 2011;30(2):175–179.
[27] Rah MJ. A review of hyaluronan and its ophthalmic applications. Optometry 2011;82(1):38–43.
[28] Inoue M, Katakami C. The effect of hyaluronic acid on corneal epithelial cell proliferation. Invest Ophthalmol Vis Sci 1993;34(7):2313–2315.
[29] Stiebel-Kalish H, Gaton DD, Weinberger D, Loya N, Schwartz-Ventik M, Solomon A. A comparison of the effect of hyaluronic acid versus gentamicin on corneal epithelial healing. Eye (Lond) 1998;12(5):829–833.
[30] Gomes JA, Amankwah R, Powell-Richards A, Dua HS. Sodium hyaluronate (hyaluronic acid) promotes migration of human corneal epithelial cells in vitro. Br J Ophthalmol 2004;88(6):821–825.
[31] Camillieri G, Bucolo C, Rossi S, Drago F. Hyaluronan-induced stimulation of corneal wound healing is a pure pharmacological effect. J Ocul Pharmacol Ther 2004;20(6):548–553.
[32] Yang G, Espandar L, Mamalis N, Prestwich GD. A cross-linked hyaluronan gel accelerates healing of corneal epithelial abrasion and alkali burn injuries in rabbits. Vet Ophthalmol 2010;13(3):144–150.
[33] Ho WT, Chiang TH, Chang SW, Chen YH, Hu FR, Wang IJ. Enhanced corneal wound healing with hyaluronic acid and high-potassium artificial tears. Clin Exp Optom 2013;96(6):536–541.
[34] Pisár?ik M, Bakoš D, ?eppan M. Non-Newtonian properties of hyaluronic acid aqueous solution. Colloids Surf A 1995;97:197–202.
[35] Johnson ME, Murphy PJ, Boulton M. Carbomer and sodium hyaluronate eyedrops for moderate dry eye treatment. Optom Vis Sci 2008;85(8):750–757.
[36] Lekhanont K, Chuckpaiwong V, Vongthongsri A, Sangiampornpanit T. Effects of sodium hyaluronate on wavefront aberrations in dry eye patients. Optom Vis Sci 2014;91(1):39–46.
[37] Kinoshita S, Oshiden K, Awamura S, Suzuki H, Nakamichi N, Yokoi N, ; Rebamipide Ophthalmic Suspension Phase 3 Study Group.. A randomized, multicenter phase 3 study comparing 2% rebamipide (OPC-12759) with 0.1% sodium hyaluronate in the treatment of dry eye. Ophthalmology 2013;120(6):1158–1165.
[38] Takamura Etsuko, Tsubota Kazuo, Watanabe Hitoshi, Ohashi Yuichi. A randomised, double-masked comparison study of diquafosol versus sodium hyaluronate ophthalmic solutions in dry eye patients. Br J Ophthalmol 2012;96(10):1310–1315.
[39] Cheema A, Aziz T, Mirza SA, Siddiqi A, Maheshwary N, Khan MA. Sodium hyaluronate eye drops in the treatment of dry eye disease: an open label, uncontrolled, multi-centre trial. J Ayub Med Coll Abbottabad 2012 Jul-Dec;24(3–4):14–16.
[40] Baudouin C, Cochener B, Pisella PJ, Girard B, Pouliquen P, Cooper H, et al. Randomized, phase III study comparing osmoprotective carboxymethylcellulose with sodium hyaluronate in dry eye disease. Eur J Ophthalmol 2012 Sep-Oct;22(5):751–761.
[41] Pinto-Fraga J, Lopez-de la Rosa A, Blazquez Arauzo F, Urbano Rodriguez R, Gonzalez-Garcia MJ. Efficacy and safety of 0.2% hyaluronic acid in the management of dry eye disease. Eye Contact Lens 2017;43:57–63.
[42] Park Y, Song JS, Choi CY, Yoon KC, Lee HK, Kim HS. A randomized multicenter Study comparing 0.1%, 0.15%, and 0.3% sodium hyaluronate with 0.05% cyclosporine in the treatment of dry eye. J Ocul Pharmacol Ther 2017;33(2):66–72.
[43] She Y, Li J, Xiao B, Lu H, Liu H, Simmons PA, et al. Evaluation of a novel artificial tear in the prevention and treatment of dry eye in an animal model. J Ocul Pharmacol Ther 2015;31(9):525–530.
[44] Simmons PA, Liu H, Carlisle-Wilcox C, Vehige JG. Efficacy and safety of two new formulations of artificial tears in subjects with dry eye disease: a 3-month, multicenter, active-controlled, randomized trial. Clin Ophthalmol 2015;9:665–675.
[45] Springs C. Novel ocular lubricant containing an intelligent delivery system: details of its mechanism of action. Dev Ophthalmol 2010;45:139–147.
[46] Benelli U. Systane lubricant eye drops in the management of ocular dryness. Clin Ophthalmol 2011;5:783–790.
[47] Christensen MT. Corneal staining reductions observed after treatment with Systane lubricant eye drops. Adv Ther 2008;25(11):1191–1199.
[48] Ousler GW, Michaelson C, Christensen MT. An evaluation of tear film breakup time extension and ocular protection index scores among three marketed lubricant eye drops. Cornea 2007;26(8):949–952.
[49] Cervan-Lopez I, Saenz-Frances-San-Baldomero F, Benitez-Del-Castillo JM, Garcia-Sanchez J. Reduction of corneal permeability in patients treated with HP-guar: a fluorophotometric study. Arch Soc Esp Oftalmol 2006;81:327–332.
[50] Moon SW, Hwang JH, Chung SH, Nam KH. The impact of artificial tears containing hydroxypropyl guar on mucous layer. Cornea 2010;29(12):1430–1435.
[51] Uchiyama E, Di Pascuale MA, Butovich IA, McCulley JP. Impact on ocular surface evaporation of an artificial tear solution containing hydroxypropyl guar. Eye Contact Lens 2008;34(6):331–334.
[52] Sánchez MA, Arriola-Villalobos P, Torralbo-Jiménez P, Girón N, de la Heras B, Herrero Vanrell R, et al. The effect of preservative-free HP-Guar on dry eye after phacoemulsification: a flow cytometric study. Eye (Lond) 2010;24(8):1331–1337.
[53] Gifford P, Evans BJ, Morris J. A clinical evaluation of Systane. Cont Lens Anter Eye 2006;29(1):31–40.
[54] Rangarajan R, Kraybill B, Ogundele A, Ketelson HA. Effects of a hyaluronic acid/hydroxypropyl guar artificial tear solution on protection, recovery, and lubricity in models of corneal epithelium. J Ocul Pharmacol Ther 2015;31(8):491–497.
[55] Werblin TP, Rheinstrom SD, Kaufman HE. The use of slow-release artificial tears in the long-term management of keratitis sicca. Ophthalmology 1981;88(1):78–81.
[56] McDonald M, D'Aversa G, Perry HD, Wittpenn JR, Donnenfeld ED, Nelinson DS. Hydroxypropyl cellulose ophthalmic inserts (lacrisert) reduce the signs and symptoms of dry eye syndrome and improve patient quality of life. Trans Am Ophthalmol Soc 2009;107:214–221.
[57] The definition and classification of dry eye disease: report of the definition and classification subcommittee of the international dry eye WorkShop. Ocul Surf 2007;2007(5):75–92.
[58] Gilbard JP, Rossi SR, Heyda KG. Ophthalmic solutions, the ocular surface, and a unique therapeutic artificial tear formulation. Am J Ophthalmol 1989;107(4):348–355.
[59] Gilbard JP, Rossi SR. An electrolyte-based solution that increases corneal glycogen and conjunctival goblet-cell density in a rabbit model for keratoconjunctivitis sicca. Ophthalmology 1992;99(4):600–604.
[60] Gilbard JP. Dry eye: pharmacological approaches, effects, and progress. CLAO J 1996;22(2):141–145.
[61] Troiano P, Monaco G. Effect of hypotonic 0.4% hyaluronic acid drops in dry eye patients: a cross-over study. Cornea 2008;27(10):1126–1130.
[62] Baeyens V, Bron A, Baudouin C, Vismed/Hylovis Study Group. Efficacy of 0.18% hypotonic sodium hyaluronate ophthalmic solution in the treatment of signs and symptoms of dry eye disease. J Fr Ophtalmol 2012;35(6):412–419.
[63] Sullivan BD, Crews LA, Sönmez B, de la Paz MF, Comert E, Charoenrook V, et al. Clinical utility of objective tests for dry eye disease: variability over time and implications for clinical trials and disease management. Cornea 2012;31(9):1000–1008.
[64] Scuderi G, Contestabile MT, Gagliano C, Iacovello D, Scuderi L, Avitabile T. Effects of phytoestrogen supplementation in postmenopausal women with dry eye syndrome: a randomized clinical trial. Can J Ophthalmol 2012;47(6):489–492.
[65] Tomlinson A, Madden LC, Simmons PA. Effectiveness of dry eye therapy under conditions of environmental stress. Curr Eye Res 2013;38(2):229–236.
[66] Versura P, Profazio V, Giannaccare G, Fresina M, Campos EC. Discomfort symptoms reduction and ocular surface parameters recovery with Artelac Rebalance treatment in mild-moderate dry eye. Eur J Ophthalmol 2013 Jul-Aug;23(4):488–495.
[67] Montani G. Intrasubject tear osmolarity changes with two different types of eyedrops. Optom Vis Sci 2013;90(4):372–377.
[68] Lee JE, Kim NM, Yang JW, Kim SJ, Lee JS, Lee JE. A randomised controlled trial comparing a thermal massager with artificial teardrops for the treatment of dry eye. Br J Ophthalmol 2014;98(1):46–51.
[69] Aslan Bayhan S, Bayhan HA, Muhaf?z E, Bekdemir ?, Gürdal C. Effects of osmoprotective eye drops on tear osmolarity in contact lens wearers. Can J Ophthalmol 2015;50(4):283–289.
[70] Miserocchi E, Iuliano L, Berchicci L, Bandello F, Modorati G. Tear film osmolarity in ocular mucous membrane pemphigoid. Cornea 2014;33(7):668–672.
[71] Gilbard JP, Huang AJ, Belldegrun R, Lee JS, Rossi SR, Gray KL. Open-label crossover study of vitamin A ointment as a treatment for keratoconjunctivitis sicca. Ophthalmology 1989;96(2):244–246.
[72] Finis D, Hayajneh J, König C, Borrelli M, Schrader S, Geerling G. Evaluation of an automated thermodynamic treatment (LipiFlow®) system for meibomian gland dysfunction: a prospective, randomized, observer-masked trial. Ocul Surf 2014;12(2):146–154.
[73] Mathers WD, Shields WJ, Sachdev MS, Petroll WM, Jester JV. Meibomian gland morphology and tear osmolarity: changes with Accutane therapy. Cornea 1991;10(4):286–290.
[74] Labbé A, Terry O, Brasnu E, Van Went C, Baudouin C. Tear film osmolarity in patients treated for glaucoma or ocular hypertension. Cornea 2012;31(9):994–999.
[75] Lee JH, Min K, Kim SK, Kim EK, Kim TI. Inflammatory cytokine and osmolarity changes in the tears of dry eye patients treated with topical 1% methylprednisolone. Yonsei Med J 2014;55(1):203–208.
[76] Jadidi K, Panahi Y, Ebrahimi A, Mafi M, Nejat F, Sahebkar A. Topical cyclosporine a for treatment of dry eye due to chronic mustard gas injury. J Ophthalmic Vis Res 2014 Oct-Dec;9(4):417–422.
[77] Hamada S, Moore TC, Moore JE, Al-Dreihi MG, Anbari A, Shah S. Assessment of the effect of cyclosporine-A 0.05% emulsion on the ocular surface and corneal sensation following cataract surgery. Cont Lens Anter Eye 2016;39(1):15–19.
[78] Nelson JD, Farris RL. Sodium hyaluronate and polyvinyl alcohol artificial tear preparations. A comparison in patients with keratoconjunctivitis sicca. Arch Ophthalmol 1988;106(4):484–487.
[79] Iester M, Orsoni GJ, Gamba G, Taffara M, Mangiafico P, Giuffrida S, et al. Improvement of the ocular surface using hypotonic 0.4% hyaluronic acid drops in keratoconjunctivitis sicca. Eye (Lond) 2000;14(Pt 6):892–898.
[80] Benelli U, Nardi M, Posarelli C, Albert TG. Tear osmolarity measurement using the TearLab Osmolarity System in the assessment of dry eye treatment effectiveness. Cont Lens Anter Eye 2010;33(2):61–67.
[81] Cömez AT, Tufan HA, Kocab?y?k O, Gencer B. Effects of lubricating agents with different osmolalities on tear osmolarity and other tear function tests in patients with dry eye. Curr Eye Res 2013;38(11):1095–1103.
[82] Garrett Q, Xu S, Simmons PA, Vehige J, Flanagan JL, Willcox MD. Expression and localization of carnitine/organic cation transporter OCTN1 and OCTN2 in ocular epithelium. Invest Ophthalmol Vis Sci 2008;49(11):4844–4849.
[83] Xu S, Flanagan JL, Simmons PA, Vehige J, Willcox MD, Garrett Q. Transport of L-carnitine in human corneal and conjunctival epithelial cells. Mol Vis 2010;16:1823–1831.
[84] Khandekar N, Willcox MD, Shih S, Simmons P, Vehige J, Garrett Q. Decrease in hyperosmotic stress-induced corneal epithelial cell apoptosis by L-carnitine. Mol Vis 2013;19:1945–1956.
[85] Garrett Q, Khandekar N, Shih S, Flanagan JL, Simmons P, Vehige J, et al. Betaine stabilizes cell volume and protects against apoptosis in human corneal epithelial cells under hyperosmotic stress. Exp Eye Res 2013;108:33–41.
[86] Corrales RM, Luo L, Chang EY, Pflugfelder SC. Effects of osmoprotectants on hyperosmolar stress in cultured human corneal epithelial cells. Cornea 2008;27(5):574–579.
[87] Hua X, Su Z, Deng R, Lin J, Li DQ, Pflugfelder SC. Effects of L-carnitine, erythritol and betaine on pro-inflammatory markers in primary human corneal epithelial cells exposed to hyperosmotic stress. Curr Eye Res 2015;40(7):657–667.
[88] Chen W, Zhang X, Li J, Wang Y, Chen Q, Hou C, et al. Efficacy of osmoprotectants on prevention and treatment of murine dry eye. Invest Ophthalmol Vis Sci 2013;54(9):6287–6297.
[89] Baudouin C, Aragona P, Messmer EM, Tomlinson A, Calonge M, Boboridis KG, et al. Role of hyperosmolarity in the pathogenesis and management of dry eye disease: proceedings of the OCEAN group meeting. Ocul Surf 2013;11(4):246–258.
[90] Chen W, Zhang X, Liu M, Zhang J, Ye Y, Lin Y, et al. Trehalose protects against ocular surface disorders in experimental murine dry eye through suppression of apoptosis. Exp Eye Res 2009;89(3):311–318.
[91] Hovakimyan M, Ramoth T, Löbler M, Schmitz KP, Witt M, Guthoff R, et al. Evaluation of protective effects of trehalose on desiccation of epithelial cells in three dimensional reconstructed human corneal epithelium. Curr Eye Res 2012;37(11):982–989.
[92] Li J, Roubeix C, Wang Y, Shi S, Liu G, Baudouin C, et al. Therapeutic efficacy of trehalose eye drops for treatment of murine dry eye induced by an intelligently controlled environmental system. Mol Vis 2012;18:317–329.
[93] Iturriaga G, Suárez R, Nova-Franco B. Trehalose metabolism: from osmoprotection to signaling. Int J Mol Sci 2009;10(9):3793–3810.
[94] Luyckx J, Baudouin C. Trehalose: an intriguing disaccharide with potential for medical application in ophthalmology. Clin Ophthalmol 2011;5:577–581.
[95] Matsuo T. Trehalose protects corneal epithelial cells from death by drying. Br J Ophthalmol 2001;85(5):610–612.
[96] Sarkar S, Davies JE, Huang Z, Tunnacliffe A, Rubinsztein DC. Trehalose, a novel mTOR-independent autophagy enhancer, accelerates the clearance of mutant huntingtin and alpha-synuclein. J Biol Chem 2007;282(8):5641–5652.
[97] Cejková J, Cejka C, Luyckx J. Trehalose treatment accelerates the healing of UVB-irradiated corneas. Comparative immunohistochemical studies on corneal cryostat sections and corneal impression cytology. Histol Histopathol 2012;27(8):1029–1040.
[98] Baudouin C, Labbé A, Liang H, Pauly A, Brignole-Baudouin F. Preservatives in eyedrops: the good, the bad and the ugly. Prog Retin Eye Res 2010;29(4):312–334.
[99] Augustin AJ, Spitznas M, Kaviani N, Meller D, Koch FH, Grus F, et al. Oxidative reactions in the tear fluid of patients suffering from dry eyes. Graefes Arch Clin Exp Ophthalmol 1995;233(11):694–698.
[100] Hongyok T, Chae JJ, Shin YJ, Na D, Li L, Chuck RS. Effect of chitosan-N-acetylcysteine conjugate in a mouse model of botulinum toxin B-induced dry eye. Arch Ophthalmol 2009;127(4):525–532.
[101] Kim EC, Choi JS, Joo CK. A comparison of vitamin a and cyclosporine a 0.05% eye drops for treatment of dry eye syndrome. Am J Ophthalmol 2009;147(2):206–213. e3.
[102] Gomes JAP, Azar DT, Baudouin C, Efron N, Hirayama M, Horwath-Winter J, et al. TFOS DEWS II Iatrogenic report. Ocul Surf 2017;15:511–538.
[103] Stoddard AR, Koetje LR, Mitchell AK, Schotanus MP, Ubels JL. Bioavailability of antioxidants applied to stratified human corneal epithelial cells. J Ocul Pharmacol Ther 2013;29(7):681–687.
[104] Brzheskiy VV, Efimova EL, Vorontsova TN, Alekseev VN, Gusarevich OG, Shaidurova KN, Ryabtseva AA, Andryukhina OM, Kamenskikh TG, Sumarokova ES, Miljudin ES, Egorov EA, Lebedev OI, Surov AV, Korol AR, Nasinnyk IO, Bezditko PA, Muzhychuk OP, Vygodin VA, Yani EV, Savchenko AY, Karger EM, Fedorkin ON, Mironov AN, Ostapenko V, Popeko NA, Skulachev VP, Skulachev MV, et al. Results of a multicenter, randomized, double-masked, placebo-controlled clinical study of the efficacy and safety of Visomitin eye drops in patients with dry eye syndrome. Adv Ther 2015;32(12):1263–1279.
[105] Mostert V. Selenoprotein P: properties, functions, and regulation. Arch Biochem Biophys 2000;376(2):433–438.
[106] Higuchi A, Takahashi K, Hirashima M, Kawakita T, Tsubota K. Selenoprotein P controls oxidative stress in cornea. PLoS One 2010;5:e9911.
[107] Baudouin C. The pathology of dry eye. Surv Ophthalmol 2001;45(Suppl 2):S211–S220.
[108] Noecker R. Effects of common ophthalmic preservatives on ocular health. Adv Ther 2001 Sep-Oct;18(5):205–215.
[109] Stewart WC, Stewart JA, Nelson LA. Ocular surface disease in patients with ocular hypertension and glaucoma. Curr Eye Res 2011;36(5):391–398.
[110] Mantelli F, Tranchina L, Lambiase A, Bonini S. Ocular surface damage by ophthalmic compounds. Curr Opin Allergy Clin Immunol 2011;11(5):464–470.
[111] Stalmans I, Sunaric Mégevand G, Cordeiro MF, Hommer A, Rossetti L, Goñi F, et al. Preservative-free treatment in glaucoma: who, when, and why. Eur J Ophthalmol 2013 Jul-Aug;23(4):518–525.
[112] Anwar Z, Wellik SR, Galor A. Glaucoma therapy and ocular surface disease: current literature and recommendations. Curr Opin Ophthalmol 2013;24(2):136–143.
[113] Pinheiro R, Panfil C, Schrage N, Dutescu RM. The impact of glaucoma medications on corneal wound healing. J Glaucoma 2016;25(1):122–127.
[114] Chen W, Zhang Z, Hu J, Xie H, Pan J, Dong N, et al. Changes in rabbit corneal innervation induced by the topical application of benzalkonium chloride. Cornea 2013;32(12):1599–1606.
[115] Lin Z, He H, Zhou T, Liu X, Wang Y, He H, et al. A mouse model of limbal stem cell deficiency induced by topical medication with the preservative benzalkonium chloride. Invest Ophthalmol Vis Sci 2013;54(9):6314–6325.
[116] Kaercher T, Hönig D, Barth W. How the most common preservative affects the Meibomian lipid layer. Orbit 1999;18(2):89–97.
[117] Schrage N, Frentz M, Spoeler F. The Ex Vivo Eye Irritation Test (EVEIT) in evaluation of artificial tears: Purite-preserved versus unpreserved eye drops. Graefes Arch Clin Exp Ophthalmol 2012;250(9):1333–1340.
[118] Jee D, Park SH, Kim MS, Kim EC. Antioxidant and inflammatory cytokine in tears of patients with dry eye syndrome treated with preservative-free versus preserved eye drops. Invest Ophthalmol Vis Sci 2014;55(8):5081–5089.
[119] Bernauer W, Thiel MA, Kurrer M, Heiligenhaus A, Rentsch KM, Schmitt A, et al. Corneal calcification following intensified treatment with sodium hyaluronate artificial tears. Br J Ophthalmol 2006;90(3):285–288.
[120] Imayasu M, Hori Y, Cavanagh HD. Effects of multipurpose contact lens care solutions and their ingredients on membrane-associated mucins of human corneal epithelial cells. Eye Contact Lens 2010;36(6):361–366.
[121] Lehmann DM, Cavet ME, Richardson ME. Nonclinical safety evaluation of boric acid and a novel borate-buffered contact lens multi-purpose solution, Biotrue multi-purpose solution. Cont Lens Anter Eye 2010;33(Suppl 1):S24–S32.
[122] Pelton R, Hu Z, Ketelson H, Meadows D. Reversible flocculation with hydroxypropyl guar-borate, a labile anionic polyelectrolyte. Langmuir 2009;25(1):192–195.
[123] Khanal A, Cui Y, Zhang L, Pelton R, Ren Y, Ketelson H, et al. Cationic liposome colloidal stability in the presence of guar derivatives suggests depletion interactions may be operative in artificial tears. Biomacromolecules 2010;11(9):2460–2464.
[124] Saarinen-Savolainen P, Järvinen T, Araki-Sasaki K, Watanabe H, Urtti A. Evaluation of cytotoxicity of various ophthalmic drugs, eye drop excipients and cyclodextrins in an immortalized human corneal epithelial cell line. Pharm Res 1998;15(8):1275–1280.
[125] Viaud-Quentric K, Lefranc-Jullien S, Feraille L, Elena PP. Long-term tolerance of preservative-free eye drops containing macrogol hydroxystearate as an excipient. J Fr Ophtalmol 2016;39(2):156–163.
[126] Smedowski A, Paterno JJ, Toropainen E, Sinha D, Wylegala E, Kaarniranta K. Excipients of preservative-free latanoprost induced inflammatory response and cytotoxicity in immortalized human HCE-2 corneal epithelial cells. J Biochem Pharmacol Res 2014;2:175–184.
[127] Gensheimer WG, Kleinman DM, Gonzalez MO, Sobti D, Cooper ER, Smits G, et al. Novel formulation of glycerin 1% artificial tears extends tear film break-up time compared with Systane lubricant eye drops. J Ocul Pharmacol Ther 2012;28(5):473–478.
[128] Willcox MDP, Argüeso P, Georgiev GA, Holopainen JM, Laurie GW, Millar TJ, et al. TFOS DEWS II Tear Film report. Ocul Surf 2017;15:366–403.
[129] Tiffany JM. Tears in health and disease. Eye (Lond) 2003;17(8):923–926.
[130] Stahl U, Willcox M, Stapleton F. Osmolality and tear film dynamics. Clin Exp Optom 2012;95(1):3–11.
[131] Schotanus MP, Koetje LR, Van Dyken RE, Ubels JL. Stratified corneal limbal epithelial cells are protected from UVB-induced apoptosis by elevated extracellular K?. Exp Eye Res 2011;93(5):735–740.
[132] Ubels JL, Schotanus MP, Bardolph SL, Haarsma LD, Koetje LR, Louters JR. Inhibition of UV-B induced apoptosis in corneal epithelial cells by potassium channel modulators. Exp Eye Res 2010;90(2):216–222.
[133] Green K, MacKeen DL, Slagle T, Cheeks L. Tear potassium contributes to maintenance of corneal thickness. Ophthalmic Res 1992;24(2):99–102.
[134] Bachman WG, Wilson G. Essential ions for maintenance of the corneal epithelial surface. Invest Ophthalmol Vis Sci 1985;26(11):1484–1488.
[135] Smolin G, Foster CS, Azar DT, Dohlman CH. Smolin and Thoft's The Cornea: Scientific Foundations and Clinical Practice. 4thLippincott Williams & Wilkins ed Lippincott Williams & Wilkins; 2005.
[136] Lopez Bernal D, Ubels JL. Artificial tear composition and promotion of recovery of the damaged corneal epithelium. Cornea 1993;12(2):115–120.
[137] Ubels JL, McCartney MD, Lantz WK, Beaird J, Dayalan A, Edelhauser HF. Effects of preservative-free artificial tear solutions on corneal epithelial structure and function. Arch Ophthalmol 1995;113(3):371–378.
[138] Craig JP, Tomlinson A. Importance of the lipid layer in human tear film stability and evaporation. Optom Vis Sci 1997;74(1):8–13.
[139] Lee SY, Tong L. Lipid-containing lubricants for dry eye: a systematic review. Optom Vis Sci 2012;89(11):1654–1661.
[140] Moshirfar M, Pierson K, Hanamaikai K, Santiago-Caban L, Muthappan V, Passi SF. Artificial tears potpourri: a literature review. Clin Ophthalmol 2014;8:1419–1433.
[141] Korb DR, Scaffidi RC, Greiner JV, Kenyon KR, Herman JP, Blackie CA, et al. The effect of two novel lubricant eye drops on tear film lipid layer thickness in subjects with dry eye symptoms. Optom Vis Sci 2005;82(7):594–601.
[142] Scaffidi RC, Korb DR. Comparison of the efficacy of two lipid emulsion eyedrops in increasing tear film lipid layer thickness. Eye Contact Lens 2007;33(1):38–44.
[143] Mason TG, Wilking JN, Meleson K, Chang CB, Graves SM. Nanoemulsions: formation, structure, and physical properties. J Phys Condens Matter 2006;18:R635.
[144] Royle L, Matthews E, Corfield A, Berry M, Rudd PM, Dwek RA, et al. Glycan structures of ocular surface mucins in man, rabbit and dog display species differences. Glycoconj J 2008;25(8):763–773.
[145] Daull P, Lallemand F, Garrigue JS. Benefits of cetalkonium chloride cationic oil-in-water nanoemulsions for topical ophthalmic drug delivery. J Pharm Pharmacol 2014;66(4):531–541.
[146] Amrane M, Creuzot-Garcher C, Robert PY, Ismail D, Garrigue JS, Pisella PJ, et al. Ocular tolerability and efficacy of a cationic emulsion in patients with mild to moderate dry eye disease - a randomised comparative study. J Fr Ophtalmol 2014;37(8):589–598.
[147] Zhang W, Wang Y, Lee BT, Liu C, Wei G, Lu W. A novel nanoscale-dispersed eye ointment for the treatment of dry eye disease. Nanotechnology 2014;25(12):125101.
[148] Lallemand F, Daull P, Benita S, Buggage R, Garrigue JS. Successfully improving ocular drug delivery using the cationic nanoemulsion, novasorb. J Drug Deliv 2012;2012:604204.
[149] Kinnunen K, Kauppinen A, Piippo N, Koistinen A, Toropainen E, Kaarniranta K. Cationorm shows good tolerability on human HCE-2 corneal epithelial cell cultures. Exp Eye Res 2014;120:82–89.
[150] Pinheiro R, Panfil C, Schrage N, Dutescu RM. Comparison of the lubricant eyedrops Optive®, Vismed Multi®, and Cationorm® on the corneal healing process in an ex vivo model. Eur J Ophthalmol 2015 Sep-Oct;25(5):379–384.
[151] Yoncheva K, Vandervoort J, Ludwig A. Development of mucoadhesive poly(lactide-co-glycolide) nanoparticles for ocular application. Pharm Dev Technol 2011;16(1):29–35.
[152] Paolicelli P, de la Fuente M, Sánchez A, Seijo B, Alonso MJ. Chitosan nanoparticles for drug delivery to the eye. Expert Opin Drug Deliv 2009;6(3):239–253.
[153] De Campos AM, Sánchez A, Alonso MJ. Chitosan nanoparticles: a new vehicle for the improvement of the delivery of drugs to the ocular surface. Application to cyclosporin A. Int J Pharm 2001;224(1–2):159–168.
[154] Rieger G. Lipid-containing eye drops: a step closer to natural tears. Ophthalmologica 1990;201(4):206–212.
[155] Choi JH, Kim JH, Li Z, Oh HJ, Ahn KY, Yoon KC. Efficacy of the mineral oil and hyaluronic acid mixture eye drops in murine dry eye. Korean J Ophthalmol 2015;29(2):131–137.
[156] Katzer T, Chaves P, Bernardi A, Pohlmann AR, Guterres SS, Beck RC. Castor oil and mineral oil nanoemulsion: development and compatibility with a soft contact lens. Pharm Dev Technol 2014;19(2):232–237.
[157] Maïssa C, Guillon M, Simmons P, Vehige J. Effect of castor oil emulsion eyedrops on tear film composition and stability. Cont Lens Anter Eye 2010;33(2):76–82.
[158] Moscovici BK, Holzchuh R, Chiacchio BB, Santo RM, Shimazaki J, Hida RY. Clinical treatment of dry eye using 0.03% tacrolimus eye drops. Cornea 2012;31(8):945–949.
[159] Rantamäki AH, Javanainen M, Vattulainen I, Holopainen JM. Do lipids retard the evaporation of the tear fluid? Invest Ophthalmol Vis Sci 2012;53(10):6442–6447.
[160] Parrilha LR, Nai GA, Giuffrida R, Barbero RC, Padovani LD, Pereira RH, et al. Comparison of 1% cyclosporine eye drops in olive oil and in linseed oil to treat experimentally-induced keratoconjunctivitis sicca in rabbits. Arq Bras Oftalmol 2015 Sep-Oct;78(5):295–299.
[161] Radomska-Soukharev A, Wojciechowska J. Microemulsions as potential ocular drug delivery systems: phase diagrams and physical properties depending on ingredients. Acta Pol Pharm 2005 Nov-Dec;62(6):465–471.
[162] Greiner JV, Glonek T, Korb DR, Booth R, Leahy CD. Phospholipids in meibomian gland secretion. Ophthalmic Res 1996;28(1):44–49.
[163] Dean AW, Glasgow BJ. Mass spectrometric identification of phospholipids in human tears and tear lipocalin. Invest Ophthalmol Vis Sci 2012;53(4):1773–1782.
[164] Ham BM, Cole RB, Jacob JT. Identification and comparison of the polar phospholipids in normal and dry eye rabbit tears by MALDI-TOF mass spectrometry. Invest Ophthalmol Vis Sci 2006;47(8):3330–3338.
[165] Shine WE, McCulley JP. Keratoconjunctivitis sicca associated with meibomian secretion polar lipid abnormality. Arch Ophthalmol 1998;116(7):849–852.
[166] Chen J, Green-Church KB, Nichols KK. Shotgun lipidomic analysis of human meibomian gland secretions with electrospray ionization tandem mass spectrometry. Invest Ophthalmol Vis Sci 2010;51(12):6220–6231.
[167] Butovich IA, Uchiyama E, Di Pascuale MA, McCulley JP. Liquid chromatography-mass spectrometric analysis of lipids present in human meibomian gland secretions. Lipids 2007;42(8):765–776.
[168] Butovich IA, Wojtowicz JC, Molai M. Human tear film and meibum. Very long chain wax esters and (O-acyl)-omega-hydroxy fatty acids of meibum. J Lipid Res 2009;50(12):2471–2485.
[169] Ham BM, Jacob JT, Cole RB. MALDI-TOF MS of phosphorylated lipids in biological fluids using immobilized metal affinity chromatography and a solid ionic crystal matrix. Anal Chem 2005;77(14):4439–4447.
[170] Saville JT, Zhao Z, Willcox MD, Ariyavidana MA, Blanksby SJ, Mitchell TW. Identification of phospholipids in human meibum by nano-electrospray ionisation tandem mass spectrometry. Exp Eye Res 2011;92(3):238–240.
[171] Ham BM, Jacob JT, Keese MM, Cole RB. Identification, quantification and comparison of major non-polar lipids in normal and dry eye tear lipidomes by electrospray tandem mass spectrometry. J Mass Spectrom 2004;39(11):1321–1336.
[172] Pucker AD, Haworth KM. The presence and significance of polar meibum and tear lipids. Ocul Surf 2015;13(1):26–42.
[173] Korb DR, Greiner JV, Glonek T. The effects of anionic and zwitterionic phospholipids on the tear film lipid layer. Adv Exp Med Biol 2002;506(Pt A):495–499.
[174] Korb D, Stone R. Are phospholipids the critical ingredient? Rev Cornea Contact Lens 2012;149:38–41.
[175] Nicolaides N. Recent findings on the chemical composition of steer and human meibomian glands. In: Holly F, editor. The Preocular Tear Film in Health, Disease, and Contact Lens Wear. Lubbock, TX: Dry Eye Institute; 1986. p. 570–576.
[176] McCulley JP, Shine W. A compositional based model for the tear film lipid layer. Trans Am Ophthalmol Soc 1997;95:79–88. discussion 88-93 discussion -93.
[177] Wang IJ, Lin IC, Hou YC, Hu FR. A comparison of the effect of carbomer-, cellulose- and mineral oil-based artificial tear formulations. Eur J Ophthalmol 2007 Mar-Apr;17(2):151–159.
[178] Craig JP, Purslow C, Murphy PJ, Wolffsohn JS. Effect of a liposomal spray on the pre-ocular tear film. Cont Lens Anter Eye 2010;33(2):83–87.
[179] Wang TJ, Wang IJ, Ho JD, Chou HC, Lin SY, Huang MC. Comparison of the clinical effects of carbomer-based lipid-containing gel and hydroxypropyl-guar gel artificial tear formulations in patients with dry eye syndrome: a 4-week, prospective, open-label, randomized, parallel-group, noninferiority study. Clin Ther 2010;32(1):44–52.
[180] Pult H, Gill F, Riede-Pult BH. Effect of three different liposomal eye sprays on ocular comfort and tear film. Cont Lens Anter Eye 2012;35. 203-7; quiz 43–4.
[181] Mutalib HA, Kaur S, Ghazali AR, Chinn Hooi N, Safie NH. A pilot study: the efficacy of virgin coconut oil as ocular rewetting agent on rabbit eyes. Evid Based Complement Altern Med 2015;2015:135987.
[182] Simmons PA, Carlisle-Wilcox C, Chen R, Liu H, Vehige JG. Efficacy, safety, and acceptability of a lipid-based artificial tear formulation: a randomized, controlled, multicenter clinical trial. Clin Ther 2015;37(4):858–868.
[183] Ralph RA, Doane MG, Dohlman CH. Clinical experience with a mobile ocular perfusion pump. Arch Ophthalmol 1975;93(10):1039–1043.
[184] Semeraro F, Forbice E, Braga O, Bova A, Di Salvatore A, Azzolini C. Evaluation of the efficacy of 50% autologous serum eye drops in different ocular surface pathologies. Biomed Res Int 2014;2014:826970.
[185] Tsubota K, Goto E, Fujita H, Ono M, Inoue H, Saito I, et al. Treatment of dry eye by autologous serum application in Sjögren's syndrome. Br J Ophthalmol 1999;83(4):390–395.
[186] Hwang J, Chung SH, Jeon S, Kwok SK, Park SH, Kim MS. Comparison of clinical efficacies of autologous serum eye drops in patients with primary and secondary Sjögren syndrome. Cornea 2014;33(7):663–667.
[187] Hondur AM, Akcam HT, Karaca EE, Yazici Eroglu H, Aydin B. Autologous serum eye drops accelerate epithelial healing after LASEK. Curr Eye Res 2016;41(1):15–19.
[188] Sagara H, Iida T, Saito K, Noji H, Ogasawara M, Oyamada H. Conservative treatment for late-onset bleb leaks after trabeculectomy with mitomycin C in patients with ocular surface disease. Clin Ophthalmol 2012;6:1273–1279.
[189] Ziakas NG, Boboridis KG, Terzidou C, Naoumidi TL, Mikropoulos D, Georgiadou EN, et al. Long-term follow up of autologous serum treatment for recurrent corneal erosions. Clin Exp Ophthalmol 2010;38(7):683–687.
[190] Geerling G, Daniels JT, Dart JK, Cree IA, Khaw PT. Toxicity of natural tear substitutes in a fully defined culture model of human corneal epithelial cells. Invest Ophthalmol Vis Sci 2001;42:948–956.
[191] Freire V, Andollo N, Etxebarria J, Hernáez-Moya R, Durán JA, Morales MC. Corneal wound healing promoted by 3 blood derivatives: an in vitro and in vivo comparative study. Cornea 2014;33(6):614–620.
[192] Akyol-Salman I. Effects of autologous serum eye drops on corneal wound healing after superficial keratectomy in rabbits. Cornea 2006;25(10):1178–1181.
[193] Hartwig D, Harloff S, Liu L, Schlenke P, Wedel T, Geerling G. Epitheliotrophic capacity of a growth factor preparation produced from platelet concentrates on corneal epithelial cells: a potential agent for the treatment of ocular surface defects? Transfusion 2004;44(12):1724–1731.
[194] Hartwig D, Herminghaus P, Wedel T, Liu L, Schlenke P, Dibbelt L, et al. Topical treatment of ocular surface defects: comparison of the epitheliotrophic capacity of fresh frozen plasma and serum on corneal epithelial cells in an in vitro cell culture model. Transfus Med 2005;15(2):107–113.
[195] Esquenazi S, He J, Bazan HE, Bazan NG. Use of autologous serum in corneal epithelial defects post-lamellar surgery. Cornea 2005;24(8):992–997.
[196] López-García JS, García-Lozano I, Rivas L, Giménez C, Acera A, Suárez-Cortés T. Effects of autologous serum eye drops on conjunctival expression of MUC5AC in patients with ocular surface disorders. Cornea 2016;35(3):336–341.
[197] Watson SL, Secker GA, Daniels JT. The effect of therapeutic human serum drops on corneal stromal wound-healing activity. Curr Eye Res 2008;33(8):641–652.
[198] Harloff S, Hartwig D, Kasper K, Wedel T, Muller M, Geerling G. Epitheliotrophic capacity of serum eye drops from healthy donors versus serum from immunosuppressed patients with rheumatoid arthritis. Klin Monbl Augenheilkd 2008;225:200–206.
[199] Maclennan S, Hartwig D, Geerling G. Experiences with a centralised national service for autologous serum eyedrops in England. Ophthalmologe 2008;105:639–643.
[200] Geerling G, Maclennan S, Hartwig D. Autologous serum eye drops for ocular surface disorders. Br J Ophthalmol 2004;88(11):1467–1474.
[201] Geerling G, Grus F, Seitz B, Hartwig D, Schirra F. Legal regulations to produce serum eye drops : when is it necessary, and how can it be obtained? Ophthalmologe 2008;105:632–638.
[202] Dietrich T, Weisbach V, Seitz B, Jacobi C, Kruse FE, Eckstein R, et al. Manufacture of autologous serum eye drops for out-patient therapy : cooperation between ophthalmic clinic and transfusion medicine department. Ophthalmologe 2008;105:1036–1038. 40-2.
[203] Herminghaus P, Geerling G, Hartwig D, Wedel T, Dibbelt L. Epitheliotrophic capacity of serum and plasma eyedrops. Influence of centrifugation. Ophthalmologe 2004;101:998–1005.
[204] Liu L, Hartwig D, Harloff S, Herminghaus P, Wedel T, Geerling G. An optimised protocol for the production of autologous serum eyedrops. Graefes Arch Clin Exp Ophthalmol 2005;243(7):706–714.
[205] Partal A, Scott E. Low-cost protocol for the production of autologous serum eye drops by blood collection and processing centres for the treatment of ocular surface diseases. Transfus Med 2011;21(4):271–277.
[206] Bradley JC, Simoni J, Bradley RH, McCartney DL, Brown SM. Time- and temperature-dependent stability of growth factor peptides in human autologous serum eye drops. Cornea 2009;28(2):200–205.
[207] Fischer KR, Opitz A, Böeck M, Geerling G. Stability of serum eye drops after storage of 6 months. Cornea 2012;31(11):1313–1318.
[208] López-García JS, García-Lozano I, Rivas L, Ramírez N, Méndez MT, Raposo R. Stability of growth factors in autologous serum eyedrops after long-term storage. Curr Eye Res 2016;41(3):292–298.
[209] Spaniol K, Koerschgen L, Sander O, Koegler G, Geerling G. Comparison of application systems for autologous serum eye drops. Curr Eye Res 2014;39(6):571–579.
[210] Kasper K, Godenschweger L, Hartwig D, Unterlauft JD, Seitz B, Geerling G. On the use of autologous serum eyedrops in Germany : results of a survey among members of the Cornea Section of the German Ophthalmological Society (DOG). Ophthalmologe 2008;105:644–649.
[211] Dalmon CA, Chandra NS, Jeng BH. Use of autologous serum eyedrops for the treatment of ocular surface disease: first US experience in a large population as an insurance-covered benefit. Arch Ophthalmol 2012;130:1612–1613.
[212] Mondy P, Brama T, Fisher J, Gemelli CN, Chee K, Keegan A, et al. Sustained benefits of autologous serum eye drops on self-reported ocular symptoms and vision-related quality of life in Australian patients with dry eye and corneal epithelial defects. Transfus Apher Sci 2015;53(3):404–411.
[213] Noble BA, Loh RS, MacLennan S, Pesudovs K, Reynolds A, Bridges LR, et al. Comparison of autologous serum eye drops with conventional therapy in a randomised controlled crossover trial for ocular surface disease. Br J Ophthalmol 2004;88:647–652.
[214] Kojima T, Ishida R, Dogru M, Goto E, Matsumoto Y, Kaido M, et al. The effect of autologous serum eyedrops in the treatment of severe dry eye disease: a prospective randomized case-control study. Am J Ophthalmol 2005;139(2):242–246.
[215] Noda-Tsuruya T, Asano-Kato N, Toda I, Tsubota K. Autologous serum eye drops for dry eye after LASIK. J Refract Surg 2006 Jan-Feb;22(1):61–66.
[216] Yoon KC, Heo H, Im SK, You IC, Kim YH, Park YG. Comparison of autologous serum and umbilical cord serum eye drops for dry eye syndrome. Am J Ophthalmol 2007;144(1):86–92.
[217] Urzua CA, Vasquez DH, Huidobro A, Hernandez H, Alfaro J. Randomized double-blind clinical trial of autologous serum versus artificial tears in dry eye syndrome. Curr Eye Res 2012;37(8):684–688.
[218] Celebi AR, Ulusoy C, Mirza GE. The efficacy of autologous serum eye drops for severe dry eye syndrome: a randomized double-blind crossover study. Graefes Arch Clin Exp Ophthalmol 2014;252(4):619–626.
[219] Hussain M, Shtein RM, Sugar A, Soong HK, Woodward MA, DeLoss K, et al. Long-term use of autologous serum 50% eye drops for the treatment of dry eye disease. Cornea 2014;33(12):1245–1251.
[220] Jirsova K, Brejchova K, Krabcova I, Filipec M, Al Fakih A, Palos M, et al. The application of autologous serum eye drops in severe dry eye patients; subjective and objective parameters before and after treatment. Curr Eye Res 2014;39(1):21–30.
[221] López-García JS, García-Lozano I, Rivas L, Ramírez N, Raposo R, Méndez MT. Autologous serum eye drops diluted with sodium hyaluronate: clinical and experimental comparative study. Acta Ophthalmol 2014;92(1):e22–e29.
[222] Aggarwal S, Kheirkhah A, Cavalcanti BM, Cruzat A, Colon C, Brown E, et al. Autologous serum tears for treatment of photoallodynia in patients with corneal neuropathy: efficacy and evaluation with in vivo confocal microscopy. Ocul Surf 2015;13(3):250–262.
[223] Li J, Zhang X, Zheng Q, Zhu Y, Wang H, Ma H, et al. Comparative evaluation of silicone hydrogel contact lenses and autologous serum for management of sjögren syndrome-associated dry eye. Cornea 2015;34(9):1072–1078.
[224] Mukhopadhyay S, Sen S, Datta H. Comparative role of 20% cord blood serum and 20% autologous serum in dry eye associated with Hansen's disease: a tear proteomic study. Br J Ophthalmol 2015;99(1):108–112.
[225] Turkoglu Elif, Celik Erkan, Alagoz Gursoy. A comparison of the efficacy of autologous serum eye drops with amniotic membrane transplantation in neurotrophic keratitis. Semin Ophthalmol 2014;29(3):119–126.
[226] Leite SC, de Castro RS, Alves M, Cunha DA, Correa ME, da Silveira LA, et al. Risk factors and characteristics of ocular complications, and efficacy of autologous serum tears after haematopoietic progenitor cell transplantation. Bone Marrow Transpl 2006;38(3):223–227.
[227] Thanathanee O, Phanphruk W, Anutarapongpan O, Romphruk A, Suwan-Apichon O. Contamination risk of 100% autologous serum eye drops in management of ocular surface diseases. Cornea 2013;32(8):1116–1119.
[228] Sanz-Marco E, Lopez-Prats MJ, Garcia-Delpech S, Udaondo P, Diaz-Llopis M. Fulminant bilateral Haemophilus influenzae keratitis in a patient with hypovitaminosis A treated with contaminated autologous serum. Clin Ophthalmol 2011;5:71–73.
[229] Petznick A, Tong L, Chung R, Wang JC, Koh M, Salleh R, et al. Autologous plasma eyedrops prepared in a closed system: a treatment for dry eye. Eye (Lond) 2013;27(9):1102.
[230] Chiang CC, Lin JM, Chen WL, Tsai YY. Allogeneic serum eye drops for the treatment of severe dry eye in patients with chronic graft-versus-host disease. Cornea 2007;26(7):861–863.
[231] Na KS, Kim MS. Allogeneic serum eye drops for the treatment of dry eye patients with chronic graft-versus-host disease. J Ocul Pharmacol Ther 2012;28(5):479–483.
[232] Harritshøj LH, Nielsen C, Ullum H, Hansen MB, Julian HO. Ready-made allogeneic ABO-specific serum eye drops: production from regular male blood donors, clinical routine, safety and efficacy. Acta Ophthalmol 2014;92(8):783–786.
[233] Badami KG, McKellar M. Allogeneic serum eye drops: time these became the norm? Br J Ophthalmol 2012;96(8):1151–1152.
[234] Yoon KC. Use of umbilical cord serum in ophthalmology. Chonnam Med J 2014;50(3):82–85.
[235] Yoon KC, Im SK, Park YG, Jung YD, Yang SY, Choi J. Application of umbilical cord serum eyedrops for the treatment of dry eye syndrome. Cornea 2006;25(3):268–272.
[236] Yoon KC, Jeong IY, Im SK, Park YG, Kim HJ, Choi J. Therapeutic effect of umbilical cord serum eyedrops for the treatment of dry eye associated with graft-versus-host disease. Bone Marrow Transpl 2007;39(4):231–235.
[237] Liu L, Hartwig D, Harloff S, Herminghaus P, Wedel T, Kasper K, et al. Corneal epitheliotrophic capacity of three different blood-derived preparations. Invest Ophthalmol Vis Sci 2006;47(6):2438–2444.
[238] Zallio F, Mazzucco L, Monaco F, Astori MR, Passera R, Drago G, et al. A single-center pilot prospective study of topical application of platelet-derived eye drops for patients with ocular chronic graft-versus-host disease. Biol Blood Marrow Transpl 2016;22(9):1664–1670.
[239] Fea AM, Aragno V, Testa V, Machetta F, Parisi S, D'Antico S, et al. The effect of autologous platelet lysate eye drops: an in vivo confocal microscopy study. Biomed Res Int 2016;2016:8406832.
[240] Riestra AC, Alonso-Herreros JM, Merayo-Lloves J. Arch Soc Esp Oftalmol 2016;91(10):475–490.
[241] Anitua E, Muruzabal F, de la Fuente M, Riestra A, Merayo-Lloves J, Orive G. PRGF exerts more potent proliferative and anti-inflammatory effects than autologous serum on a cell culture inflammatory model. Exp Eye Res 2016;151:115–121.
[242] Alio JL, Colecha JR, Pastor S, Rodriguez A, Artola A. Symptomatic dry eye treatment with autologous platelet-rich plasma. Ophthalmic Res 2007;39(3):124–129.
[243] López-Plandolit S, Morales MC, Freire V, Grau AE, Durán JA. Efficacy of plasma rich in growth factors for the treatment of dry eye. Cornea 2011;30(12):1312–1317.
[244] Pezzotta S, Del Fante C, Scudeller L, Cervio M, Antoniazzi ER, Perotti C. Autologous platelet lysate for treatment of refractory ocular GVHD. Bone Marrow Transpl 2012;47(12):1558–1563.
[245] Ichikawa Y, Tokunaga M, Shimizu H, Moriuchi J, Takaya M, Arimori S. Clinical trial of ambroxol (Mucosolvan) in Sjögren's syndrome. Tokai J Exp Clin Med 1988;13(3):165–169.
[246] Kerksick C, Willoughby D. The antioxidant role of glutathione and N-acetyl-cysteine supplements and exercise-induced oxidative stress. J Int Soc Sports Nutr 2005;2:38–44.
[247] Pokupec R, Petricek I, Sikic J, Bradic M, Popovic-Suic S, Petricek G. Comparison of local acetylcysteine and artificial tears in the management of dry eye syndrome. Acta Med Croat 2005;59:337–340.
[248] Albietz J, Sanfilippo P, Troutbeck R, Lenton LM. Management of filamentary keratitis associated with aqueous-deficient dry eye. Optom Vis Sci 2003;80(6):420–430.
[249] Pan Z, Wang Z, Yang H, Zhang F, Reinach PS. TRPV1 activation is required for hypertonicity-stimulated inflammatory cytokine release in human corneal epithelial cells. Invest Ophthalmol Vis Sci 2011;52(1):485–493.
[250] Mergler S, Garreis F, Sahlmüller M, Lyras EM, Reinach PS, Dwarakanath A, et al. Calcium regulation by thermo- and osmosensing transient receptor potential vanilloid channels (TRPVs) in human conjunctival epithelial cells. Histochem Cell Biol 2012;137(6):743–761.
[251] Benitez-Del-Castillo JM, Moreno-Montanes J, Jimenez-Alfaro I, Munoz-Negrete FJ, Turman K, Palumaa K, et al. Safety and efficacy clinical trials for SYL1001, a novel short interfering RNA for the treatment of dry eye disease. Invest Ophthalmol Vis Sci 2016;57:6447–6454.
[252] Kaido M, Ishida R, Dogru M, Tsubota K. Visual function changes after punctal occlusion with the treatment of short BUT type of dry eye. Cornea 2012;31(9):1009–1013.
[253] Chen F, Wang J, Chen W, Shen M, Xu S, Lu F. Upper punctal occlusion versus lower punctal occlusion in dry eye. Invest Ophthalmol Vis Sci 2010;51(11):5571–5577.
[254] Li M, Wang J, Shen M, Cui L, Tao A, Chen Z, et al. Effect of punctal occlusion on tear menisci in symptomatic contact lens wearers. Cornea 2012;31(9):1014–1022.
[255] Geldis JR, Nichols JJ. The impact of punctal occlusion on soft contact lens wearing comfort and the tear film. Eye Contact Lens 2008;34(5):261–265.
[256] Alfawaz AM, Algehedan S, Jastaneiah SS, Al-Mansouri S, Mousa A, Al-Assiri A. Efficacy of punctal occlusion in management of dry eyes after laser in situ keratomileusis for myopia. Curr Eye Res 2014;39(3):257–262.
[257] Yung YH, Toda I, Sakai C, Yoshida A, Tsubota K. Punctal plugs for treatment of post-LASIK dry eye. Jpn J Ophthalmol 2012;56(3):208–213.
[258] Ambrósio Jr. R, Tervo T, Wilson SE. LASIK-associated dry eye and neurotrophic epitheliopathy: pathophysiology and strategies for prevention and treatment. J Refract Surg 2008;24(4):396–407.
[259] Yaguchi S, Ogawa Y, Kamoi M, Uchino M, Tatematsu Y, Ban Y, et al. Surgical management of lacrimal punctal cauterization in chronic GVHD-related dry eye with recurrent punctal plug extrusion. Bone Marrow Transpl 2012;47(11):1465–1469.
[260] Sabti S, Halter JP, Braun Fränkl BC, Goldblum D. Punctal occlusion is safe and efficient for the treatment of keratoconjunctivitis sicca in patients with ocular GvHD. Bone Marrow Transpl 2012;47(7):981–984.
[261] Yang HY, Fujishima H, Toda I, Shimazaki J, Tsubota K. Lacrimal punctal occlusion for the treatment of superior limbic keratoconjunctivitis. Am J Ophthalmol 1997;124(1):80–87.
[262] Tai MC, Cosar CB, Cohen EJ, Rapuano CJ, Laibson PR. The clinical efficacy of silicone punctal plug therapy. Cornea 2002;21(2):135–139.
[263] Tong L, Beuerman R, Simonyi S, Hollander DA, Stern ME. Effects of punctal occlusion on clinical signs and symptoms and on tear cytokine levels in patients with dry eye. Ocul Surf 2016;14(2):233–241.
[264] Goto E, Yagi Y, Kaido M, Matsumoto Y, Konomi K, Tsubota K. Improved functional visual acuity after punctal occlusion in dry eye patients. Am J Ophthalmol 2003;135(5):704–705.
[265] Kimura K, Yokoi N, Inagaki K, Komuro A, Sonomura Y, Kato H, et al. Treatment progress of large-size puncta and clinical investigation of the extrusion rate and other complications associated with large-size punctal plugs. Nippon Ganka Gakkai Zasshi 2014;118:490–494.
[266] Schaumberg DA, Uchino M, Christen WG, Semba RD, Buring JE, Li JZ. Patient reported differences in dry eye disease between men and women: impact, management, and patient satisfaction. PLoS One 2013;8:e76121.
[267] Yokoi N, Komuro A. Non-invasive methods of assessing the tear film. Exp Eye Res 2004;78(3):399–407.
[268] Chen F, Shen M, Chen W, Wang J, Li M, Yuan Y, et al. Tear meniscus volume in dry eye after punctal occlusion. Invest Ophthalmol Vis Sci 2010;51(4):1965–1969.
[269] Foulks GN, Forstot SL, Donshik PC, Forstot JZ, Goldstein MH, Lemp MA, et al. Clinical guidelines for management of dry eye associated with Sjögren disease. Ocul Surf 2015;13(2):118–132.
[270] Hirai K, Takano Y, Uchio E, Kadonosono K. Clinical evaluation of the therapeutic effects of atelocollagen absorbable punctal plugs. Clin Ophthalmol 2012;6:133–138.
[271] Hamano T. Atelocollagen punctal occlusion for the treatment of the dry eye. Adv Exp Med Biol 2002;506(Pt B):1283–1284.
[272] Miyata K, Otani S, Miyai T, Nejima R, Amano S. Atelocollagen punctal occlusion in dry eye patients. Cornea 2006;25(1):47–50.
[273] Hadassah J, Bhuvaneshwari N, Singh D, Sehgal PK. Preparation and clinical evaluation of succinylated collagen punctal plugs in dry eye syndrome: a pilot study. Ophthalmic Res 2010;43(4):185–192.
[274] Capita L, Chalita MR, dos Santos-Neto LL. Prospective evaluation of hypromellose 2% for punctal occlusion in patients with dry eye. Cornea 2015;34(2):188–192.
[275] Mazow ML, McCall T, Prager TC. Lodged intracanalicular plugs as a cause of lacrimal obstruction. Ophthal Plast Reconstr Surg 2007 Mar-Apr;23(2):138–142.
[276] ClinicalTrialsWebsite. Tolerability, Safety and Efficacy of Lubricin (150 μg/ml) Eye Drops Versus Sodium Hyaluronate (HA) 0.18% Eye Drops in Patients With Moderate Dry Eye (DE). https://clinicaltrials.gov/ct2/show/NCT02507934?term=lubricin&rank=22015.
[277] Egrilmez S, Aslan F, Karabulut G, Kabasakal Y, Yagci A. Clinical efficacy of the SmartPlug™ in the treatment of primary Sjogren's syndrome with keratoconjunctivitis sicca: one-year follow-up study. Rheumatol Int 2011;31(12):1567–1570.
[278] SmartPlug Study G. Management of complications after insertion of the SmartPlug punctal plug: a study of 28 patients. Ophthalmology 2006;113(1859):e1–e6.
[279] Rabensteiner DF, Boldin I, Klein A, Horwath-Winter J. Collared silicone punctal plugs compared to intracanalicular plugs for the treatment of dry eye. Curr Eye Res 2013;38(5):521–525.
[280] Joganathan V, Mehta P, Murray A, Durrani OM. Complications of intracanalicular plugs: a case series. Orbit 2010;29(5):271–273.
[281] Murube J, Murube E. Treatment of dry eye by blocking the lacrimal canaliculi. Surv Ophthalmol 1996 May-Jun;40(6):463–480.
[282] Patten JT. Punctal occlusion with n-butyl cyanoacrylate tissue adhesive. Ophthalmic Surg 1976;7(2):24–26.
[283] Balaram M, Schaumberg DA, Dana MR. Efficacy and tolerability outcomes after punctal occlusion with silicone plugs in dry eye syndrome. Am J Ophthalmol 2001;131(1):30–36.
[284] Nishii M, Yokoi N, Komuro A, Kinoshita S. Clinical investigation of extrusion of a new punctal plug(Flex Plug). Nippon Ganka Gakkai Zasshi 2004;108:139–143.
[285] Nishii M, Yokoi N, Komuro A, Sugita J, Nakamura Y, Kojima K, et al. Comparison of extrusion rate for two different design of punctal plugs. Nippon Ganka Gakkai Zasshi 2003;107:322–325.
[286] Sonomura Y, Yokoi N, Komuro A, Inagaki K, Kinoshita S. Clinical investigation of the extrusion rate and other complications of the SuperEagle plug. Nippon Ganka Gakkai Zasshi 2013;117:126–131.
[287] Horwath-Winter J, Thaci A, Gruber A, Boldin I. Long-term retention rates and complications of silicone punctal plugs in dry eye. Am J Ophthalmol 2007;144(3):441–444.
[288] Kaido M, Ishida R, Dogru M, Tsubota K. Comparison of retention rates and complications of 2 different types of silicon lacrimal punctal plugs in the treatment of dry eye disease. Am J Ophthalmol 2013;155:648–653. 53 e1.
[289] Sakamoto A, Kitagawa K, Tatami A. Efficacy and retention rate of two types of silicone punctal plugs in patients with and without Sjögren syndrome. Cornea 2004;23(3):249–254.
[290] Rumelt S, Remulla H, Rubin PA. Silicone punctal plug migration resulting in dacryocystitis and canaliculitis. Cornea 1997;16(3):377–379.
[291] Scheepers M, Pearson A, Michaelides M. Bilateral canaliculitis following SmartPLUG insertion for dry eye syndrome post LASIK surgery. Graefes Arch Clin Exp Ophthalmol 2007;245(6):895–897.
[292] Yokoi N, Okada K, Sugita J, Kinoshita S. Acute conjunctivitis associated with biofilm formation on a punctal plug. Jpn J Ophthalmol 2000 Sep-Oct;44(5):559–560.
[293] Ahn HB, Seo JW, Roh MS, Jeong WJ, Park WC, Rho SH. Canaliculitis with a papilloma-like mass caused by a temporary punctal plug. Ophthal Plast Reconstr Surg 2009 Sep-Oct;25(5):413–414.
[294] Bourkiza R, Lee V. A review of the complications of lacrimal occlusion with punctal and canalicular plugs. Orbit 2012;31(2):86–93.
[295] Dohlman CH. Punctal occlusion in keratoconjunctivitis sicca. Ophthalmology 1978;85(12):1277–1281.
[296] Geerling G, Tost FH. Surgical occlusion of the lacrimal drainage system. Dev Ophthalmol 2008;41:213–229.
[297] Ohba E, Dogru M, Hosaka E, Yamazaki A, Asaga R, Tatematsu Y, et al. Surgical punctal occlusion with a high heat-energy releasing cautery device for severe dry eye with recurrent punctal plug extrusion. Am J Ophthalmol 2011;151(3):483–487. e1.
[298] Holzchuh R, Villa Albers MB, Osaki TH, Igami TZ, Santo RM, Kara-Jose N, et al. Two-year outcome of partial lacrimal punctal occlusion in the management of dry eye related to Sjögren syndrome. Curr Eye Res 2011;36(6):507–512.
[299] Yazici B, Bilge AD, Naqadan F. Lacrimal Punctal Occlusion With Conjunctival Flap. Ophthal Plast Reconstr Surg 2015 Jul-Aug;31(4):300–302.
[300] Panagopoulos A, Chalioulias K, Ramsay AS. 'Punctal switch' grafting for the treatment of dry eyes: our experience. Ophthalmic Res 2011;46(4):218–220.
[301] Obata H, Ibaraki N, Tsuru T. A technique for preventing spontaneous loss of lacrimal punctal plugs. Am J Ophthalmol 2006;141(3):567–569.
[302] Putterman AM. Canaliculectomy in the treatment of keratitis sicca. Ophthalmic Surg 1991;22(8):478–480.
[303] DeMartelaere SL, Blaydon SM, Tovilla-Canales JL, Shore JW. A permanent and reversible procedure to block tear drainage for the treatment of dry eye. Ophthal Plast Reconstr Surg 2006 Sep-Oct;22(5):352–355.
[304] Kaido M, Goto E, Dogru M, Tsubota K. Punctal occlusion in the management of chronic Stevens-Johnson syndrome. Ophthalmology 2004;111(5):895–900.
[305] Knapp ME, Frueh BR, Nelson CC, Musch DC. A comparison of two methods of punctal occlusion. Am J Ophthalmol 1989;108(3):315–318.
[306] Roberts CW, Carniglia PE, Brazzo BG. Comparison of topical cyclosporine, punctal occlusion, and a combination for the treatment of dry eye. Cornea 2007;26(7):805–809.
[307] Ervin AM, Wojciechowski R, Schein O. Punctal occlusion for dry eye syndrome. Cochrane Database Syst Rev 2010;(9):CD006775.
[308] Kojima K, Yokoi N, Nakamura Y, Takada Y, Sato H, Komuro A, et al. Outcome of punctal plug occlusion therapy for severe dry eye syndrome. Nippon Ganka Gakkai Zasshi 2002;106:360–364.
[309] Nava-Castaneda A, Tovilla-Canales JL, Rodriguez L, Tovilla Y Pomar JL, Jones CE. Effects of lacrimal occlusion with collagen and silicone plugs on patients with conjunctivitis associated with dry eye. Cornea 2003;22(1):10–14.
[310] Farrell J, Patel S, Grierson DG, Sturrock RD. A clinical procedure to predict the value of temporary occlusion therapy in keratoconjunctivitis sicca. Ophthalmic Physiol Opt 2003;23(1):1–8.
[311] Altan-Yaycioglu R, Gencoglu EA, Akova YA, Dursun D, Cengiz F, Akman A. Silicone versus collagen plugs for treating dry eye: results of a prospective randomized trial including lacrimal scintigraphy. Am J Ophthalmol 2005;140(1):88–93.
[312] Chen SX, Lee GA. SmartPlug in the management of severe dry eye syndrome. Cornea 2007;26(5):534–538.
[313] Shi S, Chen W, Zhang X, Ma HX, Sun L. Effects of silicone punctal plugs for tear deficiency dry eye patients. Zhonghua Yan Ke Za Zhi 2013;49:151–154.
[314] Savar DE. A new approach to ocular moisture chambers. J Pediatr Ophthalmol Strabismus 1978 Jan-Feb;15(1):51–53.
[315] Gresset J, Simonet P, Gordon D. Combination of a side shield with an ocular moisture chamber. Am J Optom Physiol Opt 1984;61(9):610–612.
[316] Shen G, Qi Q, Ma X. Effect of Moisture Chamber Spectacles on Tear Functions in Dry Eye Disease. Optom Vis Sci 2016;93(2):158–164.
[317] Craig J, Chan E, Ea L, Kam C, Lu Y, Misra S. Dry eye relief for VDU users from a USB-desktop humidifier. Contact Lens Anter Eye 2012;35:28. e-abstract.
[318] Shigeyasu C, Hirano S, Akune Y, Yamada M. Diquafosol Tetrasodium Increases the Concentration of Mucin-like Substances in Tears of Healthy Human Subjects. Curr Eye Res 2015;40(9):878–883.
[319] Fujihara T, Murakami T, Nagano T, Nakamura M, Nakata K. INS365 suppresses loss of corneal epithelial integrity by secretion of mucin-like glycoprotein in a rabbit short-term dry eye model. J Ocul Pharmacol Ther 2002;18(4):363–370.
[320] Lau OC, Samarawickrama C, Skalicky SE. P2Y2 receptor agonists for the treatment of dry eye disease: a review. Clin Ophthalmol 2014;8:327–334.
[321] Gong L, Sun X, Ma Z, Wang Q, Xu X, Chen X, et al. A randomised, parallel-group comparison study of diquafosol ophthalmic solution in patients with dry eye in China and Singapore. Br J Ophthalmol 2015;99(7):903–908.
[322] Bremond-Gignac D, Gicquel JJ, Chiambaretta F. Pharmacokinetic evaluation of diquafosol tetrasodium for the treatment of Sjögren's syndrome. Expert Opin Drug Metab Toxicol 2014;10(6):905–913.
[323] Koh S, Ikeda C, Takai Y, Watanabe H, Maeda N, Nishida K. Long-term results of treatment with diquafosol ophthalmic solution for aqueous-deficient dry eye. Jpn J Ophthalmol 2013;57(5):440–446.
[324] Shimazaki-Den S, Iseda H, Dogru M, Shimazaki J. Effects of diquafosol sodium eye drops on tear film stability in short BUT type of dry eye. Cornea 2013;32(8):1120–1125.
[325] Yamaguchi M, Nishijima T, Shimazaki J, Takamura E, Yokoi N, Watanabe H, et al. Real-world assessment of diquafosol in dry eye patients with risk factors such as contact lens, meibomian gland dysfunction, and conjunctivochalasis: subgroup analysis from a prospective observational study. Clin Ophthalmol 2015;9:2251–2256.
[326] Mori Y, Nejima R, Masuda A, Maruyama Y, Minami K, Miyata K, et al. Effect of diquafosol tetrasodium eye drop for persistent dry eye after laser in situ keratomileusis. Cornea 2014;33(7):659–662.
[327] Park DH, Chung JK, Seo du R, Lee SJ. Clinical Effects and Safety of 3% Diquafosol Ophthalmic Solution for Patients With Dry Eye After Cataract Surgery: A Randomized Controlled Trial. Am J Ophthalmol 2016;163:122–131. e2.
[328] Byun YS, Yoo YS, Kwon JY, Joo JS, Lim SA, Whang WJ, et al. Diquafosol promotes corneal epithelial healing via intracellular calcium-mediated ERK activation. Exp Eye Res 2016;143:89–97.
[329] Chao W, Belmonte C, Benitez Del Castillo JM, Bron AJ, Dua HS, Nichols KK, et al. Report of the Inaugural Meeting of the TFOS i(2) = initiating innovation Series: Targeting the Unmet Need for Dry Eye Treatment. Ocul Surf 2016;14(2):264–316.
[330] Samudre S, Lattanzio Jr. FA, Lossen V, Hosseini A, Sheppard Jr. JD, McKown RL, et al. Lacritin, a novel human tear glycoprotein, promotes sustained basal tearing and is well tolerated. Invest Ophthalmol Vis Sci 2011;52(9):6265–6270.
[331] Vijmasi T, Chen FY, Balasubbu S, Gallup M, McKown RL, Laurie GW, et al. Topical administration of lacritin is a novel therapy for aqueous-deficient dry eye disease. Invest Ophthalmol Vis Sci 2014;55(8):5401–5409.
[332] Itoh S, Itoh K, Shinohara H. Regulation of human corneal epithelial mucins by rebamipide. Curr Eye Res 2014;39(2):133–141.
[333] Kinoshita S, Awamura S, Nakamichi N, Suzuki H, Oshiden K, Yokoi N, et al. A multicenter, open-label, 52-week study of 2% rebamipide (OPC-12759) ophthalmic suspension in patients with dry eye. Am J Ophthalmol 2014;157(3):576–583. e1.
[334] Koh S, Inoue Y, Sugmimoto T, Maeda N, Nishida K. Effect of rebamipide ophthalmic suspension on optical quality in the short break-up time type of dry eye. Cornea 2013;32(9):1219–1223.
[335] Itakura H, Kashima T, Itakura M, Akiyama H, Kishi S. Topical rebamipide improves lid wiper epitheliopathy. Clin Ophthalmol 2013;7:2137–2141.
[336] Sasaki H, Kokubun T. Alkali burn treated with 2% rebamipide ophthalmic suspension: a case report. Case Rep Ophthalmol 2014 Sep-Dec;5(3):380–385.
[337] Kashima T, Itakura H, Akiyama H, Kishi S. Rebamipide ophthalmic suspension for the treatment of dry eye syndrome: a critical appraisal. Clin Ophthalmol 2014;8:1003–1010.
[338] Igarashi A, Kamiya K, Kobashi H, Shimizu K. Effect of Rebamipide Ophthalmic Suspension on Intraocular Light Scattering for Dry Eye After Corneal Refractive Surgery. Cornea 2015;34(8):895–900.
[339] Uchino Y, Mauris J, Woodward AM, Dieckow J, Amparo F, Dana R, et al. Alteration of galectin-3 in tears of patients with dry eye disease. Am J Ophthalmol 2015;159(6):1027–1035. e3.
[340] Nakamura T, Hata Y, Nagata M, Yokoi N, Yamaguchi S, Kaku T, et al. JBP485 promotes tear and mucin secretion in ocular surface epithelia. Sci Rep 2015;5:10248.
[341] He H, Ding H, Liao A, Liu Q, Yang J, Zhong X. Effects of mycophenolate mofetil on proliferation and mucin-5AC expression in human conjunctival goblet cells in vitro. Mol Vis 2010;16:1913–1919.
[342] Yang YM, Park S, Ji H, Kim TI, Kim EK, Kang KK, et al. DA-6034 Induces [Ca(2+)]i Increase in Epithelial Cells. Korean J Physiol Pharmacol 2014;18:89–94.
[343] Choi SM, Seo MJ, Lee YG, Lee MJ, Jeon HJ, Kang KK, et al. Effects of DA-6034, a flavonoid derivative, on mucin-like glycoprotein and ocular surface integrity in a rabbit model. Arzneimittelforschung 2009;59(10):498–503.
[344] Schulze U, Sel S, Paulsen FP. Trefoil factor family peptide 3 at the ocular surface. A promising therapeutic candidate for patients with dry eye syndrome? Dev Ophthalmol 2010;45:1–11.
[345] Schulze U, Hampel U, Sel S, Contreras-Ruiz L, Schicht M, Dieckow J, et al. Trefoil factor family peptide 3 (TFF3) is upregulated under experimental conditions similar to dry eye disease and supports corneal wound healing effects in vitro. Invest Ophthalmol Vis Sci 2014;55(5):3037–3042.
[346] Lambiase A, Micera A, Pellegrini G, Merlo D, Rama P, De Luca M, et al. In vitro evidence of nerve growth factor effects on human conjunctival epithelial cell differentiation and mucin gene expression. Invest Ophthalmol Vis Sci 2009;50(10):4622–4630.
[347] Ding J, Sullivan DA. The effects of insulin-like growth factor 1 and growth hormone on human meibomian gland epithelial cells. JAMA Ophthalmol 2014;132(5):593–599.
[348] Schirra F, Suzuki T, Richards SM, Jensen RV, Liu M, Lombardi MJ, et al. Androgen control of gene expression in the mouse meibomian gland. Invest Ophthalmol Vis Sci 2005;46(10):3666–3675.
[349] Schirra F, Richards SM, Liu M, Suzuki T, Yamagami H, Sullivan DA. Androgen regulation of lipogenic pathways in the mouse meibomian gland. Exp Eye Res 2006;83(2):291–296.
[350] Sullivan DA, Jensen RV, Suzuki T, Richards SM. Do sex steroids exert sex-specific and/or opposite effects on gene expression in lacrimal and meibomian glands? Mol Vis 2009;15:1553–1572.
[351] Khandelwal P, Liu S, Sullivan DA. Androgen regulation of gene expression in human meibomian gland and conjunctival epithelial cells. Mol Vis 2012;18:1055–1067.
[352] Schiffman R, Bradford R, Bunnell B, Lai F, Bernstein P, Whitcup S. A multi-center, double-masked, randomized, vehicle-controlled, parallel group study to evaluate the safety and efficacy of testosterone ophthalmic solution in patients with meibomian gland dysfunction. Invest Ophthalmol Vis Sci 2006;47. ARVO e-abstract #5608.
[353] Sullivan DA, Rocha EM, Aragona P, Clayton JA, Ding J, Golebiowski B, et al. TFOS DEWS II Sex, Gender, and Hormones report. Ocul Surf 2017;15:284–333.
[354] Tsifetaki N, Kitsos G, Paschides CA, Alamanos Y, Eftaxias V, Voulgari PV, et al. Oral pilocarpine for the treatment of ocular symptoms in patients with Sjögren's syndrome: a randomised 12 week controlled study. Ann Rheum Dis 2003;62(12):1204–1207.
[355] Kawakita T, Shimmura S, Tsubota K. Effect of Oral Pilocarpine in Treating Severe Dry Eye in Patients With Sjögren Syndrome. Asia Pac J Ophthalmol Phila 2015 Mar-Apr;4(2):101–105.
[356] Aragona P, Di Pietro R, Spinella R, Mobrici M. Conjunctival epithelium improvement after systemic pilocarpine in patients with Sjogren's syndrome. Br J Ophthalmol 2006;90(2):166–170.
[357] Ibrahim OM, Dogru M, Kawashima S, Wakamatsu TH, Tsubota K, Fujishima H. Visante optical coherence tomography and tear function test evaluation of cholinergic treatment response in patients with sjögren syndrome. Cornea 2013;32(5):653–657.
[358] Noaiseh G, Baker JF, Vivino FB. Comparison of the discontinuation rates and side-effect profiles of pilocarpine and cevimeline for xerostomia in primary Sjögren's syndrome. Clin Exp Rheumatol 2014 Jul-Aug;32(4):575–577.
[359] Petrone D, Condemi JJ, Fife R, Gluck O, Cohen S, Dalgin P. A double-blind, randomized, placebo-controlled study of cevimeline in Sjögren's syndrome patients with xerostomia and keratoconjunctivitis sicca. Arthritis Rheum 2002;46(3):748–754.
[360] Ono M, Takamura E, Shinozaki K, Tsumura T, Hamano T, Yagi Y, et al. Therapeutic effect of cevimeline on dry eye in patients with Sjögren's syndrome: a randomized, double-blind clinical study. Am J Ophthalmol 2004;138(1):6–17.
[361] Ramos-Casals M, Tzioufas AG, Stone JH, Siso A, Bosch X. Treatment of primary Sjogren syndrome: a systematic review. JAMA 2010;304:452–460.
[362] Akpek EK, Lindsley KB, Adyanthaya RS, Swamy R, Baer AN, McDonnell PJ. Treatment of Sjögren's syndrome-associated dry eye an evidence-based review. Ophthalmology 2011;118(7):1242–1252.
[363] Kossler AL, Wang J, Feuer W, Tse DT. Neurostimulation of the lacrimal nerve for enhanced tear production. Ophthal Plast Reconstr Surg 2015 Mar-Apr;31(2):145–151.
[364] Famm K, Litt B, Tracey KJ, Boyden ES, Slaoui M. Drug discovery: a jump-start for electroceuticals. Nature 2013;496(7444):159–161.
[365] Hydén D, Arlinger S. On the sneeze-reflex and its control. Rhinology 2007;45(3):218–219.
[366] Gumus K, Pflugfelder SC. Intranasal Tear Neurostimulation: An Emerging Concept in the Treatment of Dry Eye. Int Ophthalmol Clin 2017;57(2):101–108.
[367] Baroody FM. How nasal function influences the eyes, ears, sinuses, and lungs. Proc Am Thorac Soc 2011;8(1):53–61.
[368] Gupta A, Heigle T, Pflugfelder SC. Nasolacrimal stimulation of aqueous tear production. Cornea 1997;16(6):645–648.
[369] Friedman NJ, Butron K, Robledo N, Loudin J, Baba SN, Chayet A. A nonrandomized, open-label study to evaluate the effect of nasal stimulation on tear production in subjects with dry eye disease. Clin Ophthalmol 2016;10:795–804.
[370] Gumus K, Schuetzle KL, Pflugfelder SC. Randomized Controlled Crossover Trial Comparing the Impact of Sham or Intranasal Tear Neurostimulation on Conjunctival Goblet Cell Degranulation. Am J Ophthalmol 2017;177:159–168.
[371] Craig JP, Cohn G, Corbett D, Tenen A, Coroneo M, McAlister J, et al. Evaluating the Safety and Efficacy of Intranasal Neurostimulation for Dry Eye Disease: A Double-masked, Randomized, Controlled, Multicenter Study. Optom Vis Sci 2016;94:160041. E-abstract.
[372] Craig JP, Friedman N, Torkildsen G, Ackermann M. Symptom Reduction with Oculeve Intranasal Stimulator on Exposure to Environmental Challenge in Dry Eye: A Randomized, Controlled, Crossover Trial. Optom Vis Sci 2016;94:160057. E-abstract.
[373] Sano K, Kawashima M, Ikeura K, Arita R, Tsubota K. Abdominal breathing increases tear secretion in healthy women. Ocul Surf 2015;13(1):82–87.
[374] Hirata H, Meng ID. Cold-sensitive corneal afferents respond to a variety of ocular stimuli central to tear production: implications for dry eye disease. Invest Ophthalmol Vis Sci 2010;51(8):3969–3976.
[375] Belmonte C, Gallar J. Cold thermoreceptors, unexpected players in tear production and ocular dryness sensations. Invest Ophthalmol Vis Sci 2011;52(6):3888–3892.
[376] Nilius B, Voets T. Neurophysiology: channelling cold reception. Nature 2007;448(7150):147–148.
[377] Kovács I, Luna C, Quirce S, Mizerska K, Callejo G, Riestra A, et al. Abnormal activity of corneal cold thermoreceptors underlies the unpleasant sensations in dry eye disease. Pain 2016;157(2):399–417.
[378] Osei KA, Ovenseri-Ogbomo G, Kyei S, Ntodie M. The effect of caffeine on tear secretion. Optom Vis Sci 2014;91(2):171–177.
[379] Bron AJ, Benjamin L, Bilaniuk LT. Meibomian gland disease. Classification and grading of lid changes. Eye 1991;5(4):395–411.
[380] Green-Church KB, Butovich I, Willcox M, Borchman D, Paulsen F, Barabino S, et al. The international workshop on meibomian gland dysfunction: report of the subcommittee on tear film lipids and lipid-protein interactions in health and disease. Invest Ophthalmol Vis Sci 2011;52(4):1979–1993.
[381] McCulley JP, Dougherty JM, Deneau DG. Classification of chronic blepharitis. Ophthalmology 1982;89(10):1173–1180.
[382] McCulley JP, Shine WE. Changing concepts in the diagnosis and management of blepharitis. Cornea 2000;19(5):650–658.
[383] Nichols KK. The international workshop on meibomian gland dysfunction: introduction. Invest Ophthalmol Vis Sci 2011;52(4):1917–1921.
[384] Nichols KK, Foulks GN, Bron AJ, Glasgow BJ, Dogru M, Tsubota K, et al. The international workshop on meibomian gland dysfunction: executive summary. Invest Ophthalmol Vis Sci 2011;52(4):1922–1929.
[385] Smith RE, Flowers Jr. CW. Chronic blepharitis: a review. CLAO J 1995;21(3):200–207.
[386] Key JE. A comparative study of eyelid cleaning regimens in chronic blepharitis. CLAO J 1996;22(3):209–212.
[387] Romero JM, Biser SA, Perry HD, Levinson DH, Doshi SJ, Terraciano A, et al. Conservative treatment of meibomian gland dysfunction. Eye Contact Lens 2004;30(1):14–19.
[388] Craig JP, Sung J, Wang MT, Cheung I, Sherwin T, Ismail S. Commercial lid cleanser outperforms baby shampoo for management of blepharitis in randomized, double-masked clinical trial. Invest Ophthalmol Vis Sci 2017;58. E-abstract 2247–B0014.
[389] Geerling G, Tauber J, Baudouin C, Goto E, Matsumoto Y, O'Brien T, et al. The international workshop on meibomian gland dysfunction: report of the subcommittee on management and treatment of meibomian gland dysfunction. Invest Ophthalmol Vis Sci 2011;52(4):2050–2064.
[390] Alghamdi YA, Camp A, Feuer W, Karp CL, Wellik S, Galor A. Compliance and Subjective Patient Responses to Eyelid Hygiene. Eye Contact Lens 2017. In press.
[391] Coroneo MT, Rosenberg ML, Cheung LM. Ocular effects of cosmetic products and procedures. Ocul Surf 2006;4(2):94–102.
[392] Goto T, Zheng X, Gibbon L, Ohashi Y. Cosmetic product migration onto the ocular surface: exacerbation of migration after eyedrop instillation. Cornea 2010;29(4):400–403.
[393] Ng A, Evans K, North RV, Purslow C. Migration of Cosmetic Products into the Tear Film. Eye Contact Lens 2015;41(5):304–309.
[394] Paugh JR, Knapp LL, Martinson JR, Hom MM. Meibomian therapy in problematic contact lens wear. Optom Vis Sci 1990;67(11):803–806.
[395] Guillon M, Maissa C, Wong S. Eyelid margin modification associated with eyelid hygiene in anterior blepharitis and meibomian gland dysfunction. Eye Contact Lens 2012;38(5):319–325.
[396] Guillon M, Maissa C, Wong S. Symptomatic relief associated with eyelid hygiene in anterior blepharitis and MGD. Eye Contact Lens 2012;38(5):306–312.
[397] Doan S. Tolerability and acceptability of Blephagel: a novel eyelid hygiene aqueous gel. Clin Ophthalmol 2012;6:71–77.
[398] Khaireddin R, Hueber A. Eyelid hygiene for contact lens wearers with blepharitis. Comparative investigation of treatment with baby shampoo versus phospholipid solution. Ophthalmologe 2013;110:146–153.
[399] Arrúa M, Samudio M, Fariña N, Cibils D, Laspina F, Sanabria R, et al. Comparative study of the efficacy of different treatment options in patients with chronic blepharitis. Arch Soc Esp Oftalmol 2015;90(3):112–118.
[400] Ngo W, Srinivasan S, Houtman D, Jones L. The relief of dry eye signs and symptoms using a combination of lubricants, lid hygiene and ocular nutraceuticals. J Optom 2017;10(1):26–33.
[401] Benitez-Del-Castillo JM. How to promote and preserve eyelid health. Clin Ophthalmol 2012;6:1689–1698.
[402] Needle JJ, Petchey R, Lawrenson JG. A survey of the scope of therapeutic practice by UK optometrists and their attitudes to an extended prescribing role. Ophthalmic Physiol Opt 2008;28(3):193–203.
[403] Jackson WB. Management of dysfunctional tear syndrome: a Canadian consensus. Can J Ophthalmol 2009;44(4):385–394.
[404] Zhao YE, Wu LP, Hu L, Xu JR. Association of blepharitis with Demodex: a meta-analysis. Ophthalmic Epidemiol 2012;19(2):95–102.
[405] Junk AK, Lukacs A, Kampik A. Topical administration of metronidazole gel as an effective therapy alternative in chronic Demodex blepharitis–a case report. Klin Monbl Augenheilkd 1998;213:48–50.
[406] Czepita D, Kuzna-Grygiel W, Czepita M, Grobelny A. Demodex folliculorum and Demodex brevis as a cause of chronic marginal blepharitis. Ann Acad Med Stetin 2007;53:63–67. discussion 7.
[407] Fulk GW, Clifford C. A case report of demodicosis. J Am Optom Assoc 1990;61(8):637–639.
[408] Fulk GW, Murphy B, Robins MD. Pilocarpine gel for the treatment of demodicosis-a case series. Optom Vis Sci 1996;73(12):742–745.
[409] Kheirkhah A, Casas V, Li W, Raju VK, Tseng SC. Corneal manifestations of ocular demodex infestation. Am J Ophthalmol 2007;143(5):743–749.
[410] Gao YY, Di Pascuale MA, Elizondo A, Tseng SC. Clinical treatment of ocular demodecosis by lid scrub with tea tree oil. Cornea 2007;26(2):136–143.
[411] Holzchuh FG, Hida RY, Moscovici BK, Villa Albers MB, Santo RM, Kara-José N, et al. Clinical treatment of ocular Demodex folliculorum by systemic ivermectin. Am J Ophthalmol 2011;151(6):1030–1034. e1.
[412] Filho PA, Hazarbassanov RM, Grisolia AB, Pazos HB, Kaiserman I, Gomes JÁ. The efficacy of oral ivermectin for the treatment of chronic blepharitis in patients tested positive for Demodex spp. Br J Ophthalmol 2011;95(6):893–895.
[413] Koo H, Kim TH, Kim KW, Wee SW, Chun YS, Kim JC. Ocular surface discomfort and Demodex: effect of tea tree oil eyelid scrub in Demodex blepharitis. J Korean Med Sci 2012;27(12):1574–1579.
[414] Gao YY, Xu DL, Huang lJ, Wang R, Tseng SC. Treatment of ocular itching associated with ocular demodicosis by 5% tea tree oil ointment. Cornea 2012;31(1):14–17.
[415] Salem DA, El-Shazly A, Nabih N, El-Bayoumy Y, Saleh S. Evaluation of the efficacy of oral ivermectin in comparison with ivermectin-metronidazole combined therapy in the treatment of ocular and skin lesions of Demodex folliculorum. Int J Infect Dis 2013;17(5):e343–e347.
[416] Carson CF, Hammer KA, Riley TV. Melaleuca alternifolia (Tea Tree) oil: a review of antimicrobial and other medicinal properties. Clin Microbiol Rev 2006;19(1):50–62.
[417] Gao YY, Di Pascuale MA, Li W, Baradaran-Rafii A, Elizondo A, Kuo CL, et al. In vitro and in vivo killing of ocular Demodex by tea tree oil. Br J Ophthalmol 2005;89(11):1468–1473.
[418] Tighe S, Gao YY, Tseng SC. Terpinen-4-ol is the Most Active Ingredient of Tea Tree Oil to Kill Demodex Mites. Transl Vis Sci Technol 2013;2(7):2.
[419] Cheng AM, Sheha H, Tseng SC. Recent advances on ocular Demodex infestation. Curr Opin Ophthalmol 2015;26(4):295–300.
[420] Nicholls SG, Oakley CL, Tan A, Vote BJ. Demodex treatment in external ocular disease: the outcomes of a Tasmanian case series. Int Ophthalmol 2016;36(5):691–696.
[421] Forstinger C, Kittler H, Binder M. Treatment of rosacea-like demodicidosis with oral ivermectin and topical permethrin cream. J Am Acad Dermatol 1999;41(5 Pt 1):775–777.
[422] McCann LC, Tomlinson A, Pearce EI, Papa V. Effectiveness of artificial tears in the management of evaporative dry eye. Cornea 2012;31(1):1–5.
[423] Sindt CW, Foulks GN. Efficacy of an artificial tear emulsion in patients with dry eye associated with meibomian gland dysfunction. Clin Ophthalmol 2013;7:1713–1722.
[424] Aguilar AJ, Marquez MI, Albera PA, Tredicce JL, Berra A. Effects of Systane(®) Balance on noninvasive tear film break-up time in patients with lipid-deficient dry eye. Clin Ophthalmol 2014;8:2365–2372.
[425] Kaercher T, Thelen U, Brief G, Morgan-Warren RJ, Leaback R. A prospective, multicenter, noninterventional study of Optive Plus(®) in the treatment of patients with dry eye: the prolipid study. Clin Ophthalmol 2014;8:1147–1155.
[426] Guthrie SE, Jones L, Blackie CA, Korb DR. A Comparative Study Between an Oil-in-Water Emulsion and Nonlipid Eye Drops Used for Rewetting Contact Lenses. Eye Contact Lens 2015;41(6):373–377.
[427] Ousler 3rd G, Devries DK, Karpecki PM, Ciolino JB. An evaluation of Retaine™ ophthalmic emulsion in the management of tear film stability and ocular surface staining in patients diagnosed with dry eye. Clin Ophthalmol 2015;9:235–243.
[428] Gan L, Wang J, Jiang M, Bartlett H, Ouyang D, Eperjesi F, et al. Recent advances in topical ophthalmic drug delivery with lipid-based nanocarriers. Drug Discov Today 2013;18(5–6):290–297.
[429] Sim HS, Petznick A, Barbier S, Tan JH, Acharya UR, Yeo S, et al. A Randomized, Controlled Treatment Trial of Eyelid-Warming Therapies in Meibomian Gland Dysfunction. Ophthalmol Ther 2014;3(1–2):37–48.
[430] Villani Edoardo, Garoli Elena, Canton Veronica, Pichi Francesco, Nucci Paolo, Ratiglia Roberto. Evaluation of a novel eyelid-warming device in meibomian gland dysfunction unresponsive to traditional warm compress treatment: an in vivo confocal study. Int Ophthalmol 2015;35(3):319–323.
[431] Lacroix Z, Léger S, Bitton E. Ex vivo heat retention of different eyelid warming masks. Cont Lens Anter Eye 2015;38(3):152–156.
[432] Bitton E, Lacroix Z, Léger S. In-vivo heat retention comparison of eyelid warming masks. Cont Lens Anter Eye 2016;39(4):311–315.
[433] Murakami DK, Blackie CA, Korb DR. All Warm Compresses Are Not Equally Efficacious. Optom Vis Sci 2015;92(9):e327–e333.
[434] Bron AJ, Tiffany JM. The contribution of meibomian disease to dry eye. Ocul Surf 2004;2(2):149–165.
[435] Nichols KK, Ham BM, Nichols JJ, Ziegler C, Green-Church KB. Identification of fatty acids and fatty acid amides in human meibomian gland secretions. Invest Ophthalmol Vis Sci 2007;48(1):34–39.
[436] Olson MC, Korb DR, Greiner JV. Increase in tear film lipid layer thickness following treatment with warm compresses in patients with meibomian gland dysfunction. Eye Contact Lens 2003;29(2):96–99.
[437] Blackie CA, Korb DR, Knop E, Bedi R, Knop N, Holland EJ. Nonobvious obstructive meibomian gland dysfunction. Cornea 2010;29(12):1333–1345.
[438] Goto E, Endo K, Suzuki A, Fujikura Y, Tsubota K. Improvement of tear stability following warm compression in patients with meibomian gland dysfunction. Adv Exp Med Biol 2002;506(Pt B):1149–1152.
[439] Tiffany JM. The lipid secretion of the meibomian glands. Adv Lipid Res 1987;22:1–62.
[440] Ong BL, Larke JR. Meibomian gland dysfunction: some clinical, biochemical and physical observations. Ophthalmic Physiol Opt 1990;10(2):144–148.
[441] Korb DR, Blackie CA. Meibomian gland diagnostic expressibility: correlation with dry eye symptoms and gland location. Cornea 2008;27(10):1142–1147.
[442] Arita R, Morishige N, Shirakawa R, Sato Y, Amano S. Effects of Eyelid Warming Devices on Tear Film Parameters in Normal Subjects and Patients with Meibomian Gland Dysfunction. Ocul Surf 2015;13(4):321–330.
[443] Blackie CA, Solomon JD, Greiner JV, Holmes M, Korb DR. Inner eyelid surface temperature as a function of warm compress methodology. Optom Vis Sci 2008;85(8):675–683.
[444] Chang CM, Chu HT, Wei YH, Chen FP, Wang S, Wu PC, et al. The Core Pattern Analysis on Chinese Herbal Medicine for Sjögren's syndrome: A Nationwide Population-Based Study. Sci Rep 2015;5:9541.
[445] Despa F, Orgill DP, Neuwalder J, Lee RC. The relative thermal stability of tissue macromolecules and cellular structure in burn injury. Burns 2005;31(5):568–577.
[446] Moritz AR, Henriques FC. Studies of Thermal Injury: II. The Relative Importance of Time and Surface Temperature in the Causation of Cutaneous Burns. Am J Pathol 1947;23(5):695–720.
[447] Plaghki L, Decruynaere C, Van Dooren P, Le Bars D. The fine tuning of pain thresholds: a sophisticated double alarm system. PLoS One 2010;5:e10269.
[448] Blackie CA, McMonnies CW, Korb DR. Warm compresses and the risks of elevated corneal temperature with massage. Cornea 2013;32(7):e146–e149.
[449] Solomon JD, Case CL, Greiner JV, Blackie CA, Herman JP, Korb DR. Warm compress induced visual degradation and Fischer-Schweitzer polygonal reflex. Optom Vis Sci 2007;84(7):580–587.
[450] McMonnies CW, Korb DR, Blackie CA. The role of heat in rubbing and massage-related corneal deformation. Cont Lens Anter Eye 2012;35(4):148–154.
[451] Man Lam S, Tong L, Duan X, Acharya UR, Tan JH, Petznick A, Wenk MR, Shui G, et al. J Lipid Res 2014;55(9):1959–1969.
[452] Pearce EI, Archer CV, McWilliams MA, Tomlinson A, Fuller JR. Effects of novel eye warming goggles on the tear film. Invest Ophthalmol Vis Sci 2006;47:5601.
[453] Pult H, Riede-Pult BH, Purslow C. A comparison of an eyelid-warming device to traditional compress therapy. Optom Vis Sci 2012;89(7):E1035–E1041.
[454] Doan S, Chiambaretta F, Baudouin C, ESPOIR study group. Evaluation of an eyelid warming device (Blephasteam) for the management of ocular surface diseases in France: the ESPOIR study. J Fr Ophtalmol 2014;37(10):763–772.
[455] Wang MT, Gokul A, Craig JP. Temperature profiles of patient-applied eyelid warming therapies. Cont Lens Anter Eye 2015;38(6):430–434.
[456] Bilkhu PS, Naroo SA, Wolffsohn JS. Randomised masked clinical trial of the MGDRx EyeBag for the treatment of meibomian gland dysfunction-related evaporative dry eye. Br J Ophthalmol 2014;98(12):1707–1711.
[457] Wang MT, Jaitley Z, Lord SM, Craig JP. Comparison of Self-applied Heat Therapy for Meibomian Gland Dysfunction. Optom Vis Sci 2015;92(9):e321–e326.
[458] Goto E, Monden Y, Takano Y, Mori A, Shimmura S, Shimazaki J, et al. Treatment of non-inflamed obstructive meibomian gland dysfunction by an infrared warm compression device. Br J Ophthalmol 2002;86(12):1403–1407.
[459] Lane SS, DuBiner HB, Epstein RJ, Ernest PH, Greiner JV, Hardten DR, et al. A new system, the LipiFlow, for the treatment of meibomian gland dysfunction. Cornea 2012;31(4):396–404.
[460] Hom MM, Silverman MW. Displacement technique and meibomian gland expression. J Am Optom Assoc 1987;58(3):223–226.
[461] Korb DR, Greiner JV. Increase in tear film lipid layer thickness following treatment of meibomian gland dysfunction. Adv Exp Med Biol 1994;350:293–298.
[462] McCulley JP, Sciallis GF. Meibomian keratoconjunctivitis. Am J Ophthalmol 1977;84(6):788–793.
[463] Korb DR, Henriquez AS. Meibomian gland dysfunction and contact lens intolerance. J Am Optom Assoc 1980;51(3):243–251.
[464] Korb DR, Blackie CA. Meibomian gland therapeutic expression: quantifying the applied pressure and the limitation of resulting pain. Eye Contact Lens 2011;37(5):298–301.
[465] Blackie CA, Carlson AN, Korb DR. Treatment for meibomian gland dysfunction and dry eye symptoms with a single-dose vectored thermal pulsation: a review. Curr Opin Ophthalmol 2015;26(4):306–313.
[466] Finis D, König C, Hayajneh J, Borrelli M, Schrader S, Geerling G. Six-month effects of a thermodynamic treatment for MGD and implications of meibomian gland atrophy. Cornea 2014;33(12):1265–1270.
[467] Blackie CA, Coleman CA, Holland EJ. The sustained effect (12 months) of a single-dose vectored thermal pulsation procedure for meibomian gland dysfunction and evaporative dry eye. Clin Ophthalmol 2016;10:1385–1396.
[468] Greiner JV. Long-Term (3 Year) Effects of a Single Thermal Pulsation System Treatment on Meibomian Gland Function and Dry Eye Symptoms. Eye Contact Lens 2016;42(2):99–107.
[469] Goldberg DJ. Current trends in intense pulsed light. J Clin Aesthet Dermatol 2012;5(6):45–53.
[470] Craig JP, Chen YH, Turnbull PR. Prospective trial of intense pulsed light for the treatment of meibomian gland dysfunction. Invest Ophthalmol Vis Sci 2015;56(3):1965–1970.
[471] Vegunta S, Patel D, Shen JF. Combination Therapy of Intense Pulsed Light Therapy and Meibomian Gland Expression (IPL/MGX) Can Improve Dry Eye Symptoms and Meibomian Gland Function in Patients With Refractory Dry Eye: A Retrospective Analysis. Cornea 2016;35(3):318–322.
[472] Gupta PK, Vora GK, Matossian C, Kim M, Stinnett S. Outcomes of intense pulsed light therapy for treatment of evaporative dry eye disease. Can J Ophthalmol 2016;51(4):249–253.
[473] Maskin SL. Intraductal meibomian gland probing relieves symptoms of obstructive meibomian gland dysfunction. Cornea 2010;29(10):1145–1152.
[474] Fermon S, Hindi Zaga I, Alvarez Melloni D. Intraductal meibomian gland probing for the treatment of blepharitis. Arch Soc Esp Oftalmol 2015;90(2):76–80.
[475] Nakayama N, Kawashima M, Kaido M, Arita R, Tsubota K. Analysis of Meibum Before and After Intraductal Meibomian Gland Probing in Eyes With Obstructive Meibomian Gland Dysfunction. Cornea 2015;34(10):1206–1208.
[476] Wladis EJ. Intraductal meibomian gland probing in the management of ocular rosacea. Ophthal Plast Reconstr Surg 2012 Nov-Dec;28(6):416–418.
[477] Knop E, Knop N, Millar T, Obata H, Sullivan DA. The international workshop on meibomian gland dysfunction: report of the subcommittee on anatomy, physiology, and pathophysiology of the meibomian gland. Invest Ophthalmol Vis Sci 2011;52(4):1938–1978.
[478] Korb DR, Blackie CA. Debridement-scaling: a new procedure that increases Meibomian gland function and reduces dry eye symptoms. Cornea 2013;32(12):1554–1557.
[479] Ngo W, Caffery B, Srinivasan S, Jones LW. Effect of Lid Debridement-Scaling in Sjögren Syndrome Dry Eye. Optom Vis Sci 2015;92(9):e316–e320.
[480] McMonnies CW. Incomplete blinking: exposure keratopathy, lid wiper epitheliopathy, dry eye, refractive surgery, and dry contact lenses. Cont Lens Anter Eye 2007;30(1):37–51.
[481] Pereira MV, Glória AL. Semin Ophthalmol 2010;25(3):72–78.
[482] Zeev MS, Miller DD, Latkany R. Diagnosis of dry eye disease and emerging technologies. Clin Ophthalmol 2014;8:581–590.
[483] Bron AJ, de Paiva CS, Chauhan SK, Bonini S, Gabison EE, Jain S, et al. TFOS DEWS II Pathophysiology report. Ocul Surf 2017;15:438–510.
[484] Katz J, Kaufman HE. Corneal exposure during sleep (nocturnal lagophthalmos). Arch Ophthalmol 1977;95(3):449–453.
[485] Sohrab M, Abugo U, Grant M, Merbs S. Management of the eye in facial paralysis. Facial Plast Surg 2015;31(2):140–144.
[486] Vásquez LM, Medel R. Lagophthalmos after facial palsy: current therapeutic options. Ophthalmic Res 2014;52(4):165–169.
[487] Latkany RL, Lock B, Speaker M. Nocturnal lagophthalmos: an overview and classification. Ocul Surf 2006;4(1):44–53.
[488] So HM, Lee CC, Leung AK, Lim JM, Chan CS, Yan WW. Comparing the effectiveness of polyethylene covers (Gladwrap) with lanolin (Duratears) eye ointment to prevent corneal abrasions in critically ill patients: a randomized controlled study. Int J Nurs Stud 2008;45(11):1565–1571.
[489] Koroloff N, Boots R, Lipman J, Thomas P, Rickard C, Coyer F. A randomised controlled study of the efficacy of hypromellose and Lacri-Lube combination versus polyethylene/Cling wrap to prevent corneal epithelial breakdown in the semiconscious intensive care patient. Intensive Care Med 2004;30(6):1122–1126.
[490] Kartush JM, Linstrom CJ, McCann PM, Graham MD. Early gold weight eyelid implantation for facial paralysis. Otolaryngol Head Neck Surg 1990;103(6):1016–1023.
[491] Linder T, Linstrom C, Robert Y. Rehabilitation of the eye in patients with facial paralyses: indications and results of gold weight implantation. Klin Monbl Augenheilkd 1997;210:293–295.
[492] Lucena A, Akaishi PM, Rodrigues Mde L, Cruz AA. Upper eyelid entropion and dry eye in cicatricial trachoma without trichiasis. Arq Bras Oftalmol 2012 Nov-Dec;75(6):420–422.
[493] Geerling G, Borrelli M. Adnexal surgery for severe ocular surface disease. Semin Ophthalmol 2005 Apr-Jun;20(2):101–112.
[494] Hintschich C. Correction of entropion and ectropion. Dev Ophthalmol 2008;41:85–102.
[495] Ross AH, Cannon PS, Selva D, Malhotra R. Management of upper eyelid cicatricial entropion. Clin Exp Ophthalmol 2011;39(6):526–536.
[496] Al-Amry MA. Ocular manifestation of Ichthyosis. Saudi J Ophthalmol 2016 Jan-Mar;30(1):39–43.
[497] Damasceno RW, Avgitidou G, Belfort Jr. R, Dantas PE, Holbach LM, Heindl LM. Eyelid aging: pathophysiology and clinical management. Arq Bras Oftalmol 2015 Sep-Oct;78(5):328–331.
[498] Monga P, Gupta VP, Dhaliwal U. Clinical evaluation of changes in cornea and tear film after surgery for trachomatous upper lid entropion. Eye (Lond) 2008;22(7):912–917.
[499] Cosar CB, Cohen EJ, Rapuano CJ, Maus M, Penne RP, Flanagan JC, et al. Tarsorrhaphy: clinical experience from a cornea practice. Cornea 2001;20(8):787–791.
[500] Papas EB, Ciolino JB, Jacobs D, Miller WL, Miller WS, Pult H, et al. The TFOS International Workshop on Contact Lens Discomfort: report of the management and therapy subcommittee. Invest Ophthalmol Vis Sci 2013;54(11):TFOS183–TFOS203.
[501] Koh S, Maeda N, Soma T, Hori Y, Tsujikawa M, Watanabe H, et al. Development of Methicillin-Resistant Staphylococcus aureus Keratitis in a Dry Eye Patient With a Therapeutic Contact Lens. Eye Contact Lens Sci Clin Pract 2012;38(3):200–202.
[502] Henry CR, Flynn Jr. HW, Miller D, Forster RK, Alfonso EC. Infectious keratitis progressing to endophthalmitis: a 15-year study of microbiology, associated factors, and clinical outcomes. Ophthalmology 2012;119(12):2443–2449.
[503] Stapleton F, Keay L, Edwards K, Naduvilath T, Dart JK, Brian G, et al. The incidence of contact lens-related microbial keratitis in Australia. Ophthalmology 2008;115(10):1655–1662.
[504] Dart JK, Radford CF, Minassian D, Verma S, Stapleton F. Ophthalmology 2008;115(10):1647–1654. 1654e1-3.
[505] Schein OD, Glynn RJ, Poggio EC, Seddon JM, Kenyon KR. The relative risk of ulcerative keratitis among users of daily-wear and extended-wear soft contact lenses. A case-control study. Microbial Keratitis Study Group. N Engl J Med 1989;321(12):773–778.
[506] Stapleton F, Dart JK, Minassian D. Risk factors with contact lens related suppurative keratitis. CLAO J 1993;19(4):204–210.
[507] Foulks GN, Harvey T, Raj CV. Therapeutic contact lenses: the role of high-Dk lenses. Ophthalmol Clin North Am 2003;16(3):455–461.
[508] Ahad MA, Anandan M, Tah V, Dhingra S, Leyland M. Randomized Controlled Study of Ocular Lubrication Versus Bandage Contact Lens in the Primary Treatment of Recurrent Corneal Erosion Syndrome. Cornea 2013;32(10):1311–1314.
[509] Wipperman JL, Dorsch JN. Evaluation and management of corneal abrasions. Am Fam Physician 2013;87(2):114–120.
[510] Siu GD, Young AL, Jhanji V. Alternatives to corneal transplantation for the management of bullous keratopathy. Curr Opin Ophthalmol 2014;25(4):347–352.
[511] Grentzelos MA, Plainis S, Astyrakakis NI, Diakonis VF, Kymionis GD, Kallinikos P, et al. Efficacy of 2 types of silicone hydrogel bandage contact lenses after photorefractive keratectomy. J Cataract Refract Surg 2009;35(12):2103–2108.
[512] Chen D, Lian Y, Li J, Ma Y, Shen M, Lu F. Monitor corneal epithelial healing under bandage contact lens using ultrahigh-resolution optical coherence tomography after pterygium surgery. Eye Contact Lens 2014;40(3):175–180.
[513] Daglioglu MC, Coskun M, Ilhan N, Tuzcu EA, Ilhan O, Keskin U, et al. The effects of soft contact lens use on cornea and patient's recovery after autograft pterygium surgery. Cont Lens Anter Eye 2014;37(3):175–177.
[514] Mohammadpour M, Amouzegar A, Hashemi H, Jabbarvand M, Kordbacheh H, Rahimi F, et al. Comparison of Lotrafilcon B and Balafilcon A silicone hydrogel bandage contact lenses in reducing pain and discomfort after photorefractive keratectomy: A contralateral eye study. Cont Lens Anter Eye 2015;38(3):211–214.
[515] Russo PA, Bouchard CS, Galasso JM. Extended-wear silicone hydrogel soft contact lenses in the management of moderate to severe dry eye signs and symptoms secondary to graft-versus-host disease. Eye Contact Lens 2007;33(3):144–147.
[516] Goyal S, Hamrah P. Understanding Neuropathic Corneal Pain–Gaps and Current Therapeutic Approaches. Semin Ophthalmol 2016;31:59–70.
[517] Galor A, Levitt RC, Felix ER, Martin ER, Sarantopoulos CD. Neuropathic ocular pain: an important yet underevaluated feature of dry eye. Eye (Lond) 2015;29(3):301–312.
[518] Smiddy WE, Hamburg TR, Kracher GP, Gottsch JD, Stark WJ. Therapeutic contact lenses. Ophthalmology 1990;97(3):291–295.
[519] Lim L, Tan DT, Chan WK. Therapeutic use of Bausch & Lomb PureVision contact lenses. CLAO J 2001;27(4):179–185.
[520] Jacobs DS, Rosenthal P. Boston scleral lens prosthetic device for treatment of severe dry eye in chronic graft-versus-host disease. Cornea 2007;26(10):1195–1199.
[521] Schornack MM, Baratz KH, Patel SV, Maguire LJ. Jupiter scleral lenses in the management of chronic graft versus host disease. Eye Contact Lens 2008;34(6):302–305.
[522] Takahide K, Parker PM, Wu M, Hwang WY, Carpenter PA, Moravec C, et al. Use of fluid-ventilated, gas-permeable scleral lens for management of severe keratoconjunctivitis sicca secondary to chronic graft-versus-host disease. Biol Blood Marrow Transpl 2007;13(9):1016–1021.
[523] Tougeron-Brousseau B, Delcampe A, Gueudry J, Vera L, Doan S, Hoang-Xuan T, et al. Vision-Related Function After Scleral Lens Fitting in Ocular Complications of Stevens-Johnson Syndrome and Toxic Epidermal Necrolysis. Am J Ophthalmol 2009;148(6):852–859.
[524] Schein OD, Rosenthal P, Ducharme C. A gas-permeable scleral contact lens for visual rehabilitation. Am J Ophthalmol 1990;109(3):318–322.
[525] Kok JH, Visser R. Treatment of ocular surface disorders and dry eyes with high gas-permeable scleral lenses. Cornea 1992;11(6):518–522.
[526] Tan DT, Pullum KW, Buckley RJ. Medical applications of scleral contact lenses: 1. A retrospective analysis of 343 cases. Cornea 1995;14(2):121–129.
[527] Weyns M, Koppen C, Tassignon MJ. Scleral contact lenses as an alternative to tarsorrhaphy for the long-term management of combined exposure and neurotrophic keratopathy. Cornea 2013;32(3):359–361.
[528] Jacobs DS. Update on scleral lenses. Curr Opin Ophthalmol 2008;19(4):298–301.
[529] Schornack MM. Scleral lenses: a literature review. Eye Contact Lens 2015;41(1):3–11.
[530] van der Worp E, Bornman D, Ferreira DL, Faria-Ribeiro M, Garcia-Porta N, González-Meijome JM. Modern scleral contact lenses: A review. Cont Lens Anter Eye 2014;37(4):240–250.
[531] Heur M, Bach D, Theophanous C, Chiu GB. Prosthetic Replacement of the Ocular Surface Ecosystem Scleral Lens Therapy for Patients With Ocular Symptoms of Chronic Stevens-Johnson Syndrome. Am J Ophthalmol 2014;158(1):49–54.
[532] Papakostas TD, Le HG, Chodosh J, Jacobs DS. Prosthetic Replacement of the Ocular Surface Ecosystem as Treatment for Ocular Surface Disease in Patients with a History of Stevens–Johnson Syndrome/Toxic Epidermal Necrolysis. Ophthalmology 2015;122(2):248–253.
[533] Bavinger JC, DeLoss K, Mian SI. Scleral lens use in dry eye syndrome. Curr Opin Ophthalmol 2015;26(4):319–324.
[534] Sonsino J, Mathe DS. Central vault in dry eye patients successfully wearing scleral lens. Optom Vis Sci 2013;90. e248–51; discussion 1030.
[535] Fernandes M, Sharma S. Polymicrobial and microsporidial keratitis in a patient using Boston scleral contact lens for Sjogren's syndrome and ocular cicatricial pemphigoid. Contact Lens Anter Eye 2013;36(2):95–97.
[536] Alipour F, Kheirkhah A, Jabarvand Behrouz M. Use of mini scleral contact lenses in moderate to severe dry eye. Cont Lens Anter Eye 2012;35(6):272–276.
[537] Grey F, Carley F, Biswas S, Tromans C. Scleral contact lens management of bilateral exposure and neurotrophic keratopathy. Cont Lens Anter Eye 2012;35(6):288–291.
[538] Wang Y, Kornberg DL, St Clair RM, Lee M, Muhic I, Ciralsky JB, et al. Corneal nerve structure and function after long-term wear of fluid-filled scleral lens. Cornea 2015;34(4):427–432.
[539] Belmonte C, Nichols JJ, Cox SM, Brock JA, Begley CG, Bereiter DA, et al. TFOS DEWS II Pain and Sensation report. Ocul Surf 2017;15:404–437.
[540] Coronel MF, Labombarda F, González SL. Neuroactive steroids, nociception and neuropathic pain: A flashback to go forward. Steroids 2016;110:77–87.
[541] De Paiva CS, Corrales RM, Villarreal AL, Farley W, Li DQ, Stern ME, et al. Apical corneal barrier disruption in experimental murine dry eye is abrogated by methylprednisolone and doxycycline. Invest Ophthalmol Vis Sci 2006;47(7):2847–2856.
[542] De Paiva CS, Corrales RM, Villarreal AL, Farley WJ, Li DQ, Stern ME, et al. Corticosteroid and doxycycline suppress MMP-9 and inflammatory cytokine expression, MAPK activation in the corneal epithelium in experimental dry eye. Exp Eye Res 2006;83(3):526–535.
[543] Lekhanont K, Leyngold IM, Suwan-Apichon O, Rangsin R, Chuck RS. Comparison of topical dry eye medications for the treatment of keratoconjunctivitis sicca in a botulinum toxin B-induced mouse model. Cornea 2007;26(1):84–89.
[544] Okanobo A, Chauhan SK, Dastjerdi MH, Kodati S, Dana R. Efficacy of topical blockade of interleukin-1 in experimental dry eye disease. Am J Ophthalmol 2012;154(1):63–71.
[545] Shafiee A, Bucolo C, Budzynski E, Ward KW, López FJ. In vivo ocular efficacy profile of mapracorat, a novel selective glucocorticoid receptor agonist, in rabbit models of ocular disease. Invest Ophthalmol Vis Sci 2011;52(3):1422–1430.
[546] Ji YW, Seo Y, Choi W, Yeo A, Noh H, Kim EK, et al. Dry eye-induced CCR7+CD11b+ cell lymph node homing is induced by COX-2 activities. Invest Ophthalmol Vis Sci 2014;55(10):6829–6838.
[547] Marsh P, Pflugfelder SC. Topical nonpreserved methylprednisolone therapy for keratoconjunctivitis sicca in Sjögren syndrome. Ophthalmology 1999;106(4):811–816.
[548] Sainz De La Maza Serra M, Simon Castellvi C, Kabbani O. Nonpreserved topical steroids and lacrimal punctal occlusion for severe keratoconjunctivitis sicca. Arch Soc Esp Oftalmol 2000;75:751–756.
[549] Avunduk AM, Avunduk MC, Varnell ED, Kaufman HE. The comparison of efficacies of topical corticosteroids and nonsteroidal anti-inflammatory drops on dry eye patients: a clinical and immunocytochemical study. Am J Ophthalmol 2003;136(4):593–602.
[550] Pflugfelder SC, Maskin SL, Anderson B, Chodosh J, Holland EJ, De Paiva CS, et al. A randomized, double-masked, placebo-controlled, multicenter comparison of loteprednol etabonate ophthalmic suspension, 0.5%, and placebo for treatment of keratoconjunctivitis sicca in patients with delayed tear clearance. Am J Ophthalmol 2004;138:444–457.
[551] Lee HK, Ryu IH, Seo KY, Hong S, Kim HC, Kim EK. Topical 0.1% prednisolone lowers nerve growth factor expression in keratoconjunctivitis sicca patients. Ophthalmology 2006;113:198–205.
[552] Yang CQ, Sun W, Gu YS. A clinical study of the efficacy of topical corticosteroids on dry eye. J Zhejiang Univ Sci B 2006;7(8):675–678.
[553] Jonisch J, Steiner A, Udell IJ. Preservative-free low-dose dexamethasone for the treatment of chronic ocular surface disease refractory to standard therapy. Cornea 2010;29(7):723–726.
[554] Sheppard JD, Donnenfeld ED, Holland EJ, Slonim CB, Solomon R, Solomon KD, et al. Effect of loteprednol etabonate 0.5% on initiation of dry eye treatment with topical cyclosporine 0.05%. Eye Contact Lens 2014;40(5):289–296.
[555] Kheirkhah A, Dohlman TH, Amparo F, Arnoldner MA, Jamali A, Hamrah P, et al. Effects of corneal nerve density on the response to treatment in dry eye disease. Ophthalmology 2015;122(4):662–668.
[556] Lin T, Gong L. Topical fluorometholone treatment for ocular dryness in patients with Sjogren syndrome: a randomized clinical trial in China. Med Baltim 2015;94:e551.
[557] Pinto-Fraga José, López-Miguel Alberto, González-García María J, Fernández Itziar, López-de-la-Rosa Alberto, Enríquez-de-Salamanca Amalia, et al. Topical Fluorometholone Protects the Ocular Surface of Dry Eye Patients from Desiccating Stress. Ophthalmology 2016;123(1):141–153.
[558] Villani E, Garoli E, Termine V, Pichi F, Ratiglia R, Nucci P. Corneal Confocal Microscopy in Dry Eye Treated with Corticosteroids. Optom Vis Sci 2015;92(9):e290–e295.
[559] Hong S, Kim T, Chung SH, Kim EK, Seo KY. Recurrence after topical nonpreserved methylprednisolone therapy for keratoconjunctivitis sicca in Sjögren's syndrome. J Ocul Pharmacol Ther 2007;23(1):78–82.
[560] McGhee CN, Dean S, Danesh-Meyer H. Locally administered ocular corticosteroids: benefits and risks. Drug Saf 2002;25(1):33–55.
[561] LeHoang P. The gold standard of noninfectious uveitis: corticosteroids. Dev Ophthalmol 2012;51:7–28.
[562] Mataftsi A, Narang A, Moore W, Nischal KK. Do reducing regimens of fluorometholone for paediatric ocular surface disease cause glaucoma? Br J Ophthalmol 2011;95(11):1531–1533.
[563] Bilgihan K, Gürelik G, Akata F, Hasanreisoglu B. Fluorometholone-induced cataract after photorefractive keratectomy. Ophthalmologica 1997;211(6):394–396.
[564] Sheppard JD, Comstock TL, Cavet ME. Impact of the Topical Ophthalmic Corticosteroid Loteprednol Etabonate on Intraocular Pressure. Adv Ther 2016;33(4):532–552.
[565] Byun YJ, Kim TI, Kwon SM, Seo KY, Kim SW, Kim EK, et al. Efficacy of combined 0.05% cyclosporine and 1% methylprednisolone treatment for chronic dry eye. Cornea 2012;31(5):509–513.
[566] Chen W, Li Z, Hu J, Zhang Z, Chen L, Chen Y, et al. Corneal alternations induced by topical application of benzalkonium chloride in rabbit. PLoS One 2011;6:e26103.
[567] Kim YH, Jung JC, Jung SY, Yu S, Lee KW, Park YJ. Comparison of the Efficacy of Fluorometholone With and Without Benzalkonium Chloride in Ocular Surface Disease. Cornea 2016;35(2):234–242.
[568] Barbarino JM, Staatz CE, Venkataramanan R, Klein TE, Altman RB. PharmGKB summary: cyclosporine and tacrolimus pathways. Pharmacogenet Genomics 2013;23(10):563–585.
[569] Donnenfeld E, Pflugfelder SC. Topical ophthalmic cyclosporine: pharmacology and clinical uses. Surv Ophthalmol 2009 May-Jun;54(3):321–338.
[570] Matsuda S, Koyasu S. Mechanisms of action of cyclosporine. Immunopharmacology 2000;47(2–3):119–125.
[571] Haddad EM, McAlister VC, Renouf E, Malthaner R, Kjaer MS, Gluud LL. Cyclosporin versus tacrolimus for liver transplanted patients. Cochrane Database Syst Rev 2006;(4):CD005161.
[572] Gorantla VS, Barker JH, Jones Jr. JW, Prabhune K, Maldonado C, Granger DK. Immunosuppressive agents in transplantation: mechanisms of action and current anti-rejection strategies. Microsurgery 2000;20(8):420–429.
[573] Kumar NS, Khosla R, Makharia GK. Cyclosporine in steroid refractory acute severe colitis. Trop Gastroenterol 2014;35(Suppl 1):S21–S28.
[574] Gremese E, Ferraccioli GF. Benefit/risk of cyclosporine in rheumatoid arthritis. Clin Exp Rheumatol 2004 Sep-Oct;22(5 Suppl 35):S101–S107.
[575] Utine CA, Stern M, Akpek EK. Clinical review: topical ophthalmic use of cyclosporin A. Ocul Immunol Inflamm 2010;18(5):352–361.
[576] Keklikci U, Dursun B, Cingu AK. Topical cyclosporine a 0.05% eyedrops in the treatment of vernal keratoconjunctivitis - randomized placebo-controlled trial. Adv Clin Exp Med 2014;23:455–461.
[577] Gonzalez-Lopez JJ, Lopez-Alcalde J, Morcillo Laiz R, Fernandez Buenaga R, Rebolleda Fernandez G. Topical cyclosporine for atopic keratoconjunctivitis. Cochrane Database Syst Rev 2012;9:CD009078.
[578] Kim BY, Riaz KM, Bakhtiari P, Chan CC, Welder JD, Holland EJ, et al. Medically reversible limbal stem cell disease: clinical features and management strategies. Ophthalmology 2014;121(10):2053–2058.
[579] Kunert KS, Tisdale AS, Stern ME, Smith JA, Gipson IK. Analysis of topical cyclosporine treatment of patients with dry eye syndrome: effect on conjunctival lymphocytes. Arch Ophthalmol 2000;118(11):1489–1496.
[580] Brignole F, Pisella PJ, De Saint Jean M, Goldschild M, Goguel A, Baudouin C. Flow cytometric analysis of inflammatory markers in KCS: 6-month treatment with topical cyclosporin A. Invest Ophthalmol Vis Sci 2001;42(1):90–95.
[581] Gao J, Sana R, Calder V, Calonge M, Lee W, Wheeler LA, et al. Mitochondrial permeability transition pore in inflammatory apoptosis of human conjunctival epithelial cells and T cells: effect of cyclosporin A. Invest Ophthalmol Vis Sci 2013;54:4717–4733.
[582] Tsubota K, Fujita H, Tadano K, Takeuchi T, Murakami T, Saito I, et al. Improvement of lacrimal function by topical application of CyA in murine models of Sjögren's syndrome. Invest Ophthalmol Vis Sci 2001;42(1):101–110.
[583] Brignole F, Pisella PJ, Goldschild M, De Saint Jean M, Goguel A, Baudouin C. Flow cytometric analysis of inflammatory markers in conjunctival epithelial cells of patients with dry eyes. Invest Ophthalmol Vis Sci 2000;41(6):1356–1363.
[584] Strong B, Farley W, Stern ME, Pflugfelder SC. Topical cyclosporine inhibits conjunctival epithelial apoptosis in experimental murine keratoconjunctivitis sicca. Cornea 2005;24(1):80–85.
[585] Gao J, Gelber-Schwalb TA, Addeo JV, Stern ME. Apoptosis in the lacrimal gland and conjunctiva of dry eye dogs. Adv Exp Med Biol 1998;438:453–460.
[586] Sall K, Stevenson OD, Mundorf TK, Reis BL. Two multicenter, randomized studies of the efficacy and safety of cyclosporine ophthalmic emulsion in moderate to severe dry eye disease. CsA Phase 3 Study Group. Ophthalmology 2000;107(4):631–639.
[587] Pflugfelder SC, De Paiva CS, Villarreal AL, Stern ME. Effects of sequential artificial tear and cyclosporine emulsion therapy on conjunctival goblet cell density and transforming growth factor-beta2 production. Cornea 2008;27(1):64–69.
[588] Baiza-Durán L, Medrano-Palafox J, Hernández-Quintela E, Lozano-Alcazar J, Alaníz-de la O JF. A comparative clinical trial of the efficacy of two different aqueous solutions of cyclosporine for the treatment of moderate-to-severe dry eye syndrome. Br J Ophthalmol 2010;94(10):1312–1315.
[589] Chen M, Gong L, Sun X, Xie H, Zhang Y, Zou L, et al. A comparison of cyclosporine 0.05% ophthalmic emulsion versus vehicle in Chinese patients with moderate to severe dry eye disease: an eight-week, multicenter, randomized, double-blind, parallel-group trial. J Ocul Pharmacol Ther 2010;26:361–366.
[590] Su MY, Perry HD, Barsam A, Perry AR, Donnenfeld ED, Wittpenn JR, et al. The effect of decreasing the dosage of cyclosporine A 0.05% on dry eye disease after 1 year of twice-daily therapy. Cornea 2011;30(10):1098–1104.
[591] Deveci H, Kobak S. The efficacy of topical 0.05 % cyclosporine A in patients with dry eye disease associated with Sjogren's syndrome. Int Ophthalmol 2014;34:1043–1048.
[592] Salib GM, McDonald MB, Smolek M. Safety and efficacy of cyclosporine 0.05% drops versus unpreserved artificial tears in dry-eye patients having laser in situ keratomileusis. J Cataract Refract Surg 2006;32:772–778.
[593] Perry HD, Solomon R, Donnenfeld ED, Perry AR, Wittpenn JR, Greenman HE, et al. Evaluation of topical cyclosporine for the treatment of dry eye disease. Arch Ophthalmol 2008;126(8):1046–1050.
[594] Alves M, Fonseca EC, Alves MF, Malki LT, Arruda GV, Reinach PS, et al. Dry eye disease treatment: a systematic review of published trials and a critical appraisal of therapeutic strategies. Ocul Surf 2013;11(3):181–192.
[595] Sacchetti M, Mantelli F, Lambiase A, Mastropasqua A, Merlo D, Bonini S. Systematic review of randomised clinical trials on topical ciclosporin A for the treatment of dry eye disease. Br J Ophthalmol 2014;98(8):1016–1022.
[596] Zhou XQ, Wei RL. Topical cyclosporine A in the treatment of dry eye: a systematic review and meta-analysis. Cornea 2014;33(7):760–767.
[597] Wan KH, Chen LJ, Young AL. Efficacy and Safety of Topical 0.05% Cyclosporine Eye Drops in the Treatment of Dry Eye Syndrome: A Systematic Review and Meta-analysis. Ocul Surf 2015;13(3):213–225.
[598] Brown MM, Brown GC, Brown HC, Peet J, Roth Z. Value-based medicine, comparative effectiveness, and cost-effectiveness analysis of topical cyclosporine for the treatment of dry eye syndrome. Arch Ophthalmol 2009;127(2):146–152.
[599] Perry HD, Doshi-Carnevale S, Donnenfeld ED, Solomon R, Biser SA, Bloom AH. Efficacy of commercially available topical cyclosporine A 0.05% in the treatment of meibomian gland dysfunction. Cornea 2006;25(2):171–175.
[600] Rubin M, Rao SN. Efficacy of topical cyclosporin 0.05% in the treatment of posterior blepharitis. J Ocul Pharmacol Ther 2006;22(1):47–53.
[601] Schechter BA, Katz RS, Friedman LS. Efficacy of topical cyclosporine for the treatment of ocular rosacea. Adv Ther 2009;26(6):651–659.
[602] Prabhasawat P, Tesavibul N, Karnchanachetanee C, Kasemson S. Efficacy of cyclosporine 0.05% eye drops in Stevens Johnson syndrome with chronic dry eye. J Ocul Pharmacol Ther 2013;29(3):372–377.
[603] Wilson SE, Perry HD. Long-term resolution of chronic dry eye symptoms and signs after topical cyclosporine treatment. Ophthalmology 2007;114(1):76–79.
[604] Leonardi A, Van Setten G, Amrane M, Ismail D, Garrigue JS, Figueiredo FC, et al. Efficacy and safety of 0.1% cyclosporine A cationic emulsion in the treatment of severe dry eye disease: a multicenter randomized trial. Eur J Ophthalmol 2016;26(4):287–296.
[605] Takeuchi H, Okuyama K, Konno O, Jojima Y, Akashi I, Nakamura Y, et al. Optimal dose and target trough level in cyclosporine and tacrolimus conversion in renal transplantation as evaluated by lymphocyte drug sensitivity and pharmacokinetic parameters. Transplant Proc 2005;37(4):1745–1747.
[606] Sanz-Marco E, Udaondo P, García-Delpech S, Vazquez A, Diaz-Llopis M. Treatment of refractory dry eye associated with graft versus host disease with 0.03% tacrolimus eyedrops. J Ocul Pharmacol Ther 2013;29(8):776–783.
[607] Moscovici BK, Holzchuh R, Sakassegawa-Naves FE, Hoshino-Ruiz DR, Albers MB, Santo RM, et al. Treatment of Sjögren's syndrome dry eye using 0.03% tacrolimus eye drop: Prospective double-blind randomized study. Cont Lens Anter Eye 2015;38(5):373–378.
[608] Liu X, Wang S, Kao AA, Long Q. The effect of topical pranoprofen 0.1% on the clinical evaluation and conjunctival HLA-DR expression in dry eyes. Cornea 2012;31(11):1235–1239.
[609] Rolando M, Barabino S, Alongi S, Calabria G. Topical non-preserved diclofenac therapy for keratoconjunctivitis sicca. Adv Exp Med Biol 2002;506(Pt B):1237–1240.
[610] Aragona P, Stilo A, Ferreri F, Mobrici M. Effects of the topical treatment with NSAIDs on corneal sensitivity and ocular surface of Sjögren's syndrome patients. Eye (Lond) 2005;19(5):535–539.
[611] Schechter BA. Ketorolac during the induction phase of cyclosporin-A therapy. J Ocul Pharmacol Ther 2006;22(2):150–154.
[612] Sawazaki R, Ishihara T, Usui S, Hayashi E, Tahara K, Hoshino T, et al. Diclofenac protects cultured human corneal epithelial cells against hyperosmolarity and ameliorates corneal surface damage in a rat model of dry eye. Invest Ophthalmol Vis Sci 2014;55:2547–2556.
[613] Avisar R, Robinson A, Appel I, Yassur Y, Weinberger D. Diclofenac sodium, 0.1% (Voltaren Ophtha), versus sodium chloride, 5%, in the treatment of filamentary keratitis. Cornea 2000;19(2):145–147.
[614] Isawi H, Dhaliwal DK. Corneal melting and perforation in Stevens Johnson syndrome following topical bromfenac use. J Cataract Refract Surg 2007;33(9):1644–1646.
[615] Singer DD, Kennedy J, Wittpenn JR. Topical NSAIDs effect on corneal sensitivity. Cornea 2015;34(5):541–543.
[616] Aragona P, Di Pietro R. Is it safe to use topical NSAIDs for corneal sensitivity in Sjögren's syndrome patients? Expert Opin Drug Saf 2007;6(1):33–43.
[617] Swann DA, Sotman S, Dixon M, Brooks C. The isolation and partial characterization of the major glycoprotein (LGP-I) from the articular lubricating fraction from bovine synovial fluid. Biochem J 1977;161(3):473–485.
[618] Schmidt TA, Sullivan DA, Knop E, Richards SM, Knop N, Liu S, et al. Transcription, translation, and function of lubricin, a boundary lubricant, at the ocular surface. JAMA Ophthalmol 2013;131(6):766–776.
[619] Schmidt TA, Gastelum NS, Nguyen QT, Schumacher BL, Sah RL. Boundary lubrication of articular cartilage: role of synovial fluid constituents. Arthritis Rheum 2007;56(3):882–891.
[620] Das S, Banquy X, Zappone B, Greene GW, Jay GD, Israelachvili JN. Synergistic interactions between grafted hyaluronic acid and lubricin provide enhanced wear protection and lubrication. Biomacromolecules 2013;14(5):1669–1677.
[621] Bonnevie ED, Galesso D, Secchieri C, Cohen I, Bonassar LJ. Elastoviscous Transitions of Articular Cartilage Reveal a Mechanism of Synergy between Lubricin and Hyaluronic Acid. PLoS One 2015;10:e0143415.
[622] Iqbal SM, Leonard C, Regmi SC, De Rantere D, Tailor P, Ren G, et al. Lubricin/Proteoglycan 4 binds to and regulates the activity of Toll-Like Receptors In Vitro. Sci Rep 2016;6:18910.
[623] Alquraini A, Garguilo S, D'Souza G, Zhang LX, Schmidt TA, Jay GD, et al. The interaction of lubricin/proteoglycan 4 (PRG4) with toll-like receptors 2 and 4: an anti-inflammatory role of PRG4 in synovial fluid. Arthritis Res Ther 2015;17:353.
[624] Al-Sharif A, Jamal M, Zhang LX, Larson K, Schmidt TA, Jay GD, et al. Lubricin/Proteoglycan 4 Binding to CD44 Receptor: A Mechanism of the Suppression of Proinflammatory Cytokine-Induced Synoviocyte Proliferation by Lubricin. ;67(6):1503–1513.
[625] Samsom ML, Morrison S, Masala N, Sullivan BD, Sullivan DA, Sheardown H, et al. Characterization of full-length recombinant human Proteoglycan 4 as an ocular surface boundary lubricant. Exp Eye Res 2014;127:14–19.
[626] Lambiase A, Sullivan BD, Schmidt TA, Sullivan DA, Jay GD, Truitt ER, et al. A Two-Week, Randomized, Double-masked Study to Evaluate Safety and Efficacy of Lubricin (150 mug/mL) Eye Drops Versus Sodium Hyaluronate (HA) 0.18% Eye Drops (Vismed(R)) in Patients with Moderate Dry Eye Disease. Ocul Surf 2017;15:77–87.
[627] Lee HK, Lee KS, Kim HC, Lee SH, Kim EK. Nerve growth factor concentration and implications in photorefractive keratectomy vs laser in situ keratomileusis. Am J Ophthalmol 2005;139(6):965–971.
[628] Yoon JS, Choi SH, Lee JH, Lee SJ, Lee SY. Ocular surface inflammation, and nerve growth factor level in tears in active thyroid-associated ophthalmopathy. Graefes Arch Clin Exp Ophthalmol 2010;248(2):271–276.
[629] Lambiase A, Micera A, Sacchetti M, Cortes M, Mantelli F, Bonini S. Alterations of tear neuromediators in dry eye disease. Arch Ophthalmol 2011;129(8):981–986.
[630] Patapoutian A, Reichardt LF. Trk receptors: mediators of neurotrophin action. Curr Opin Neurobiol 2001;11(3):272–280.
[631] de Castro F, Silos-Santiago I, López de Armentia M, Barbacid M, Belmonte C. Corneal innervation and sensitivity to noxious stimuli in trkA knockout mice. Eur J Neurosci 1998;10(1):146–152.
[632] Qi H, Li DQ, Shine HD, Chen Z, Yoon KC, Jones DB, et al. Nerve growth factor and its receptor TrkA serve as potential markers for human corneal epithelial progenitor cells. Exp Eye Res 2008;86(1):34–40.
[633] Coassin M, Lambiase A, Costa N, De Gregorio A, Sgrulletta R, Sacchetti M, et al. Efficacy of topical nerve growth factor treatment in dogs affected by dry eye. Graefes Arch Clin Exp Ophthalmol 2005;243(2):151–155.
[634] Bonini S, Rama P, Olzi D, Lambiase A. Neurotrophic keratitis. Eye (Lond) 2003;17(8):989–995.
[635] Ma K, Yan N, Huang Y, Cao G, Deng J, Deng Y. Effects of nerve growth factor on nerve regeneration after corneal nerve damage. Int J Clin Exp Med 2014;7(11):4584–4589.
[636] Jain P, Li R, Lama T, Saragovi HU, Cumberlidge G, Meerovitch K. An NGF mimetic, MIM-D3, stimulates conjunctival cell glycoconjugate secretion and demonstrates therapeutic efficacy in a rat model of dry eye. Exp Eye Res 2011;93(4):503–512.
[637] Meerovitch K, Torkildsen G, Lonsdale J, Goldfarb H, Lama T, Cumberlidge G, et al. Safety and efficacy of MIM-D3 ophthalmic solutions in a randomized, placebo-controlled Phase 2 clinical trial in patients with dry eye. Clin Ophthalmol 2013;7:1275–1285.
[638] Lee RH, Pulin AA, Seo MJ, Kota DJ, Ylostalo J, Larson BL, et al. Intravenous hMSCs improve myocardial infarction in mice because cells embolized in lung are activated to secrete the anti-inflammatory protein TSG-6. Cell Stem Cell 2009;5(1):54–63.
[639] Roddy GW, Oh JY, Lee RH, Bartosh TJ, Ylostalo J, Coble K, et al. Action at a distance: systemically administered adult stem/progenitor cells (MSCs) reduce inflammatory damage to the cornea without engraftment and primarily by secretion of TNF-alpha stimulated gene/protein 6. Stem Cells 2011;29:1572–1579.
[640] Choi H, Lee RH, Bazhanov N, Oh JY, Prockop DJ. Anti-inflammatory protein TSG-6 secreted by activated MSCs attenuates zymosan-induced mouse peritonitis by decreasing TLR2/NF-κB signaling in resident macrophages. Blood 2011;118(2):330–338.
[641] Kim JA, Ko JH, Ko AY, Lee HJ, Kim MK, Wee WR, et al. TSG-6 protects corneal endothelium from transcorneal cryoinjury in rabbits. Invest Ophthalmol Vis Sci 2014;55(8):4905–4912.
[642] Kim YJ, Ryu JS, Park SY, Lee HJ, Ko JH, Kim MK, et al. Comparison of Topical Application of TSG-6, Cyclosporine, and Prednisolone for Treating Dry Eye. Cornea 2016;35(4):536–542.
[643] Oh JY, Roddy GW, Choi H, Lee RH, Ylöstalo JH, Rosa Jr. RH, et al. Anti-inflammatory protein TSG-6 reduces inflammatory damage to the cornea following chemical and mechanical injury. Proc Natl Acad Sci U S A 2010;107(39):16875–16880.
[644] Lee MJ, Kim DH, Ryu JS, Ko AY, Ko JH, Kim MK, et al. Topical TSG-6 Administration Protects the Ocular Surface in Two Mouse Models of Inflammation-Related Dry Eye. Invest Ophthalmol Vis Sci 2015;56:5175–5181.
[645] Furst DE. Anakinra: review of recombinant human interleukin-I receptor antagonist in the treatment of rheumatoid arthritis. Clin Ther 2004;26(12):1960–1975.
[646] Arend WP. Interleukin-1 receptor antagonist. Adv Immunol 1993;54:167–227.
[647] Yamada J, Dana MR, Sotozono C, Kinoshita S. Local suppression of IL-1 by receptor antagonist in the rat model of corneal alkali injury. Exp Eye Res 2003;76(2):161–167.
[648] Keane-Myers AM, Miyazaki D, Liu G, Dekaris I, Ono S, Dana MR. Prevention of allergic eye disease by treatment with IL-1 receptor antagonist. Invest Ophthalmol Vis Sci 1999;40(12):3041–3046.
[649] Biswas PS, Banerjee K, Zheng M, Rouse BT. Counteracting corneal immunoinflammatory lesion with interleukin-1 receptor antagonist protein. J Leukoc Biol 2004;76(4):868–875.
[650] Stapleton WM, Chaurasia SS, Medeiros FW, Mohan RR, Sinha S, Wilson SE. Topical interleukin-1 receptor antagonist inhibits inflammatory cell infiltration into the cornea. Exp Eye Res 2008;86(5):753–757.
[651] Vijmasi T, Chen FY, Chen YT, Gallup M, McNamara N. Topical administration of interleukin-1 receptor antagonist as a therapy for aqueous-deficient dry eye in autoimmune disease. Mol Vis 2013;19:1957–1965.
[652] Amparo F, Dastjerdi MH, Okanobo A, Ferrari G, Smaga L, Hamrah P, et al. Topical interleukin 1 receptor antagonist for treatment of dry eye disease: a randomized clinical trial. JAMA Ophthalmol 2013;131(6):715–723.
[653] Aggarwal BB. Signalling pathways of the TNF superfamily: a double-edged sword. Nat Rev Immunol 2003;3(9):745–756.
[654] Cope AP, Londei M, Chu NR, Cohen SB, Elliott MJ, Brennan FM, et al. Chronic exposure to tumor necrosis factor (TNF) in vitro impairs the activation of T cells through the T cell receptor/CD3 complex; reversal in vivo by anti-TNF antibodies in patients with rheumatoid arthritis. J Clin Invest 1994;94(2):749–760.
[655] Pflugfelder SC, Jones D, Ji Z, Afonso A, Monroy D. Altered cytokine balance in the tear fluid and conjunctiva of patients with Sjögren's syndrome keratoconjunctivitis sicca. Curr Eye Res 1999;19(3):201–211.
[656] Yoon KC, Jeong IY, Park YG, Yang SY. Interleukin-6 and tumor necrosis factor-alpha levels in tears of patients with dry eye syndrome. Cornea 2007;26(4):431–437.
[657] Lam H, Bleiden L, de Paiva CS, Farley W, Stern ME, Pflugfelder SC. Tear cytokine profiles in dysfunctional tear syndrome. Am J Ophthalmol 2009;147(2):198–205. e1.
[658] Mariette X, Ravaud P, Steinfeld S, Baron G, Goetz J, Hachulla E, et al. Inefficacy of infliximab in primary Sjögren's syndrome: results of the randomized, controlled Trial of Remicade in Primary Sjögren's Syndrome (TRIPSS). Arthritis Rheum 2004;50(4):1270–1276.
[659] Sankar V, Brennan MT, Kok MR, Leakan RA, Smith JA, Manny J, et al. Etanercept in Sjögren's syndrome: a twelve-week randomized, double-blind, placebo-controlled pilot clinical trial. Arthritis Rheum 2004;50(7):2240–2245.
[660] Zandbelt MM, de Wilde P, van Damme P, Hoyng CB, van de Putte L, van den Hoogen F. Etanercept in the treatment of patients with primary Sjögren's syndrome: a pilot study. J Rheumatol 2004;31(1):96–101.
[661] Moutsopoulos NM, Katsifis GE, Angelov N, Leakan RA, Sankar V, Pillemer S, et al. Lack of efficacy of etanercept in Sjögren syndrome correlates with failed suppression of tumour necrosis factor alpha and systemic immune activation. Ann Rheum Dis 2008;67(10):1437–1443.
[662] Li Z, Choi W, Oh HJ, Yoon KC. Effectiveness of topical infliximab in a mouse model of experimental dry eye. Cornea 2012;31(Suppl 1):S25–S31.
[663] Ji YW, Byun YJ, Choi W, Jeong E, Kim JS, Noh H, et al. Neutralization of ocular surface TNF-α reduces ocular surface and lacrimal gland inflammation induced by in vivo dry eye. Invest Ophthalmol Vis Sci 2013;54(12):7557–7566.
[664] Zheng X, de Paiva CS, Li DQ, Farley WJ, Pflugfelder SC. Desiccating stress promotion of Th17 differentiation by ocular surface tissues through a dendritic cell-mediated pathway. Invest Ophthalmol Vis Sci 2010;51(6):3083–3091.
[665] Chauhan SK, Dana R. Role of Th17 cells in the immunopathogenesis of dry eye disease. Mucosal Immunol 2009;2(4):375–376.
[666] De Paiva CS, Chotikavanich S, Pangelinan SB, Pitcher 3rd JD, Fang B, Zheng X, et al. IL-17 disrupts corneal barrier following desiccating stress. Mucosal Immunol 2009;2(3):243–253.
[667] Chauhan SK, Jin Y, Goyal S, Lee HS, Fuchsluger TA, Lee HK, et al. A novel pro-lymphangiogenic function for Th17/IL-17. Blood 2011;118(17):4630–4634.
[668] Peral A, Domínguez-Godínez CO, Carracedo G, Pintor J. Therapeutic targets in dry eye syndrome. Drug News Perspect 2008;21(3):166–176.
[669] Kam WR, Sullivan DA. Neurotransmitter influence on human meibomian gland epithelial cells. Invest Ophthalmol Vis Sci 2011;52(12):8543–8548.
[670] Lambiase A, Sacchetti M, Bonini S. Nerve growth factor therapy for corneal disease. Curr Opin Ophthalmol 2012;23(4):296–302.
[671] Millard M, Odde S, Neamati N. Integrin targeted therapeutics. Theranostics 2011;1:154–188.
[672] Marlin SD, Springer TA. Purified intercellular adhesion molecule-1 (ICAM-1) is a ligand for lymphocyte function-associated antigen 1 (LFA-1). Cell 1987;51(5):813–819.
[673] Grakoui A, Bromley SK, Sumen C, Davis MM, Shaw AS, Allen PM, et al. The immunological synapse: a molecular machine controlling T cell activation. Science 1999;285(5425):221–227.
[674] Zhong M, Gadek TR, Bui M, Shen W, Burnier J, Barr KJ, et al. Discovery and Development of Potent LFA-1/ICAM-1 Antagonist SAR 1118 as an Ophthalmic Solution for Treating Dry Eye. ACS Med Chem Lett 2012;3(3):203–206.
[675] Sun Y, Zhang R, Gadek TR, O'Neill CA, Pearlman E. Corneal inflammation is inhibited by the LFA-1 antagonist, lifitegrast (SAR 1118). J Ocul Pharmacol Ther 2013;29(4):395–402.
[676] Perez VL, Pflugfelder SC, Zhang S, Shojaei A, Haque R. Lifitegrast, a Novel Integrin Antagonist for Treatment of Dry Eye Disease. Ocul Surf 2016;14(2):207–215.
[677] Semba CP, Torkildsen GL, Lonsdale JD, McLaurin EB, Geffin JA, Mundorf TK, et al. A phase 2 randomized, double-masked, placebo-controlled study of a novel integrin antagonist (SAR 1118) for the treatment of dry eye. Am J Ophthalmol 2012;153(6):1050–1060. e1.
[678] Sheppard JD, Torkildsen GL, Lonsdale JD, D'Ambrosio Jr. FA, McLaurin EB, Eiferman RA, et al. Lifitegrast ophthalmic solution 5.0% for treatment of dry eye disease: results of the OPUS-1 phase 3 study. Ophthalmology 2014;121(2):475–483.
[679] Tauber J, Karpecki P, Latkany R, Luchs J, Martel J, Sall K, et al. Lifitegrast Ophthalmic Solution 5.0% versus Placebo for Treatment of Dry Eye Disease: Results of the Randomized Phase III OPUS-2 Study. Ophthalmology 2015;122(12):2423–2431.
[680] Donnenfeld ED, Karpecki PM, Majmudar PA, Nichols KK, Raychaudhuri A, Roy M, et al. Safety of Lifitegrast Ophthalmic Solution 5.0% in Patients With Dry Eye Disease: A 1-Year, Multicenter, Randomized, Placebo-Controlled Study. Cornea 2016;35:741–748.
[681] Shine WE, McCulley JP, Pandya AG. Minocycline effect on meibomian gland lipids in meibomianitis patients. Exp Eye Res 2003;76(4):417–420.
[682] Ta CN, Shine WE, McCulley JP, Pandya A, Trattler W, Norbury JW. Effects of minocycline on the ocular flora of patients with acne rosacea or seborrheic blepharitis. Cornea 2003;22(6):545–548.
[683] Dougherty JM, McCulley JP, Silvany RE, Meyer DR. The role of tetracycline in chronic blepharitis. Inhibition of lipase production in staphylococci. Invest Ophthalmol Vis Sci 1991;32(11):2970–2975.
[684] Solomon A, Rosenblatt M, Li DQ, Liu Z, Monroy D, Ji Z, et al. Doxycycline inhibition of interleukin-1 in the corneal epithelium. Invest Ophthalmol Vis Sci 2000;41(9):2544–2557.
[685] Li Y, Kuang K, Yerxa B, Wen Q, Rosskothen H, Fischbarg J. Rabbit conjunctival epithelium transports fluid, and P2Y2(2) receptor agonists stimulate Cl(-) and fluid secretion. Am J Physiol Cell Physiol 2001;281(2):C595–C602.
[686] Li DQ, Luo L, Chen Z, Kim HS, Song XJ, Pflugfelder SC. JNK and ERK MAP kinases mediate induction of IL-1beta, TNF-alpha and IL-8 following hyperosmolar stress in human limbal epithelial cells. Exp Eye Res 2006;82(4):588–596.
[687] Zhang Z, Yang WZ, Zhu ZZ, Hu QQ, Chen YF, He H, et al. Therapeutic effects of topical doxycycline in a benzalkonium chloride-induced mouse dry eye model. Invest Ophthalmol Vis Sci 2014;55:2963–2974.
[688] Liu Y, Kam WR, Ding J, Sullivan DA. Can tetracycline antibiotics duplicate the ability of azithromycin to stimulate human meibomian gland epithelial cell differentiation? Cornea 2015;34(3):342–346.
[689] Hoeprich PD, Warshauer DM. Entry of four tetracyclines into saliva and tears. Antimicrob Agents Chemother 1974;5(3):330–336.
[690] Driver PJ, Lemp MA. Meibomian gland dysfunction. Surv Ophthalmol 1996 Mar-Apr;40(5):343–367.
[691] Forton F, Germaux MA, Brasseur T, De Liever A, Laporte M, Mathys C, et al. Demodicosis and rosacea: epidemiology and significance in daily dermatologic practice. J Am Acad Dermatol 2005;52(1):74–87.
[692] Mc Aleer MA, Lacey N, Powell FC. The pathophysiology of rosacea. G Ital Dermatol Venereol 2009;144(6):663–671.
[693] Lazaridou E, Giannopoulou C, Fotiadou C, Vakirlis E, Trigoni A, Ioannides D. The potential role of microorganisms in the development of rosacea. J Dtsch Dermatol Ges 2011;9(1):21–25.
[694] Jarmuda S, O'Reilly N, Zaba R, Jakubowicz O, Szkaradkiewicz A, Kavanagh K. Potential role of Demodex mites and bacteria in the induction of rosacea. J Med Microbiol 2012;61(Pt 11):1504–1510.
[695] van Zuuren EJ, Fedorowicz Z. Interventions for Rosacea. JAMA 2015;314:2403–2404.
[696] van Zuuren EJ, Fedorowicz Z, Carter B, van der Linden MM, Charland L. Interventions for rosacea. Cochrane Database Syst Rev 2015;4:CD003262.
[697] Ding J, Kam WR, Dieckow J, Sullivan DA. The influence of 13-cis retinoic acid on human meibomian gland epithelial cells. Invest Ophthalmol Vis Sci 2013;54(6):4341–4350.
[698] Macdonald A, Feiwel M. Perioral dermatitis: aetiology and treatment with tetracycline. Br J Dermatol 1972;87(4):315–319.
[699] Jansen T, Plewig G. Rosacea: classification and treatment. J R Soc Med 1997;90(3):144–150.
[700] Frucht-Pery J, Chayet AS, Feldman ST, Lin S, Brown SI. The effect of doxycycline on ocular rosacea. Am J Ophthalmol 1989;107(4):434–435.
[701] Pfeffer I, Borelli C, Zierhut M, Schaller M. Treatment of ocular rosacea with 40 mg doxycycline in a slow release form. J Dtsch Dermatol Ges 2011;9(11):904–907.
[702] Seal DV, Wright P, Ficker L, Hagan K, Troski M, Menday P. Placebo controlled trial of fusidic acid gel and oxytetracycline for recurrent blepharitis and rosacea. Br J Ophthalmol 1995;79(1):42–45.
[703] Määttä M, Kari O, Tervahartiala T, Peltonen S, Kari M, Saari M, et al. Tear fluid levels of MMP-8 are elevated in ocular rosacea-treatment effect of oral doxycycline. Graefes Arch Clin Exp Ophthalmol 2006;244(8):957–962.
[704] Gulbenkian A, Myers J, Fries D. Hamster flank organ hydrolase and lipase activity. J Invest Dermatol 1980;75(4):289–292.
[705] Lindsley K, Matsumura S, Hatef E, Akpek EK. Interventions for chronic blepharitis. Cochrane Database Syst Rev 2012;5:CD005556.
[706] Voils SA, Evans ME, Lane MT, Schosser RH, Rapp RP. Use of macrolides and tetracyclines for chronic inflammatory diseases. Ann Pharmacother 2005;39(1):86–94.
[707] Aronowicz JD, Shine WE, Oral D, Vargas JM, McCulley JP. Short term oral minocycline treatment of meibomianitis. Br J Ophthalmol 2006;90(7):856–860.
[708] Yoo SE, Lee DC, Chang MH. The effect of low-dose doxycycline therapy in chronic meibomian gland dysfunction. Korean J Ophthalmol 2005;19(4):258–263.
[709] Seitsalo H, Niemelä RK, Marinescu-Gava M, Vuotila T, Tjäderhane L, Salo T. Effectiveness of low-dose doxycycline (LDD) on clinical symptoms of Sjögren's syndrome: a randomized, double-blind, placebo controlled cross-over study. J Negat Results Biomed 2007;6:11.
[710] Lee H, Min K, Kim EK, Kim TI. Minocycline Controls Clinical Outcomes and Inflammatory Cytokines in Moderate and Severe Meibomian Gland Dysfunction. Am J Ophthalmol 2012;154(6):949–957.
[711] Gilbard JP. The scientific context and basis of the pharmacologic management of dry eyes. Ophthalmol Clin N Am 2005;18:475–484.
[712] Del Rosso JQ. A status report on the use of subantimicrobial-dose doxycycline: a review of the biologic and antimicrobial effects of the tetracyclines. Cutis 2004;74(2):118–122.
[713] Skidmore R, Kovach R, Walker C, Thomas J, Bradshaw M, Leyden J, et al. Effects of subantimicrobial-dose doxycycline in the treatment of moderate acne. Arch Dermatol 2003;139(4):459–464.
[714] Velicer CM, Heckbert SR, Lampe JW, Potter JD, Robertson CA, Taplin SH. Antibiotic use in relation to the risk of breast cancer. JAMA 2004;291:827–835.
[715] Velicer CM, Heckbert SR, Rutter C, Lampe JW, Malone K. Association between antibiotic use prior to breast cancer diagnosis and breast tumour characteristics (United States). Cancer Causes Control 2006;17(3):307–313.
[716] García Rodríguez LA, González-Pérez A. Use of antibiotics and risk of breast cancer. Am J Epidemiol 2005;161(7):616–619.
[717] Kashkouli MB, Fazel AJ, Kiavash V, Nojomi M, Ghiasian L. Oral azithromycin versus doxycycline in meibomian gland dysfunction: a randomised double-masked open-label clinical trial. Br J Ophthalmol 2015;99(2):199–204.
[718] Greene JB, Jeng BH, Fintelmann RE, Margolis TP. Oral azithromycin for the treatment of meibomitis. JAMA Ophthalmol 2014;132(1):121–122.
[719] Qiao J, Yan X. Emerging treatment options for meibomian gland dysfunction. Clin Ophthalmol 2013;7:1797–1803.
[720] Igami TZ, Holzchuh R, Osaki TH, Santo RM, Kara-Jose N, Hida RY. Oral azithromycin for treatment of posterior blepharitis. Cornea 2011;30(10):1145–1149.
[721] Bakar O, Demircay Z, Toker E, Cakir S. Ocular signs, symptoms and tear function tests of papulopustular rosacea patients receiving azithromycin. J Eur Acad Dermatol Venereol 2009;23(5):544–549.
[722] Fernandez-Obregon A. Oral use of azithromycin for the treatment of acne rosacea. Arch Dermatol 2004;140(4):489–490.
[723] Bakar O, Demirçay Z, Gürbüz O. Therapeutic potential of azithromycin in rosacea. Int J Dermatol 2004;43(2):151–154.
[724] Giamarellos-Bourboulis EJ. Macrolides beyond the conventional antimicrobials: a class of potent immunomodulators. Int J Antimicrob Agents 2008;31(1):12–20.
[725] Labro MT. J Antimicrob Chemother 1998;41(Suppl B):37–46.
[726] Rubin BK. Immunomodulatory properties of macrolides: overview and historical perspective. Am J Med 2004;117(Suppl 9A):2S–4S.
[727] Modi S, Harting M, Rosen T. Azithromycin as an alternative rosacea therapy when tetracyclines prove problematic. J Drugs Dermatol 2008;7(9):898–899.
[728] Singhi MK, Ghiya BC, Dhabhai RK. Comparison of oral azithromycin pulse with daily doxycycline in the treatment of acne vulgaris. Indian J Dermatol Venereol Leprol 2003 Jul-Aug;69(4):274–276.
[729] Antonio JR, Pegas JR, Cestari TF, Do Nascimento LV. Azithromycin pulses in the treatment of inflammatory and pustular acne: efficacy, tolerability and safety. J Dermatol Treat 2008;19(4):210–215.
[730] Luchs J. Efficacy of topical azithromycin ophthalmic solution 1% in the treatment of posterior blepharitis. Adv Ther 2008;25(9):858–870.
[731] Haque RM, Torkildsen GL, Brubaker K, Zink RC, Kowalski RP, Mah FS, et al. Multicenter open-label study evaluating the efficacy of azithromycin ophthalmic solution 1% on the signs and symptoms of subjects with blepharitis. Cornea 2010;29(8):871–877.
[732] Opitz DL, Tyler KF. Efficacy of azithromycin 1% ophthalmic solution for treatment of ocular surface disease from posterior blepharitis. Clin Exp Optom 2011;94(2):200–206.
[733] Nichols JJ, Bickle KM, Zink RC, Schiewe MD, Haque RM, Nichols KK. Safety and efficacy of topical azithromycin ophthalmic solution 1.0% in the treatment of contact lens-related dry eye. Eye Contact Lens 2012;38(2):73–79.
[734] Fadlallah A, Rami HE, Fahd D, Dunia I, Bejjani R, Chlela E, et al. Azithromycin 1.5% ophthalmic solution: efficacy and treatment modalities in chronic blepharitis. Arq Bras Oftalmol 2012 May-Jun;75(3):178–182.
[735] Hosseini K, Lindstrom RL, Foulks G, Nichols KK. A randomized, double-masked, parallel-group, comparative study to evaluate the clinical efficacy and safety of 1% azithromycin-0.1% dexamethasone combination compared to 1% azithromycin alone, 0.1% dexamethasone alone, and vehicle in the treatment of subjects with blepharitis. Clin Ophthalmol 2016;10:1495–1503.
[736] Foulks GN, Borchman D, Yappert M, Kakar S. Topical azithromycin and oral doxycycline therapy of meibomian gland dysfunction: a comparative clinical and spectroscopic pilot study. Cornea 2013;32(1):44–53.
[737] Wladis EJ, Bradley EA, Bilyk JR, Yen MT, Mawn LA. Oral Antibiotics for Meibomian Gland-Related Ocular Surface Disease: A Report by the American Academy of Ophthalmology. Ophthalmology 2016;123(3):492–496.
[738] Kirkness CM, Adams GG, Dilly PN, Lee JP. Botulinum toxin A-induced protective ptosis in corneal disease. Ophthalmology 1988;95(4):473–480.
[739] Gossman MD, Bowe BE, Tanenbaum M. Reversible suture tarsorrhaphy for eyelid malposition and keratopathy. Ophthalmic Surg 1991;22(4):237–239.
[740] Chhadva P, Alexander A, McClellan AL, McManus KT, Seiden B, Galor A. The impact of conjunctivochalasis on dry eye symptoms and signs. Invest Ophthalmol Vis Sci 2015;56(5):2867–2871.
[741] Uchino M, Dogru M, Yagi Y, Goto E, Tomita M, Kon T, et al. The features of dry eye disease in a Japanese elderly population. Optom Vis Sci 2006;83(11):797–802.
[742] Hoh H, Schirra F, Kienecker C, Ruprecht KW. Lid-parallel conjunctival folds are a sure diagnostic sign of dry eye. Ophthalmologe 1995;92:802–808.
[743] Németh J, Fodor E, Lang Z, Kosina-Hagyó K, Berta A, Komár T, et al. Lid-parallel conjunctival folds (LIPCOF) and dry eye: a multicentre study. Br J Ophthalmol 2012;96(11):1380–1385.
[744] Huang Y, Sheha H, Tseng SC. Conjunctivochalasis interferes with tear flow from fornix to tear meniscus. Ophthalmology 2013;120(8):1681–1687.
[745] Pult H, Riede-Pult BH. Impact of conjunctival folds on central tear meniscus height. Invest Ophthalmol Vis Sci 2015;56(3):1459–1466.
[746] Liu D. Conjunctivochalasis, A cause of tearing and its management. Ophthal Plast Reconstr Surg 1986;2:25–28.
[747] Petris CK, Holds JB. Medial conjunctival resection for tearing associated with conjunctivochalasis. Ophthal Plast Reconstr Surg 2013 Jul-Aug;29(4):304–307.
[748] Yokoi N, Inatomi T, Kinoshita S. Surgery of the conjunctiva. Dev Ophthalmol 2008;41:138–158.
[749] Nakasato S, Uemoto R, Mizuki N. Thermocautery for inferior conjunctivochalasis. Cornea 2012;31(5):514–519.
[750] Zhang XR, Zhang ZY, Hoffman MR. Electrocoagulative surgical procedure for treatment of conjunctivochalasis. Int Surg 2012 Jan-Mar;97(1):90–93.
[751] Otaka I, Kyu N. A new surgical technique for management of conjunctivochalasis. Am J Ophthalmol 2000;129(3):385–387.
[752] Yang HS, Choi S. New approach for conjunctivochalasis using an argon green laser. Cornea 2013;32(5):574–578.
[753] Price J, O'Day J. A comparative study of tear secretion in blepharospasm and hemifacial spasm patients treated with botulinum toxin. J Clin Neuroophthalmol 1993;13(1):67–71.
[754] Elston JS, Marsden CD, Grandas F, Quinn NP. The significance of ophthalmological symptoms in idiopathic blepharospasm. Eye (Lond) 1988;2(Pt 4):435–439.
[755] Grandas F, Elston J, Quinn N, Marsden CD. Blepharospasm: a review of 264 patients. J Neurol Neurosurg Psychiatr 1988;51(6):767–772.
[756] Jankovic J, Ford J. Blepharospasm and orofacial-cervical dystonia: clinical and pharmacological findings in 100 patients. Ann Neurol 1983;13(4):402–411.
[757] Lu R, Huang R, Li K, Zhang X, Yang H, Quan Y, et al. The influence of benign essential blepharospasm on dry eye disease and ocular inflammation. Am J Ophthalmol 2014;157(3):591–597. e1-2.
[758] Park DI, Shin HM, Lee SY, Lew H. Tear production and drainage after botulinum toxin A injection in patients with essential blepharospasm. Acta Ophthalmol 2013;91(2):e108–e112.
[759] Sahlin S, Chen E, Kaugesaar T, Almqvist H, Kjellberg K, Lennerstrand G. Effect of eyelid botulinum toxin injection on lacrimal drainage. Am J Ophthalmol 2000;129(4):481–486.
[760] Kocabeyoglu S, Sekeroglu HT, Mocan MC, Muz E, Irkec M, Sanac AS. Ocular surface alterations in blepharospasm patients treated with botulinum toxin A injection. Eur J Ophthalmol 2014 Nov-Dec;24(6):830–834.
[761] Horwath-Winter J, Bergloeff J, Floegel I, Haller-Schober EM, Schmut O. Botulinum toxin A treatment in patients suffering from blepharospasm and dry eye. Br J Ophthalmol 2003;87(1):54–56.
[762] Sahlin S, Linderoth R. Eyelid botulinum toxin injections for the dry eye. Dev Ophthalmol 2008;41:187–192.
[763] Vold SD, Carroll RP, Nelson JD. Dermatochalasis and dry eye. Am J Ophthalmol 1993;115(2):216–220.
[764] Floegel I, Horwath-Winter J, Muellner K, Haller-Schober EM. A conservative blepharoplasty may be a means of alleviating dry eye symptoms. Acta Ophthalmol Scand 2003;81(3):230–232.
[765] Moesen I, van den Bosch W, Wubbels R, Paridaens D. Is dry eye associated with acquired aponeurogenic blepharoptosis? Orbit 2014;33(3):173–177.
[766] Bagheri A, Najmi H, Salim RE, Yazdani S. Tear condition following unilateral ptosis surgery. Orbit 2015;34(2):66–71.
[767] Watanabe A, Kakizaki H, Selva D, Ohmae M, Yokoi N, Wakimasu K, et al. Short-term changes in tear volume after blepharoptosis repair. Cornea 2014;33(1):14–17.
[768] Watanabe A, Selva D, Kakizaki H, Oka Y, Yokoi N, Wakimasu K, et al. Long-term Tear Volume Changes After Blepharoptosis Surgery and Blepharoplasty. Invest Ophthalmol Vis Sci 2015;56(1):54–58.
[769] Prischmann J, Sufyan A, Ting JY, Ruffin C, Perkins SW. Dry eye symptoms and chemosis following blepharoplasty: a 10-year retrospective review of 892 cases in a single-surgeon series. JAMA Facial Plast Surg 2013;15:39–46.
[770] Leatherbarrow B, Saha K. Complications of blepharoplasty. Facial Plast Surg 2013;29(4):281–288.
[771] Shao Chunyi, Fu Yao, Lu Linna, Chen Junzhao, Shen Qin, Zhu Huimin, et al. Dynamic Changes of Tear Fluid After Cosmetic Transcutaneous Lower Blepharoplasty Measured by Optical Coherence Tomography. Am J Ophthalmol 2014;158(1):55–63.
[772] Pacella SJ, Codner MA. Minor complications after blepharoplasty: dry eyes, chemosis, granulomas, ptosis, and scleral show. Plast Reconstr Surg 2010;125(2):709–718.
[773] Honavar SG, Bansal AK, Sangwan VS, Rao GN. Amniotic membrane transplantation for ocular surface reconstruction in Stevens-Johnson syndrome. Ophthalmology 2000;107(5):975–979.
[774] Donnenfeld ED, Perry HD, Wallerstein A, Caronia RM, Kanellopoulos AJ, Sforza PD, et al. Subconjunctival mitomycin C for the treatment of ocular cicatricial pemphigoid. Ophthalmology 1999;106:72–78. discussion 9.
[775] Barabino S, Rolando M, Bentivoglio G, Mingari C, Zanardi S, Bellomo R, et al. Role of amniotic membrane transplantation for conjunctival reconstruction in ocular-cicatricial pemphigoid. Ophthalmology 2003;110(3):474–480.
[776] Clearfield E, Muthappan V, Wang X, Kuo IC. Conjunctival autograft for pterygium. Cochrane Database Syst Rev 2016;2:CD011349.
[777] Kaufman SC, Jacobs DS, Lee WB, Deng SX, Rosenblatt MI, Shtein RM. Options and adjuvants in surgery for pterygium: a report by the American Academy of Ophthalmology. Ophthalmology 2013;120(1):201–208.
[778] Foster CS, Sainz De La Maza M. Ocular cicatricial pemphigoid review. Curr Opin Allergy Clin Immunol 2004;4(5):435–439.
[779] Shay E, Kheirkhah A, Liang L, Sheha H, Gregory DG, Tseng SC. Amniotic membrane transplantation as a new therapy for the acute ocular manifestations of Stevens-Johnson syndrome and toxic epidermal necrolysis. Surv Ophthalmol 2009 Nov-Dec;54(6):686–696.
[780] Arya SK, Bhala S, Malik A, Sood S. Role of amniotic membrane transplantation in ocular surface disorders. Nepal J Ophthalmol 2010 Jul-Dec;2(2):145–153.
[781] Gregory DG. Treatment of acute Stevens-Johnson syndrome and toxic epidermal necrolysis using amniotic membrane: a review of 10 consecutive cases. Ophthalmology 2011;118(5):908–914.
[782] Cheng AM, Zhao D, Chen R, Yin HY, Tighe S, Sheha H, et al. Accelerated Restoration of Ocular Surface Health in Dry Eye Disease by Self-Retained Cryopreserved Amniotic Membrane. Ocul Surf 2016;14(1):56–63.
[783] Elwan MA, Ishii T, Ono F, Sakuragawa N. Evidence for the presence of dopamine D1 receptor mRNA and binding sites in monkey amniotic epithelial cells. Neurosci Lett 1999;262(1):9–12.
[784] Elwan MA, Thangavel R, Ono F, Sakuragawa N. Synthesis and release of catecholamines by cultured monkey amniotic epithelial cells. J Neurosci Res 1998;53(1):107–113.
[785] Meller D, Schröder A, Steuhl KP, Theiss C. Neurotrophic Effect of Amniotic Membrane on Neuronal Cell Cultures: An in vitro Model to Study Underlying Action Mechanisms of Amniotic Membrane in the Treatment of Neurotrophic Keratopathy. Invest Ophthalmol Vis Sci 2005;46:875.
[786] Sakuragawa N, Elwan MA, Uchida S, Fujii T, Kawashima K. Non-neuronal neurotransmitters and neurotrophic factors in amniotic epithelial cells: expression and function in humans and monkey. Jpn J Pharmacol 2001;85(1):20–23.
[787] Stelnicki EJ, Doolabh V, Lee S, Levis C, Baumann FG, Longaker MT, et al. Nerve dependency in scarless fetal wound healing. Plast Reconstr Surg 2000;105(1):140–147.
[788] Ryff K, Ryff B, Lighthizer N. Insert and remove and amniotic membrane graft. Rev Optom 2015;152:23–25.
[789] Suri K, Kosker M, Raber IM, Hammersmith KM, Nagra PK, Ayres BD, et al. Sutureless amniotic membrane ProKera for ocular surface disorders: short-term results. Eye Contact Lens 2013;39(5):341–347.
[790] Kolomeyer AM, Do BK, Tu Y, Chu DS. Placement of ProKera in the management of ocular manifestations of acute Stevens-Johnson syndrome in an outpatient. Eye Contact Lens 2013;39(3):e7–11.
[791] Kwon JW, Kim JS, Choi SB, Lee JH, Wee WR. Experimental study of an automated system for the delivery of eyedrops using a microinfusion pump. Am J Ophthalmol 2005;139(3):547–549.
[792] Murube J, Murube E, ChenZhuo L, Rivas L. Subcutaneous abdominal artificial tears pump-reservoir for severe dry eye. Orbit 2003;22(1):29–40.
[793] Murube J, Geerling G. Mechanical pump dacryoreservoirs. Dev Ophthalmol 2008;41:269–282.
[794] Geerling G, Honnicke K, Schröder C, Framme C, Sieg P, Lauer I, et al. Quality of salivary tears following autologous submandibular gland transplantation for severe dry eye. Graefes Arch Clin Exp Ophthalmol 2000;238(1):45–52.
[795] Murube J, Manyari A, ChenZhuo L, Rivas L, Murube I. Labial Salivary Gland Transplantation in Severe Dry Eye. Oper Tech Oculoplast Orbital Reconstr Surg 1998;2:104–110.
[796] Filatov V, Chevaljev V. Surgical Treatment of Parenchymatous Opthalmoxerosis. J Oftalmol Odessa 1951;3:131–137.
[797] Geerling G, Sieg P. Transplantation of the major salivary glands. Dev Ophthalmol 2008;41:255–268.
[798] Murube-del-Castillo J. Transplantation of salivary gland to the lacrimal basin. Scand J Rheumatol Suppl 1986;61:264–267.
[799] Qin J, Zhang L, Cai ZG, Mao C, Liu XJ, Lv L, et al. Microvascular autologous transplantation of partial submandibular gland for severe keratoconjunctivitis sicca. Br J Ophthalmol 2013;97(9):1123–1128.
[800] Geerling G, Garrett JR, Paterson KL, Sieg P, Collin JR, Carpenter GH, et al. Innervation and secretory function of transplanted human submandibular salivary glands. Transplantation 2008;85(1):135–140.
[801] Lasudry J. Experimental approach to surgical treatment of lacrimal insufficiency by microvascular submandibular salivary gland autotransplantation. Bull Soc Belge Ophtalmol 1992;245:45–51.
[802] Kumar PA, Macleod AM, O'Brien BM, Hickey MJ, Knight KR. Microvascular submandibular gland transfer for the management of xerophthalmia; an experimental study. Br J Plast Surg 1990;43(4):431–436.
[803] Murube J, Marcos MG, Javate R. Amylase in mare lacrimale in patients with submandibular salivary gland transplantation to the lacrimal basin. Adv Exp Med Biol 1994;350:565–570.
[804] MacLeod AM, Robbins SP. Submandibular gland transfer in the correction of dry eye. Aust N. Z J Ophthalmol 1992;20(2):99–103.
[805] Geerling G, Sieg P, Bastian GO, Laqua H. Transplantation of the autologous submandibular gland for most severe cases of keratoconjunctivitis sicca. Ophthalmology 1998;105(2):327–335.
[806] Paniello RC. Submandibular gland transfer for severe xerophthalmia. Laryngoscope 2007;117(1):40–44.
[807] Borrelli M, Schröder C, Dart JK, Collin JR, Sieg P, Cree IA, et al. Long-term follow-up after submandibular gland transplantation in severe dry eyes secondary to cicatrizing conjunctivitis. Am J Ophthalmol 2010;150(6):894–904.
[808] Lauer I, Sieg P, Bähre M, Richter E. Salivary gland scintigraphy using technetium-99m-pertechnetate after autotransplantation of the submandibular salivary gland in the correction of dry eye. Eur J Nucl Med 1998;25(2):128–131.
[809] Jacobsen HC, Hakim SG, Trenkle T, Nitschke M, Steven P, Sieg P. Allogenic submandibular gland transplantation following hematopoietic stem cell transplantation. J Craniomaxillofac Surg 2013;41(8):764–769.
[810] Keegan DJ, Geerling G, Lee JP, Blake G, Collin JR, Plant GT. Botulinum toxin treatment for hyperlacrimation secondary to aberrant regenerated seventh nerve palsy or salivary gland transplantation. Br J Ophthalmol 2002;86(1):43–46.
[811] Cai JR, Shan XF, Cai ZG, Zhang X, Yu GY. A new treatment for epiphora secondary to submandibular gland transplantation: transcutaneous atropine gel. Ocul Surf 2014;12(3):221–226.
[812] Leibovitch I, Hoyama E, Limawararut V, Crompton J, Selva D. Novel technique to control hypersecretion from a transplanted autologous submandibular salivary gland for keratoconjunctivitis sicca. Cornea 2006;25(10):1251–1253.
[813] Song B, Zhang L, Liu XJ, Ding C, Wu LL, Gan YH, et al. Proteomic analysis of secretion from human transplanted submandibular gland replacing lacrimal gland with severe keratoconjunctivitis sicca. Biochim Biophys Acta 2012;1824(4):550–560.
[814] Wenkel H, Rummelt V, Naumann GO. Long term results after autologous nasal mucosal transplantation in severe mucus deficiency syndromes. Br J Ophthalmol 2000;84(3):279–284.
[815] Kuckelkorn R, Schrage N, Redbrake C, Kottek A, Reim M. Autologous transplantation of nasal mucosa after severe chemical and thermal eye burns. Acta Ophthalmol Scand 1996;74(5):442–448.
[816] Wang Z, Shen MM, Liu XJ, Si Y, Yu GY. Characteristics of the saliva flow rates of minor salivary glands in healthy people. Arch Oral Biol 2015;60(3):385–392.
[817] Marinho DR, Burmann TG, Kwitko S. Labial salivary gland transplantation for severe dry eye due to chemical burns and Stevens-Johnson syndrome. Ophthal Plast Reconstr Surg 2010 May-Jun;26(3):182–184.
[818] Sant' Anna AE, Hazarbassanov RM, de Freitas D, Gomes JÁ. Minor salivary glands and labial mucous membrane graft in the treatment of severe symblepharon and dry eye in patients with Stevens-Johnson syndrome. Br J Ophthalmol 2012;96(2):234–239.
[819] Fortes MB, Diment BC, Di Felice U, Gunn AE, Kendall JL, Esmaeelpour M, et al. Tear fluid osmolarity as a potential marker of hydration status. Med Sci Sports Exerc 2011;43(8):1590–1597.
[820] Walsh NP, Fortes MB, Esmaeelpour M. Influence of modest changes in whole-body hydration on tear fluid osmolarity: important considerations for dry eye disease detection. Cornea 2011;30:1517. author reply -8.
[821] Walsh NP, Fortes MB, Raymond-Barker P, Bishop C, Owen J, Tye E, et al. Is whole-body hydration an important consideration in dry eye? Invest Ophthalmol Vis Sci 2012;53(10):6622–6627.
[822] Simopoulos AP. Omega-6/omega-3 essential fatty acids: biological effects. World Rev Nutr Diet 2009;99:1–16.
[823] Harris W. Omega-6 and omega-3 fatty acids: partners in prevention. Curr Opin Clin Nutr Metab Care 2010;13(2):125–129.
[824] Calder PC. N-3 polyunsaturated fatty acids and inflammation: from molecular biology to the clinic. Lipids 2003;38(4):343–352.
[825] Serhan CN, Petasis NA. Resolvins and protectins in inflammation resolution. Chem Rev 2011;111(10):5922–5943.
[826] Simopoulos AP. Evolutionary aspects of diet: the omega-6/omega-3 ratio and the brain. Mol Neurobiol 2011;44(2):203–215.
[827] Simopoulos AP. The importance of the ratio of omega-6/omega-3 essential fatty acids. Biomed Pharmacother 2002;56(8):365–379.
[828] Endres S, Ghorbani R, Kelley VE, Georgilis K, Lonnemann G, van der Meer JW, et al. The effect of dietary supplementation with n-3 polyunsaturated fatty acids on the synthesis of interleukin-1 and tumor necrosis factor by mononuclear cells. N Engl J Med 1989;320(5):265–271.
[829] Meydani SN, Endres S, Woods MM, Goldin BR, Soo C, Morrill-Labrode A, et al. Oral (n-3) fatty acid supplementation suppresses cytokine production and lymphocyte proliferation: comparison between young and older women. J Nutr 1991;121:547–555.
[830] Khan NA, Yessoufou A, Kim M, Hichami A. N-3 fatty acids modulate Th1 and Th2 dichotomy in diabetic pregnancy and macrosomia. J Autoimmun 2006;26(4):268–277.
[831] Purasiri P, Mckechnie A, Heys SD, Eremin O. Modulation in vitro of human natural cytotoxicity, lymphocyte proliferative response to mitogens and cytokine production by essential fatty acids. Immunology 1997;92(2):166–172.
[832] Zurier RB, Rossetti RG, Seiler CM, Laposata M. Human peripheral blood T lymphocyte proliferation after activation of the T cell receptor: effects of unsaturated fatty acids. Prostaglandins Leukot Essent Fatty Acids 1999;60(5–6):371–375.
[833] Hampel U, Krüger M, Kunnen C, Garreis F, Willcox M, Paulsen F. In vitro effects of docosahexaenoic and eicosapentaenoic acid on human meibomian gland epithelial cells. Exp Eye Res 2015;140:139–148.
[834] Liu Y, Kam WR, Sullivan DA. Influence of Omega 3 and 6 Fatty Acids on Human Meibomian Gland Epithelial Cells. Cornea 2016;35(8):1122–1126.
[835] Schnebelen C, Viau S, Grégoire S, Joffre C, Creuzot-Garcher CP, Bron AM, et al. Nutrition for the eye: different susceptibility of the retina and the lacrimal gland to dietary omega-6 and omega-3 polyunsaturated fatty acid incorporation. Ophthalmic Res 2009;41(4):216–224.
[836] Viau S, Maire MA, Pasquis B, Grégoire S, Acar N, Bron AM, et al. Efficacy of a 2-month dietary supplementation with polyunsaturated fatty acids in dry eye induced by scopolamine in a rat model. Graefes Arch Clin Exp Ophthalmol 2009;247(8):1039–1050.
[837] Rashid S, Jin Y, Ecoiffier T, Barabino S, Schaumberg DA, Dana MR. Topical omega-3 and omega-6 fatty acids for treatment of dry eye. Arch Ophthalmol 2008;126(2):219–225.
[838] Li Z, Choi JH, Oh HJ, Park SH, Lee JB, Yoon KC. Effects of eye drops containing a mixture of omega-3 essential fatty acids and hyaluronic acid on the ocular surface in desiccating stress-induced murine dry eye. Curr Eye Res 2014;39(9):871–878.
[839] Dartt DA, Hodges RR, Li D, Shatos MA, Lashkari K, Serhan CN. Conjunctival goblet cell secretion stimulated by leukotrienes is reduced by resolvins D1 and E1 to promote resolution of inflammation. J Immunol 2011;186(7):4455–4466.
[840] Erdinest N, Ovadia H, Kormas R, Solomon A. Anti-inflammatory effects of resolvin-D1 on human corneal epithelial cells: in vitro study. J Inflamm (Lond) 2014;11(1):6.
[841] Li N, He J, Schwartz CE, Gjorstrup P, Bazan HE. Resolvin E1 improves tear production and decreases inflammation in a dry eye mouse model. J Ocul Pharmacol Ther 2010;26(5):431–439.
[842] de Paiva Cintia S, Schwartz C Eric, Gjörstrup Per, Pflugfelder Stephen C. Resolvin E1 (RX-10001) Reduces Corneal Epithelial Barrier Disruption and Protects Against Goblet Cell Loss in a Murine Model of Dry Eye. Cornea 2012;31(11):1299–1303.
[843] Torricelli AA, Santhanam A, Agrawal V, Wilson SE. Resolvin E1 analog RX-10045 0.1% reduces corneal stromal haze in rabbits when applied topically after PRK. Mol Vis 2014;20:1710–1716.
[844] Cortina MS, He J, Li N, Bazan NG, Bazan HE. Neuroprotectin D1 synthesis and corneal nerve regeneration after experimental surgery and treatment with PEDF plus DHA. Invest Ophthalmol Vis Sci 2010;51(2):804–810.
[845] Cortina MS, He J, Li N, Bazan NG, Bazan HE. Recovery of corneal sensitivity, calcitonin gene-related peptide-positive nerves, and increased wound healing induced by pigment epithelial-derived factor plus docosahexaenoic acid after experimental surgery. Arch Ophthalmol 2012;130(1):76–83.
[846] Miljanovic B, Trivedi KA, Dana MR, Gilbard JP, Buring JE, Schaumberg DA. Relation between dietary n-3 and n-6 fatty acids and clinically diagnosed dry eye syndrome in women. Am J Clin Nutr 2005;82:887–893.
[847] Walter SD, Gronert K, McClellan AL, Levitt RC, Sarantopoulos KD, Galor A. ω-3 Tear Film Lipids Correlate With Clinical Measures of Dry Eye. Invest Ophthalmol Vis Sci 2016;57(6):2472–2478.
[848] Sullivan BD, Cermak JM, Sullivan RM, Papas AS, Evans JE, Dana MR, et al. Correlations between nutrient intake and the polar lipid profiles of meibomian gland secretions in women with Sjögren's syndrome. Adv Exp Med Biol 2002;506(Pt A):441–447.
[849] Macsai MS. The role of omega-3 dietary supplementation in blepharitis and meibomian gland dysfunction (an AOS thesis). Trans Am Ophthalmol Soc 2008;106:336–356.
[850] Wojtowicz JC, Butovich I, Uchiyama E, Aronowicz J, Agee S, McCulley JP. Pilot, prospective, randomized, double-masked, placebo-controlled clinical trial of an omega-3 supplement for dry eye. Cornea 2011;30(3):308–314.
[851] Bhargava R, Kumar P, Kumar M, Mehra N, Mishra A. A randomized controlled trial of omega-3 fatty acids in dry eye syndrome. Int J Ophthalmol 2013;6(6):811–816.
[852] Oleñik A, Jiménez-Alfaro I, Alejandre-Alba N, Mahillo-Fernández I. A randomized, double-masked study to evaluate the effect of omega-3 fatty acids supplementation in meibomian gland dysfunction. Clin Interv Aging 2013;8:1133–1138.
[853] Kawakita T, Kawabata F, Tsuji T, Kawashima M, Shimmura S, Tsubota K. Effects of dietary supplementation with fish oil on dry eye syndrome subjects: randomized controlled trial. Biomed Res 2013;34(5):215–220.
[854] Kangari H, Eftekhari MH, Sardari S, Hashemi H, Salamzadeh J, Ghassemi-Broumand M, et al. Short-term consumption of oral omega-3 and dry eye syndrome. Ophthalmology 2013;120(11):2191–2196.
[855] Pinazo-Durán MD, Galbis-Estrada C, Pons-Vázquez S, Cantú-Dibildox J, Marco-Ramírez C, Benítez-del-Castillo J. Effects of a nutraceutical formulation based on the combination of antioxidants and ω-3 essential fatty acids in the expression of inflammation and immune response mediators in tears from patients with dry eye disorders. Clin Interv Aging 2013;8:139–148.
[856] Oleñik A. Effectiveness and tolerability of dietary supplementation with a combination of omega-3 polyunsaturated fatty acids and antioxidants in the treatment of dry eye symptoms: results of a prospective study. Clin Ophthalmol 2014;8:169–176.
[857] Bhargava R, Kumar P, Arora Y. Short-Term Omega 3 Fatty Acids Treatment for Dry Eye in Young and Middle-Aged Visual Display Terminal Users. Eye Contact Lens 2016;42(4):231–236.
[858] Deinema LA, Vingrys AJ, Wong CY, Jackson DC, Chinnery HR, Downie LE. A Randomized, Double-Masked, Placebo-Controlled Clinical Trial of Two Forms of Omega-3 Supplements for Treating Dry Eye Disease. Ophthalmology 2017;124(1):43–52.
[859] Epitropoulos AT, Donnenfeld ED, Shah ZA, Holland EJ, Gross M, Faulkner WJ, et al. Effect of Oral Re-esterified Omega-3 Nutritional Supplementation on Dry Eyes. Cornea 2016;35(9):1185–1191.
[860] Chinnery HR, Naranjo Golborne C, Downie LE. Omega-3 supplementation is neuroprotective to corneal nerves in dry eye disease: a pilot study. Ophthalmic Physiol Opt. 2017 Jul;37(4):473–481.
[861] Liu A, Ji J. Omega-3 essential fatty acids therapy for dry eye syndrome: a meta-analysis of randomized controlled studies. Med Sci Monit 2014;20:1583–1589.
[862] Buckley MS, Goff AD, Knapp WE. Fish oil interaction with warfarin. Ann Pharmacother 2004;38(1):50–52.
[863] Roncone M, Bartlett H, Eperjesi F. Essential fatty acids for dry eye: A review. Cont Lens Anter Eye 2010;33:49–54. quiz 100.
[864] Brasky TM, Darke AK, Song X, Tangen CM, Goodman PJ, Thompson IM, et al. Plasma phospholipid fatty acids and prostate cancer risk in the SELECT trial. J Natl Cancer Inst 2013;105(15):1132–1141.
[865] Brenna JT, Burdge GC, Crawford MA, Clayton P, Cunnane SC, Gow R, et al. RE: Plasma phospholipid fatty acids and prostate cancer risk in the SELECT trial. J Natl Cancer Inst 2014;106:dju015.
[866] Szymanski KM, Wheeler DC, Mucci LA. Fish consumption and prostate cancer risk: a review and meta-analysis. Am J Clin Nutr 2010;92(5):1223–1233.
[867] Manthorpe R, Hagen Petersen S, Prause JU. Primary Sjögren's syndrome treated with Efamol/Efavit. A double-blind cross-over investigation. Rheumatol Int 1984;4(4):165–167.
[868] Oxholm P, Manthorpe R, Prause JU, Horrobin D. Patients with primary Sjögren's syndrome treated for two months with evening primrose oil. Scand J Rheumatol 1986;15(2):103–108.
[869] Theander E, Horrobin DF, Jacobsson LT, Manthorpe R. Gammalinolenic acid treatment of fatigue associated with primary Sjögren's syndrome. Scand J Rheumatol 2002;31(2):72–79.
[870] Aragona P, Bucolo C, Spinella R, Giuffrida S, Ferreri G. Systemic omega-6 essential fatty acid treatment and pge1 tear content in Sjögren's syndrome patients. Invest Ophthalmol Vis Sci 2005;46(12):4474–4479.
[871] Pinna A, Piccinini P, Carta F. Effect of oral linoleic and gamma-linolenic acid on meibomian gland dysfunction. Cornea 2007;26(3):260–264.
[872] Creuzot C, Passemard M, Viau S, Joffre C, Pouliquen P, Elena PP, et al. Improvement of dry eye symptoms with polyunsaturated fatty acids. J Fr Ophtalmol 2006;29:868–873.
[873] Larmo PS, Järvinen RL, Setälä NL, Yang B, Viitanen MH, Engblom JR, et al. Oral sea buckthorn oil attenuates tear film osmolarity and symptoms in individuals with dry eye. J Nutr 2010;140(8):1462–1468.
[874] Brignole-Baudouin F, Baudouin C, Aragona P, Rolando M, Labetoulle M, Pisella PJ, et al. A multicentre, double-masked, randomized, controlled trial assessing the effect of oral supplementation of omega-3 and omega-6 fatty acids on a conjunctival inflammatory marker in dry eye patients. Acta Ophthalmol 2011;89(7):e591–e597.
[875] Jackson MA, Burrell K, Gaddie IB, Richardson SD. Efficacy of a new prescription-only medical food supplement in alleviating signs and symptoms of dry eye, with or without concomitant cyclosporine A. Clin Ophthalmol 2011;5:1201–1206.
[876] Creuzot-Garcher C, Baudouin C, Labetoulle M, Pisella PJ, Mouriaux F, Meddeb-Ouertani A, et al. Efficacy assessment of Nutrilarm(R), a per os omega-3 and omega-6 polyunsaturated essential fatty acid dietary formulation versus placebo in patients with bilateral treated moderate dry eye syndrome. J Fr Ophtalmol 2011;34:448–455.
[877] Sheppard Jr. JD, Singh R, McClellan AJ, Weikert MP, Scoper SV, Joly TJ, et al. Long-term Supplementation With n-6 and n-3 PUFAs Improves Moderate-to-Severe Keratoconjunctivitis Sicca: A Randomized Double-Blind Clinical Trial. Cornea 2013;32(10):1297–1304.
[878] Zhu W, Wu Y, Li G, Wang J, Li X. Efficacy of polyunsaturated fatty acids for dry eye syndrome: a meta-analysis of randomized controlled trials. Nutr Rev 2014;72(10):662–671.
[879] Ng SM, Lindsley K, Akpek EK. Omega-3 and omega-6 polyunsaturated fatty acids for dry eye syndrome (Protocol). Cochrane Database Syst Rev 2014;3:CD011016.
[880] Ren J, Mozurkewich EL, Sen A, Vahratian AM, Ferreri TG, Morse AN, et al. Total Serum Fatty Acid Analysis by GC-MS: Assay Validation and Serum Sample Stability. Curr Pharm Anal 2013;9(4):331–339.
[881] Danjo Y, Lee M, Horimoto K, Hamano T. Ocular surface damage and tear lactoferrin in dry eye syndrome. Acta Ophthalmol (Copenh) 1994;72(4):433–437.
[882] Boukes RJ, Boonstra A, Breebaart AC, Reits D, Glasius E, Luyendyk L, et al. Analysis of human tear protein profiles using high performance liquid chromatography (HPLC). Doc Ophthalmol 1987 Sep-Oct;67(1–2):105–113.
[883] Seal DV. The effect of ageing and disease on tear constituents. Trans Ophthalmol Soc U K 1985;104(Pt 4):355–362.
[884] Mackie IA, Seal DV. Diagnostic implications of tear protein profiles. Br J Ophthalmol 1984;68(5):321–324.
[885] Goren MB, Goren SB. Diagnostic tests in patients with symptoms of keratoconjunctivitis sicca. Am J Ophthalmol 1988;106(5):570–574.
[886] Versura P, Nanni P, Bavelloni A, Blalock WL, Piazzi M, Roda A, et al. Tear proteomics in evaporative dry eye disease. Eye (Lond) 2010;24(8):1396–1402.
[887] Kawashima M, Kawakita T, Inaba T, Okada N, Ito M, Shimmura S, et al. Dietary lactoferrin alleviates age-related lacrimal gland dysfunction in mice. PLoS One 2012;7:e33148.
[888] Dogru M, Matsumoto Y, Yamamoto Y, Goto E, Saiki M, Shimazaki J, et al. Lactoferrin in Sjögren's syndrome. Ophthalmology 2007;114(12):2366–2367.
[889] Devendra J, Singh S. Effect of Oral Lactoferrin on Cataract Surgery Induced Dry Eye: A Randomised Controlled Trial. J Clin Diagn Res 2015;9(10):NC06–NC09.
[890] Dogru M, Wakamatsu T, Kojima T, Matsumoto Y, Kawakita T, Schnider C, et al. The role of oxidative stress and inflammation in dry eye disease. Cornea 2009;28(supp1). S70–S4.
[891] Blades KJ, Patel S, Aidoo KE. Oral antioxidant therapy for marginal dry eye. Eur J Clin Nutr 2001;55(7):589–597.
[892] Drouault-Holowacz S, Bieuvelet S, Burckel A, Rigal D, Dubray C, Lichon JL, et al. Antioxidants intake and dry eye syndrome: a crossover, placebo-controlled, randomized trial. Eur J Ophthalmol 2009 May-Jun;19(3):337–342.
[893] Hitoe S, Tanaka J, Shimoda H. MaquiBright standardized maqui berry extract significantly increases tear fluid production and ameliorates dry eye-related symptoms in a clinical pilot trial. Panminerva Med 2014;56:1–6.
[894] Cakatay U. Pro-oxidant actions of alpha-lipoic acid and dihydrolipoic acid. Med Hypotheses 2006;66(1):110–117.
[895] Andrade AS, Salomon TB, Behling CS, Mahl CD, Hackenhaar FS, Putti J, et al. Alpha-lipoic acid restores tear production in an animal model of dry eye. Exp Eye Res 2014;120:1–9.
[896] Kawashima M, Tsubota K. Effect of calorie restriction on change in lacrimal gland with age. Cornea 2011;30(Suppl 1):S29–S33.
[897] Kawashima M, Nakamura S, Izuta Y, Inoue S, Tsubota K. Dietary Supplementation with a Combination of Lactoferrin, Fish Oil, and Enterococcus faecium WB2000 for Treating Dry Eye: A Rat Model and Human Clinical Study. Ocul Surf 2016;14(2):255–263.
[898] Ho KC, Jalbert I, Watt K, Golebiowski BA. Possible Association Between Dry Eye Symptoms and Body Fat: A Prospective, Cross-Sectional Preliminary Study. Eye Contact Lens 2017. In press.
[899] Kim JH, Kim JH, Nam WH, Yi K, Choi DG, Hyon JY, et al. Oral alcohol administration disturbs tear film and ocular surface. Ophthalmology 2012;119(5):965–971.
[900] Choi W, Kim JC, Kim WS, Oh HJ, Yang JM, Lee JB, et al. Clinical Effect of Antioxidant Glasses Containing Extracts of Medicinal Plants in Patients with Dry Eye Disease: A Multi-Center, Prospective, Randomized, Double-Blind, Placebo-Controlled Trial. PLoS One 2015;10:e0139761.
[901] Pisella PJ, Pouliquen P, Baudouin C. Prevalence of ocular symptoms and signs with preserved and preservative free glaucoma medication. Br J Ophthalmol 2002;86(4):418–423.
[902] Jaenen N, Baudouin C, Pouliquen P, Manni G, Figueiredo A, Zeyen T. Ocular symptoms and signs with preserved and preservative-free glaucoma medications. Eur J Ophthalmol 2007 May-Jun;17(3):341–349.
[903] Leung EW, Medeiros FA, Weinreb RN. Prevalence of ocular surface disease in glaucoma patients. J Glaucoma 2008;17(5):350–355.
[904] Erb C, Gast U, Schremmer D. German register for glaucoma patients with dry eye. I. Basic outcome with respect to dry eye. Graefes Arch Clin Exp Ophthalmol 2008;246(11):1593–1601.
[905] Fechtner RD, Godfrey DG, Budenz D, Stewart JA, Stewart WC, Jasek MC. Prevalence of ocular surface complaints in patients with glaucoma using topical intraocular pressure-lowering medications. Cornea 2010;29(6):618–621.
[906] Rossi GC, Pasinetti GM, Scudeller L, Raimondi M, Lanteri S, Bianchi PE. Risk factors to develop ocular surface disease in treated glaucoma or ocular hypertension patients. Eur J Ophthalmol 2013 May-Jun;23(3):296–302.
[907] Chen HY, Lin CL, Tsai YY, Kao CH. Association between Glaucoma Medication Usage and Dry Eye in Taiwan. Optom Vis Sci 2015;92(9):e227–e232.
[908] Iester M, Telani S, Frezzotti P, Motolese I, Figus M, Fogagnolo P, et al. Ocular surface changes in glaucomatous patients treated with and without preservatives beta-blockers. J Ocul Pharmacol Ther 2014;30(6):476–481.
[909] Ciancaglini M, Carpineto P, Agnifili L, Nubile M, Fasanella V, Lanzini M, et al. An in vivo confocal microscopy and impression cytology analysis of preserved and unpreserved levobunolol-induced conjunctival changes. Eur J Ophthalmol 2008;18:400–407.
[910] Renieri G, Führer K, Scheithe K, Lorenz K, Pfeiffer N, Thieme H. Efficacy and tolerability of preservative-free eye drops containing a fixed combination of dorzolamide and timolol in glaucoma patients. J Ocul Pharmacol Ther 2010;26(6):597–603.
[911] Uusitalo H, Chen E, Pfeiffer N, Brignole-Baudouin F, Kaarniranta K, Leino M, et al. Switching from a preserved to a preservative-free prostaglandin preparation in topical glaucoma medication. Acta Ophthalmol 2010;88(3):329–336.
[912] Freeman P David, Kahook Malik Y. Preservatives in topical ophthalmic medications: historical and clinical perspectives. Expert Rev Ophthalmol 2009;4(1):59–64.
[913] Labbé A, Pauly A, Liang H, Brignole-Baudouin F, Martin C, Warnet JM, et al. Comparison of toxicological profiles of benzalkonium chloride and polyquaternium-1: an experimental study. J Ocul Pharmacol Ther 2006;22(4):267–278.
[914] Henry JC, Peace JH, Stewart JA, Stewart WC. Efficacy, safety, and improved tolerability of travoprost BAK-free ophthalmic solution compared with prior prostaglandin therapy. Clin Ophthalmol 2008;2(3):613–621.
[915] Katz G, Springs CL, Craven ER, Montecchi-Palmer M. Ocular surface disease in patients with glaucoma or ocular hypertension treated with either BAK-preserved latanoprost or BAK-free travoprost. Clin Ophthalmol 2010;4:1253–1261.
[916] Aihara M, Oshima H, Araie M, ; group EXs.. Effects of SofZia-preserved travoprost and benzalkonium chloride-preserved latanoprost on the ocular surface – a multicentre randomized single-masked study. Acta Ophthalmol 2013;91:e7–e14.
[917] Wong J, Lan W, Ong LM, Tong L. Non-hormonal systemic medications and dry eye. Ocul Surf 2011;9(4):212–226.
[918] Yokoi N, Bron AJ, Georgiev GA. The precorneal tear film as a fluid shell: the effect of blinking and saccades on tear film distribution and dynamics. Ocul Surf 2014;12(4):252–266.
[919] Tsubota K, Nakamori K. Dry eyes and video display terminals. N Engl J Med 1993;328(8):584.
[920] Tsubota K, Nakamori K. Effects of ocular surface area and blink rate on tear dynamics. Arch Ophthalmol 1995;113(2):155–158.
[921] Uchino M, Yokoi N, Uchino Y, Dogru M, Kawashima M, Komuro A, et al. Prevalence of dry eye disease and its risk factors in visual display terminal users: the Osaka study. Am J Ophthalmol 2013;156(4):759–766.
[922] Stapleton F, Alves M, Bunya VY, Jalbert I, Lekhanont K, Malet F, et al. TFOS DEWS II Epidemiology report. Ocul Surf 2017;15:334–365.
[923] Uchino M, Schaumberg DA, Dogru M, Uchino Y, Fukagawa K, Shimmura S, et al. Prevalence of dry eye disease among Japanese visual display terminal users. Ophthalmology 2008;115(11):1982–1988.
[924] Fenga C, Aragona P, Cacciola A, Spinella R, Di Nola C, Ferreri F, et al. Meibomian gland dysfunction and ocular discomfort in video display terminal workers. Eye (Lond) 2008;22(1):91–95.
[925] Wu H, Wang Y, Dong N, Yang F, Lin Z, Shang X, et al. Meibomian gland dysfunction determines the severity of the dry eye conditions in visual display terminal workers. PLoS One 2014;9:e105575.
[926] Uchino Y, Uchino M, Yokoi N, Dogru M, Kawashima M, Okada N, et al. Alteration of tear mucin 5AC in office workers using visual display terminals: The Osaka Study. JAMA Ophthalmol 2014;132(8):985–992.
[927] Nakamura S, Shibuya M, Nakashima H, Hisamura R, Masuda N, Imagawa T, et al. Involvement of oxidative stress on corneal epithelial alterations in a blink-suppressed dry eye. Invest Ophthalmol Vis Sci 2007;48:1552–1558.
[928] Miura DL, Hazarbassanov RM, Yamasato CK, Bandeira e Silva F, Godinho CJ, Gomes JÁ. Effect of a light-emitting timer device on the blink rate of non-dry eye individuals and dry eye patients. Br J Ophthalmol 2013;97(8):965–967.
[929] Cardona G, Gómez M, Quevedo L, Gispets J. Effects of transient blur and VDT screen luminance changes on eyeblink rate. Cont Lens Anter Eye 2014;37(5):363–367.
[930] Blehm C, Vishnu S, Khattak A, Mitra S, Yee RW. Computer vision syndrome: a review. Surv Ophthalmol 2005 May-Jun;50(3):253–262.
[931] McCulley JP, Uchiyama E, Aronowicz JD, Butovich IA. Impact of evaporation on aqueous tear loss. Trans Am Ophthalmol Soc 2006;104:121–128.
[932] Abusharha AA, Pearce EI. The effect of low humidity on the human tear film. Cornea 2013;32(4):429–434.
[933] Alex A, Edwards A, Hays JD, Kerkstra M, Shih A, de Paiva CS, et al. Factors predicting the ocular surface response to desiccating environmental stress. Invest Ophthalmol Vis Sci 2013;54:3325–3332.
[934] López-Miguel A, Tesón M, Martín-Montañez V, Enríquez-de-Salamanca A, Stern ME, Calonge M, et al. Dry eye exacerbation in patients exposed to desiccating stress under controlled environmental conditions. Am J Ophthalmol 2014;157(4):788–798. e2.
[935] Lopez-Miguel A, Teson M, Martin-Montanez V, Enriquez-de-Salamanca A, Stern ME, Gonzalez-Garcia MJ, et al. Clinical and Molecular Inflammatory Response in Sjogren Syndrome-Associated Dry Eye Patients Under Desiccating Stress. Am J Ophthalmol 2016;161. 133-41 e1–2.
[936] Oh HJ, Li Z, Park SH, Yoon KC. Effect of hypotonic 0.18% sodium hyaluronate eyedrops on inflammation of the ocular surface in experimental dry eye. J Ocul Pharmacol Ther 2014;30(7):533–542.
[937] Hill-Bator A, Misiuk-Hoj?o M, Marycz K, Grzesiak J. Trehalose-based eye drops preserve viability and functionality of cultured human corneal epithelial cells during desiccation. Biomed Res Int 2014;2014:292139.
[938] Moore QL, De Paiva CS, Pflugfelder SC. Effects of Dry Eye Therapies on Environmentally Induced Ocular Surface Disease. Am J Ophthalmol 2015;160(1):135–142. e1.
[939] Dohlman TH, Chauhan SK, Kodati S, Hua J, Chen Y, Omoto M, et al. The CCR6/CCL20 axis mediates Th17 cell migration to the ocular surface in dry eye disease. Invest Ophthalmol Vis Sci 2013;54(6):4081–4091.
[940] Goyal S, Chauhan SK, Zhang Q, Dana R. Amelioration of murine dry eye disease by topical antagonist to chemokine receptor 2. Arch Ophthalmol 2009;127(7):882–887.
[941] Urashima Hiroki, Takeji Yasuhiro, Okamoto Takashi, Fujisawa Shigeki, Shinohara Hisashi. Rebamipide Increases Mucin-Like Substance Contents and Periodic Acid Schiff Reagent-Positive Cells Density in Normal Rabbits. J Ocul Pharmacol Ther 2012;28(3):264–270.
[942] Nakamura S, Shibuya M, Nakashima H, Imagawa T, Uehara M, Tsubota K. D-beta-hydroxybutyrate protects against corneal epithelial disorders in a rat dry eye model with jogging board. Invest Ophthalmol Vis Sci 2005;46:2379–2387.
[943] Hirayama M, Murat D, Liu Y, Kojima T, Kawakita T, Tsubota K. Efficacy of a novel moist cool air device in office workers with dry eye disease. Acta Ophthalmol 2013;91(8):756–762.
[944] Willis RM, Folberg R, Krachmer JH, Holland EJ. The treatment of aqueous-deficient dry eye with removable punctal plugs. A clinical and impression-cytologic study. Ophthalmology 1987;94(5):514–518.
[945] Tsubota K, Yamada M, Urayama K. Spectacle side panels and moist inserts for the treatment of dry-eye patients. Cornea 1994;13(3):197–201.
[946] Yee RW, Sperling HG, Kattek A, Paukert MT, Dawson K, Garcia M, et al. Isolation of the ocular surface to treat dysfunctional tear syndrome associated with computer use. Ocul Surf 2007;5(4):308–315.
[947] Wakamatsu TH, Dogru M, Tsubota K. Tearful relations: oxidative stress, inflammation and eye diseases. Arq Bras Oftalmol 2008 Nov-Dec;71(6 Suppl):72–79.
[948] Satici A, Bitiren M, Ozardali I, Vural H, Kilic A, Guzey M. The effects of chronic smoking on the ocular surface and tear characteristics: a clinical, histological and biochemical study. Acta Ophthalmol Scand 2003;81(6):583–587.
[949] Altinors DD, Akça S, Akova YA, Bilezikçi B, Goto E, Dogru M, et al. Smoking associated with damage to the lipid layer of the ocular surface. Am J Ophthalmol 2006;141(6):1016–1021.
[950] Thomas J, Jacob GP, Abraham L, Noushad B. The effect of smoking on the ocular surface and the precorneal tear film. Australas Med J 2012;5(4):221–226.
[951] Matsumoto Y, Dogru M, Goto E, Sasaki Y, Inoue H, Saito I, et al. Alterations of the tear film and ocular surface health in chronic smokers. Eye (Lond) 2008;22(7):961–968.
[952] Rummenie VT, Matsumoto Y, Dogru M, Wang Y, Hu Y, Ward SK, et al. Tear cytokine and ocular surface alterations following brief passive cigarette smoke exposure. Cytokine 2008;43(2):200–208.
[953] Jones L, Brennan NA, González-Méijome J, Lally J, Maldonado-Codina C, Schmidt TA, et al. The TFOS International Workshop on Contact Lens Discomfort: report of the contact lens materials, design, and care subcommittee. Invest Ophthalmol Vis Sci 2013;54(11):TFOS37–TFOS70.
[954] Efron N, Jones L, Bron AJ, Knop E, Arita R, Barabino S, et al. The TFOS International Workshop on Contact Lens Discomfort: report of the contact lens interactions with the ocular surface and adnexa subcommittee. Invest Ophthalmol Vis Sci 2013;54:TFOS98–TFOS122.
[955] Zhou WY, Li YH. A survey on treatment of dry eye by traditional chinese medicine and integrative chinese and Western medicine. Chin J Integr Med 2006;12(2):154–159.
[956] Wu GL, Pu XH, Li TY, Yu GY, Lu WW, Fan YS. Effect of yangyin yiqi huoxue recipe on immune balance of Th1/Th2 in serum and submaxillary glands of NOD mice with Sjogren's syndrome. Zhongguo Zhong Xi Yi Jie He Za Zhi 2013;33:1653–1657.
[957] Wu X, Ren C, Zhou H, Zhang L, Juan C, Yang Y. Therapeutic effect of Zeng Ye decoction on primary Sjögren's syndrome via upregulation of aquaporin1 and aquaporin5 expression levels. Mol Med Rep 2014;10(1):429–434.
[958] Luo H, Li X, Liu J, Andrew F, George L. Chinese Herbal Medicine in Treating Primary Sjögren's Syndrome: A Systematic Review of Randomized Trials. Evid Based Complement Altern Med 2012;2012:640658.
[959] Chang YH, Lin HJ, Li WC. Clinical evaluation of the traditional chinese prescription Chi-Ju-Di-Huang-Wan for dry eye. Phytother Res 2005;19(4):349–354.
[960] Hu W, Qian X, Guo F, Zhang M, Lyu C, Tao J, et al. Traditional Chinese medicine compound ShengJinRunZaoYangXue granules for treatment of primary Sjögren's syndrome: a randomized, double-blind, placebo-controlled clinical trial. Chin Med J 2014;127(15):2721–2726.
[961] Boukraa L. Additive activity of royal jelly and honey against Pseudomonas aeruginosa. Altern Med Rev 2008;13(4):330–333.
[962] Tartakovskaia AI. Apilak (royal jelly) in the therapy of trophic disorders of the cornea in eye burns. Vestn Oftalmol 1966;79:59–61.
[963] Hussein SZ, Yusoff KM, Makpol S, Yusof YA. Antioxidant capacities and total phenolic contents increase with gamma irradiation in two types of Malaysian honey. Molecules 2011;16(8):6378–6395.
[964] Lusby PE, Coombes AL, Wilkinson JM. Bactericidal activity of different honeys against pathogenic bacteria. Arch Med Res 2005 Sep-Oct;36(5):464–467.
[965] Imada T, Nakamura S, Kitamura N, Shibuya I, Tsubota K. Oral administration of royal jelly restores tear secretion capacity in rat blink-suppressed dry eye model by modulating lacrimal gland function. PLoS One 2014;9:e106338.
[966] Albietz JM, Lenton LM. Effect of antibacterial honey on the ocular flora in tear deficiency and meibomian gland disease. Cornea 2006;25(9):1012–1019.
[967] Craig JP, Rupenthal ID, Seyfoddin A, Cheung IM, Uy B, Wang MT, et al. Pre-clinical development of MGO Manuka Honey microemulsion for blephar-itis management. BMJ Open Ophth 2017;0:e000065.
[968] Craig JP, Wang MT, Ganesalingam K, Rupenthal ID, Swift S, Loh CS, et al. Randomised masked trial of the clinical safety and tolerability of MGO Manuka Honey eye cream for the management of blepharitis. BMJ Open Ophth 2017;0:e000066.
[969] Ajite KO, Fadamiro OC. Prevalence of harmful/traditional medication use in traumatic eye injury. Glob J Health Sci 2013;5(4):55–59.
[970] Prajna NV, Pillai MR, Manimegalai TK, Srinivasan M. Use of Traditional Eye Medicines by corneal ulcer patients presenting to a hospital in South India. Indian J Ophthalmol 1999;47(1):15–18.
[971] Verd S. Switch from antibiotic eye drops to instillation of mother's milk drops as a treatment of infant epiphora. J Trop Pediatr 2007;53(1):68–69.
[972] Ghaemi S, Navaei P, Rahimirad S, Behjati M, Kelishadi R. Evaluation of preventive effects of colostrum against neonatal conjunctivitis: A randomized clinical trial. J Educ Health Promot 2014;3:63.
[973] Singh M, Sugathan PS, Bhujwala RA. Human colostrum for prophylaxis against sticky eyes and conjunctivitis in the newborn. J Trop Pediatr 1982;28(1):35–37.
[974] Baynham JT, Moorman MA, Donnellan C, Cevallos V, Keenan JD. Antibacterial effect of human milk for common causes of paediatric conjunctivitis. Br J Ophthalmol 2013;97(3):377–379.
[975] Ibhanesebhor SE, Otobo ES. In vitro activity of human milk against the causative organisms of ophthalmia neonatorum in Benin City, Nigeria. J Trop Pediatr 1996;42(6):327–329.
[976] Chaumeil C, Liotet S, Kogbe O. Treatment of severe eye dryness and problematic eye lesions with enriched bovine colostrum lactoserum. Adv Exp Med Biol 1994;350:595–599.
[977] Bucolo C, Musumeci M, Salomone S, Romano GL, Leggio GM, Gagliano C, et al. Effects of Topical Fucosyl-Lactose, a Milk Oligosaccharide, on Dry Eye Model: An Example of Nutraceutical Candidate. Front Pharmacol 2015;6:280.
[978] Cheng KJ. Neurobiological mechanisms of acupuncture for some common illnesses: a clinician's perspective. J Acupunct Meridian Stud 2014;7(3):105–114.
[979] Lan W, Tong L. Acupuncture has effect on increasing tear break-up time: acupuncture for treating dry eye, a randomized placebo-controlled trial. Acta Ophthalmol 2012;90:e73.
[980] Kim TH, Kang JW, Kim KH, Kang KW, Shin MS, Jung SY, et al. Acupuncture for the treatment of dry eye: a multicenter randomised controlled trial with active comparison intervention (artificial teardrops). PLoS One 2012;7:e36638.
[981] Gong L, Sun X, Chapin WJ. Clinical curative effect of acupuncture therapy on xerophthalmia. Am J Chin Med 2010;38(4):651–659.
[982] Yang L, Yang Z, Yu H, Song H. Acupuncture therapy is more effective than artificial tears for dry eye syndrome: evidence based on a meta-analysis. Evid Based Complement Altern Med 2015;2015:143858.
[983] Lin T, Gong L, Liu X, Ma X. Fourier-domain optical coherence tomography for monitoring the lower tear meniscus in dry eye after acupuncture treatment. Evid Based Complement Altern Med 2015;2015:492150.
[984] Nepp J, Wedrich A, Akramian J, Derbolav A, Mudrich C, Ries E, et al. Dry eye treatment with acupuncture. A prospective, randomized, double-masked study. Adv Exp Med Biol 1998;438:1011–1016.
[985] Tseng KL, Liu HJ, Tso KY, Woung LC, Su YC, Lin JG. A clinical study of acupuncture and SSP (silver spike point) electro-therapy for dry eye syndrome. Am J Chin Med 2006;34(2):197–206.
[986] Shin MS, Kim JI, Lee MS, Kim KH, Choi JY, Kang KW, et al. Acupuncture for treating dry eye: a randomized placebo-controlled trial. Acta Ophthalmol 2010;88(8):e328–e333.
[987] Na KS, Han K, Park YG, Na C, Joo CK. Depression, Stress, Quality of Life, and Dry Eye Disease in Korean Women: A Population-Based Study. Cornea 2015;34(7):733–738.
[988] Kim KW, Han SB, Han ER, Woo SJ, Lee JJ, Yoon JC, et al. Association between depression and dry eye disease in an elderly population. Invest Ophthalmol Vis Sci 2011;52:7954–7958.
[989] Li M, Gong L, Sun X, Chapin WJ. Anxiety and depression in patients with dry eye syndrome. Curr Eye Res 2011;36(1):1–7.
[990] Ayaki M, Kawashima M, Negishi K, Tsubota K. High prevalence of sleep and mood disorders in dry eye patients: survey of 1,000 eye clinic visitors. Neuropsychiatr Dis Treat 2015;11:889–894.
[991] DeGargino J. Children's Health and the Environment: A Global Perspective. Geneva, Switzerland: World Health Organization; 2004.
[992] Seligman ME, Steen TA, Park N, Peterson C. Positive psychology progress: empirical validation of interventions. Am Psychol 2005 Jul-Aug;60(5):410–421.
[993] Kawashima M, Uchino M, Yokoi N, Uchino Y, Dogru M, Komuro A, et al. Associations between subjective happiness and dry eye disease: a new perspective from the Osaka study. PLoS One 2015;10:e0123299.
[994] Kawashima M, Uchino M, Yokoi N, Uchino Y, Dogru M, Komuro A, et al. The Association between Dry Eye Disease and Physical Activity as well as Sedentary Behavior: Results from the Osaka Study. J Ophthalmol 2014;2014:943786.
[995] Sano K, Kawashima M, Ito A, Inaba T, Morimoto K, Watanabe M, et al. Aerobic exercise increases tear secretion in type 2 diabetic mice. Invest Ophthalmol Vis Sci 2014;55(7):4287–4294.
[996] Begley CG, Chalmers RL, Abetz L, Venkataraman K, Mertzanis P, Caffery BA, et al. The relationship between habitual patient-reported symptoms and clinical signs among patients with dry eye of varying severity. Invest Ophthalmol Vis Sci 2003;44(11):4753–4761.
[997] Schein OD, Tielsch JM, Munõz B, Bandeen-Roche K, West S. Relation between signs and symptoms of dry eye in the elderly. A population-based perspective. Ophthalmology 1997;104(9):1395–1401.
[998] Nichols KK, Nichols JJ, Mitchell GL. The lack of association between signs and symptoms in patients with dry eye disease. Cornea 2004;23(8):762–770.
[999] Savini G, Prabhawasat P, Kojima T, Grueterich M, Espana E, Goto E. The challenge of dry eye diagnosis. Clin Ophthalmol 2008;2(1):31–55.
[1000] Adatia FA, Michaeli-Cohen A, Naor J, Caffery B, Bookman A, Slomovic A. Correlation between corneal sensitivity, subjective dry eye symptoms and corneal staining in Sjögren's syndrome. Can J Ophthalmol 2004;39(7):767–771.
[1001] Bourcier T, Acosta MC, Borderie V, Borrás F, Gallar J, Bury T, et al. Decreased corneal sensitivity in patients with dry eye. Invest Ophthalmol Vis Sci 2005;46(7):2341–2345.
[1002] Baudouin C, Aragona P, Van Setten G, Rolando M, Irkeç M, Benítez del Castillo J, et al. Diagnosing the severity of dry eye: a clear and practical algorithm. Br J Ophthalmol 2014;98(9):1168–1176.
Tabla 1
Esquema de clasificación de las evidencias de investigación.
|
Estudios clínicos
|
|
Nivel 1
|
Evidencia obtenida de al menos un ensayo controlado, aleatorizado, bien diseñado y realizado debidamente, o evidencia de estudios bien diseñados que aplican enfoques estadísticos rigurosos
|
|
Nivel 2
|
Evidencia obtenida de uno de los siguientes: un ensayo controlado y bien diseñado sin aleatorización, un estudio analítico de casos y controles o de cohortes bien diseñado, preferiblemente de uno o varios centros, o un estudio bien diseñado accesible para análisis estadísiticos más rigurosos
|
|
Nivel 3
|
Evidencia obtenida de uno de los siguientes: estudios descriptivos, informes de casos, informes de comités de expertos, opinión de expertos
|
|
Estudios de investigación fundamental
|
|
Nivel 1
|
Estudios bien realizados que confirman una hipótesis con controles adecuados publicados en una publicación de gran impacto
|
|
Nivel 2
|
Estudio preliminar o publicado con limitaciones
|
|
Nivel 3
|
Resúmenes de reuniones o presentaciones no publicadas
|
Tabla 2
Estudios comparativos que investigan los colirios lubricantes y los sprays liposomales para la gestión de la enfermedad del ojo seco.
|
Autor, año
|
N
|
Periodo del estudio
|
Grupos de tratamiento
|
|
Parámetros con mejoras significativas
|
Parámetros sin efecto significativo
|
|
Korb et al., 2005 [141]
|
40
|
15 min
|
Soothea, Systane
|
|
LLT mejorada con ambos colirios. (Soothea 107 %; Systane 16 %)
|
Ninguno
|
|
Scaf?di & Korb, 2007 [142]
|
41
|
15 min
|
Gotas del tratamiento Refresh para el ojo seco; Gotas de Soothea
|
|
Mejora del GCL con ambos colirios;
Soothea > aumento que el tratamiento Refresh para el ojo seco
|
N/D
|
|
Wang et al., 2007 [177]
|
67
|
4 semanas
|
Fórmulas de lágrimas artificiales basadas en carbómero, celulosa y aceite mineral
|
|
Mejoraron las puntuaciones totales, los síntomas, los signos y la prueba de Schirmer. Los síntomas mejoraron con la fórmula basada en carbómero.
|
Ninguno
|
|
Craig et al., 2010 [178]
|
22
|
30, 60, 90, 135 min
|
Spray liposomal Tears Again (Optrex ActiMist)
Control: spray salino
|
|
GCL, estabilidad de la película lagrimal, TDNI, confort.
|
AML
|
|
Wang et al., 2010 [179]
|
30
|
4 semanas
|
Gel con contenido lipídico basado en carbómero (CLBC), gel de guar-HP
|
|
Tanto la puntuación de Schimer como la evaluación subjetiva del paciente mejoraron. CLBC > guar-HP.
Los TDL mejoraron igualmente con ambos IESO, el TDNI mejoró en ambos con AM
|
Ninguno
|
|
Pult et al., 2012 [180]
|
80
|
10 min
|
Optrex ActiMist (AM), DryEyesMist (DEM), TearMist (TM)
|
|
DEM y TM redujeron el confort y el TDNI
|
|
Tomlinson et al., 2013 [65]
|
37
|
2 semanas
|
Carmelosa sódica, carmelosa sódica con lípidos, gotas de glicerina con lípidos
|
|
Evaporación, TDL, osmolaridad, síntomas. La tasas de evaporación de lípidos mejoró con las gotas con lipídicas en comparación con las no lipídicas. La carmelosa sódica con lípidos fue superior a los demás.
|
Ninguno
|
|
Mutalib et al., 2015 [181]
|
9
(conejos)
|
2 semanas
|
Aceite de coco Virgin, Tears Naturale II, Salino
Control: ojo contralateral
|
|
Ninguno
|
TDNI
enrojecimiento, tinción corneal, pH, Schirmer
|
|
Simmons et al., 2015 [182]
|
256
|
3 meses
|
- gotas lipídicas comercializadas,
- gotas lipídicas no comercializadas
|
|
Síntomas, IESO, TDL
|
Tinción corneal, tinción de la conjuntiva, glándulas de Meibomio, Schirmer
|
|
GCL = grosor de la capa lipídica, N = número de sujetos; TDNI = tiempo de desintegración no invasiva; IESO = índice de enfermedad de la superficie ocular; TDL = tiempo de desintegración lagrimal.
a La fórmula Soothe utilizada en estos estudios se comercializa hoy en día como Soothe XP.
|
Tabla 3
Estudios clínicos que investigan el uso del suero autólogo para la gestión de la enfermedad del ojo seco.
|
Autor
|
Nivel de evidencia
|
N
|
Indicación
|
Seguimiento
|
% de suero y diluyente
|
Controles
|
Mejorado
|
Sin mejora
|
|
Noble et al., 2004 [213]
|
ECA (Nivel 1)
|
16
|
SS y QCS
|
3 M
|
50 % (0,9 NaCl)
|
Cruzado: Lubricantes
|
Síntomas, DCC
|
|
|
Kojima et al., 2005 [214]
|
ECA (Nivel 1)
|
10
|
SS y no SS de acuerdo con el GOS Jap
|
2 S
|
20 % (0,9 % NaCl)
|
LA sinc
|
Síntomas, TDL, TCF
|
Puntuación de Schirmer
|
|
Noda-Tsuruya et al., 2006 [215]
|
ECA (Nivel 1)
|
12
|
LASIK
|
6 M
|
20 % (0,9 % NaCl)
|
LA
|
TDL, TCF
|
Síntomas, puntuación de Schirmer
|
|
Yoon et al., 2007 [216]
|
ECA (Nivel 1)
|
41
|
SS, no SS
|
2 M
|
20 % (0,9 NaCl)
|
Suero del cordón umbilical
|
Síntomas, TDL, TCF, DCC; Mejores síntomas, TCF (a los 2 M)
|
Puntuación de Schirmer, sensibilidad corneal, aclaramiento lagrimal
|
|
Urzua et al., 2012 [217]
|
ECA (Nivel 1)
|
12
|
No SS grave según los criterios DEWS
|
2 S (cruce después de un reposo farmacológico de 7 días)
|
20 % SA
|
LA
|
Síntomas (IESO)
|
Tinción con fluoresceína, TDL
|
|
Celebi et al., 2014 [218]
|
ECA con doble enmascaramiento (Nivel 1)
|
20
|
Schirmer <5 mm, TDL <5 s, IESO >40, TCF ≥1
|
1 M
|
20 % (0,9 % NaCl)
|
Cruce, Refresh sinc
|
Síntomas, TDL
|
Puntuación de Schirmer, TCF
|
|
Hussain et al., 2014 [219]
|
Revisión retrospectiva de la gráfica
|
63
|
Cualquier paciente que usase LA entre junio de 2008 y enero de 2013 durante al menos 3 meses
|
Hasta 48 M
|
50 % (0,9 % NaCl)
|
Ninguno
|
Puntuación de Schirmer, IESO, TCF
|
|
|
Hwang et al., 2014 [186]
|
Comparación de cohortes (Nivel 2)
|
20
|
1.° SS*
|
1 M
|
50 %
|
2.° SS*
|
1.° SS*: Síntoma, TCF, TDL
|
2.° SS*, posiblemente debido a un aumento de los niveles de citocinas proinflamatorias
|
|
Jirsova et al., 2014 [220]
|
Intervencionista (Nivel 2)
|
17
|
Schirmer I <5 mm/5 min;
TDIL <5 s; síntomas graves definidos según DEWS
|
3 M
|
20 %
|
Ninguno
|
Puntuación de Schirmer, varios síntomas, TCF, citología de impresión
|
TDL, AML, sequedad, molestias
|
|
Lopez-Garcia et al., 2014 [221]
|
ECA (Nivel 1)
|
26
|
SS
|
2 M
|
20 % (0,9 NaCl)
|
SA diluido al 20 % con AH en ojo contralateral
|
Mejora de síntomas, TDL, TCF, DCC en ambos, pero mejor en AH-SA
|
Puntuación de Schirmer, AV
|
|
Semeraro et al., 2014 [184]
|
Comparación de cohortes (Nivel 2)
|
26
|
ESO aguda (ojo seco, queratitis neurotrópica, erosión recurrente)
|
16-31 S
|
50 % (0,9 % NaCl)
|
ESO crónica
|
Todos los defectos epiteliales curados
|
Recurrencia del 18 % en ESO crónica tras el cese del SA
|
|
Aggarwal et al., 2015 [222]
|
Intervencionista (Nivel 2)
|
16
|
Foto-alodinia (excluidos aquellos con ESO)
|
3 M
|
20 % SA
|
Ninguno
|
Densidad y morfología subbasales de los nervios corneales, síntomas de fotofobia
|
Densidad DCC
|
|
Li et al., 2015 [223]
|
ECA (Nivel 1)
|
18
|
SS
Schirmer <5 mm, TDL <5s, TCF >5
|
6 S
|
50 % (0,9 BSS)
|
Lentes de contacto de hidrogel de silicona
|
Síntomas, TDL, TCF, pero los síntomas y la TCF fueron mejores en el grupo control
|
Puntuación de Schirmer, AVMC
|
|
Mukhopadhyay et al., 2015 [224]
|
ECA (Nivel 1)
|
52
|
Schirmer <5 mm
|
18 S - 6 en tratamiento y 12 sin tratamiento)
|
20 % (0,9 % NaCl)
|
(1) LA (2) suero de la sangre del cordón
|
Síntomas, TDL, TCF
|
Puntuación de Schirmer
|
1.°/2.° = primario/secundario (*clasificación histórica); 2 M = 2 meses; SA = suero autólogo; LA = lágrimas artificiales; TCF = tinción corneal con ?uoresceína; LC = lentes de contacto; DCC = densidad de las células calciformes; GVHD = enfermedad de injerto contra huésped (Graft versus host disease); AH = ácido hialurónico; QCS = queratoconjuntivitis seca; GOS Jap = grupo de ojo seco japones; LASIK = queratomileuisis in situ asistida con láser (laser in-situ keratomileusis); M = meses; N = número de sujetos tratados con suero; NaCl = salino; ESO = enfermedad de la superficie ocular; IESO = índice de enfermedad de la superficie ocular; Oxford = puntuación de epiteliopatía punteada; ECA = ensayo controlado aleatorizado; s = segundos; SS = síndrome de Sjögren; TDL = tiempo de desintegración lagrimal; sinc = sin conservantes; AV = agudeza visual; S = semanas.
Tabla 4
Estudios de Nivel 2 de oclusión del conducto lagrimal en la enfermedad del ojo seco.
|
Autor
|
Grupo de sujetos
|
N
|
Duración del tratamiento (meses)
|
Beneficios notificados
|
Comentarios
|
|
Balaram et al., 2001 [283]
|
Ojo seco con tapón
|
50
|
6
|
Mejora de los síntomas
|
37 % de pérdida de tapón; es más probable perder tapones insertados en los puntos lagrimales superiores
|
|
Kojima et al., 2002 [308]
|
Ojo seco con tapón de silicona
|
51
|
21
|
Mejora de los síntomas, daño epitelial
|
55,9 % de pérdida de tapón
|
|
Nava-Castaneda et al., 2003 [309]
|
Ojo seco con tapón de colágeno y silicona
|
61
|
2
|
Mejora de los síntomas, tinción vital
|
|
|
Farrell et al., 2003 [310]
|
Ojo seco con tapón de colágeno
|
62
|
0,3
|
Mejora de los síntomas, función lagrimal
|
Beneficio de ocluir solo los puntos lagrimales inferiores
|
|
Altan-Yaycioglu et al., 2005 [311]
|
Ojo seco con tapón de colágeno y silicona
|
24
|
|
Mejora de la función lagrimal
|
Resultados similares con ambos tipos
|
|
Miyata et al., 2006 [272]
|
Ojo seco con tapón de atelocolágeno
|
28
|
2
|
Mejora de la función lagrimal, tinción vital, TDL, puntuación Schirmer
|
|
|
Chen et al., 2007 [312]
|
Ojo seco con tapón Smart
|
54
|
13
|
Mejora de los síntomas, tinción vital
|
|
|
Hirai et al., 2012 [270]
|
Ojo seco con tapón de atelocolágeno
|
37
|
2
|
Mejora de los síntomas, estado de la superficie ocular
|
|
|
Yung et al., 2012 [257]
|
Ojo seco con tapón después de LASIK
|
18
|
3
|
Mejora de los síntomas, función lagrimal
|
|
|
Kaido et al., 2012 [252]
|
TDL corto en pacientes con tapón
|
43
|
1
|
Mejora de los síntomas, función lagrimal, tinción vital
|
|
|
Shi et al., 2013 [313]
|
Ojo seco con tapón de silicona
|
65
|
6
|
Mejora de los síntomas, tinción corneal, TDL y puntuación Schirmer
|
|
|
Capita et al., 2015 [274]
|
Ojo seco SS con oclusión con hipromelosa
|
38
|
2
|
Mejora de los síntomas, tinción corneal y puntuación Schirmer
|
|
|
Tong et al., 2016 [263]
|
Ojo seco moderado con tapón lagrimal
|
29
|
0,75
|
Mejora de los síntomas, tinción corneal
|
Sin cambios en las citocinas lagrimales
|
|
LASIK = queratomileusis in situ asistida con láser (laser in-situ keratomileusis); N = número de sujetos; SS = síndrome de Sjögren; TDL = tiempo de desintegración lagrimal.
|
Tabla 5
Estudios de nivel 2 sobre la higiene del párpado en la enfermedad del ojo seco.
|
Autor
|
Grupo de sujetos
|
N
|
Variaciones en la higiene del párpado
|
Duración del tratamiento (meses)
|
Beneficios notificados
|
|
Paugh et al., 1990 [394]
|
DGM
|
21
|
Frotado + masaje del párpado
|
0,5
|
Mejora del TDL
|
|
Key et al., 1996 [386]
|
Blefaritis crónica (el 80 % usaba LC)
|
25
|
Frote del párpado vs. jabón hipoalergénico en pastilla
|
4
|
Mejora de los síntomas y apariencia del párpado
|
|
Romero et al., 2004 [387]
|
DGM
|
37
|
Higiene del párpado + salino calentado + LA
|
1,5
|
Mejora de los síntomas y TDL
|
|
Guillon et al., 2012 [395]
|
Blefaritis y DGM
|
40
|
Higiene del párpado con toallitas (Blephaclean)
|
3
|
Mejora del estado del margen del párpado
|
|
Guillon et al., 2012 [396]
|
Blefaritis y DGM
|
40
|
Higiene del párpado con toallitas (Blephaclean)
|
3
|
Mejora de los síntomas
|
|
Doan et al., 2012 [397]
|
Blefaritis crónica
|
33
|
Higiene del párpado con solución limpiadora (Blephagel)
|
0,75
|
Sin cambios en el TDL y la AV; la rutina se toleró bien
|
|
Khaireddin et al., 2013 [398]
|
Blefaritis crónica y uso de lentes de contacto
|
53
|
Higiene del párpado (champú para bebés)
|
1
|
Mejora de los síntomas
|
|
Arrua et al., 2015 [399]
|
Blefaritis crónica
|
45
|
Higiene del párpado con champú neutro
|
2
|
Mejora de síntomas y signos
|
|
Ngo et al., 2017 [400]
|
EOS
|
20
|
Combinación de LA, limpiador de párpados (TheraTears SteriLid) y suplementos orales de omega-3 (TheraTears Nutrition)
|
3
|
Mejora de síntomas y signos
|
|
LA = lágrima artificial; LC = lentes de contacto; DGM = disfunción de la glándula de Meibomio; N = número de sujetos; TDL = tiempo de desintegración lagrimal; AV = agudeza visual.
|
Tabla 6
Estudios de nivel 2 relacionados con la gestión de Demodex y la enfermedad del ojo seco.
|
Autor
|
Grupo de sujetos
|
N
|
Variaciones en el tratamiento
|
Duración del tratamiento (meses)
|
Beneficios notificados
|
|
Kheirkhah et al., 2007 [409]
|
Blefaritis crónica con Demodex ocular
|
6
|
AAT al 50 % para frotado semanal del párpado + uso diario
champú de AT
|
2
|
Reducción del recuento de Demodex, mejora de la irritación ocular y de los signos inflamatorios corneales
|
|
Gao et al., 2007 [410]
|
Demodex ocular
|
11
|
AAT al 50 % para frotado semanal del párpado + uso diario
champú de AT
|
1
|
Reducción del recuento de Demodex
|
|
Holzchuh et al., 2011 [411]
|
Blefaritis resistente con Demodex ocular
|
12
|
Ivermectina ocular
|
1
|
Reducción del recuento de Demodex, mejora de las
funciones lagrimales
|
|
Filho et al., 2011 [412]
|
Blefaritis crónica con Demodex ocular
|
19
|
Ivermectina ocular
|
3
|
Reducción del recuento de Demodex
|
|
Koo et al., 2012 [413]
|
Demodex ocular
|
106
|
Frotado diario del párpado con AAT
|
1
|
Reducción del recuento de Demodex,
mejora del
confort ocular
|
|
Gao et al., 2012 [414]
|
Demodex ocular
|
24
|
Masaje con pomada de AAT al 5 %
|
1
|
Reducción del recuento de Demodex,
mejora del
picor ocular
|
|
Salem et al., 2013 [415]
|
Demodex ocular/dérmico
|
30
|
Ivermectina oral vs.
ivermectina + metronidazol
|
1
|
Reducción del recuento de Demodex
|
|
N = número de sujetos; AT = árbol del té; AAT = aceite de árbol del té.
|
Tabla 7
Estudios de colirios con lípidos en la enfermedad del ojo seco.
|
Autor
|
Nivel de evidencia
|
Grupo de pacientes
|
N
|
Duración del tratamiento
|
Beneficios notificados
|
Comentarios
|
|
Korb et al., 2005 [141]
|
2
|
EOS de leve a grave
|
40
|
Una única gota de cada tipo
|
Aumento del GCL emulsión > colirio acuoso
|
Prueba 1 = emulsión de aceite en agua, Prueba 2 = colirio acuoso
|
|
Scaf?di et al., 2007 [142]
|
2
|
EOS de leve a grave
|
41
|
Una única gota de cada tipo
|
Aumento del GCL
|
Pruebas 1 y 2 = dos emulsiones de aceite en agua
|
|
Maissa et al., 2010 [157]
|
3
|
10 EOS, 5 normales
|
15
|
Una sola gota
|
Mejora de los síntomas, aceite de ricino detectado hasta 4 horas después de la instilación del colirio
|
Prueba = emulsión de aceite en agua
|
|
McCann et al., 2012 [422]
|
1
|
OSE de leve a moderada
|
75
|
90 días
|
Mejora de los síntomas, evaporación, aumento de la capa lipídica y TDL emulsión > hialuronato sódico, reducción de la tinción corneal y de la osmolaridad con la emulsión
|
Prueba 1 = colirio acuoso con hialuronato sódico, Prueba 2 = colirio acuoso con HMPC, Prueba 3 = emulsión de aceite en agua
|
|
Tomlinson et al., 2013 [65]
|
1
|
EOS de leve a moderada, controles emparejados por edad y sexo
|
38
|
2 semanas
|
IESO, evaporimetría, TDL y osmolaridad mejorados
|
Prueba 1 = colirio acuoso,
Pruebas 2 y 3 = dos emulsiones de aceite en agua
|
|
Sindt et al., 2013 [423]
|
2
|
DGM de leve a moderada
|
49
|
4 semanas
|
Mejora de síntomas, tinción corneal, TDL y expresión de Meibomio
|
Prueba = emulsión de aceite en agua
|
|
Aguilar et al., 2014 [424]
|
1
|
OSE de leve a moderada
|
49
|
4 semanas
|
Mejora de TDL, tinción corneal, tinción conjuntiva y expresión de Meibomio
|
Prueba = emulsión de aceite en agua, control = cloruro sódico
|
|
Kaercher et al., 2014 [425]
|
3
|
OSDAde leve a grave, OSE y EOS mixta
|
1209
|
4 semanas
|
Mejora de síntomas, IESO,
TDL y puntuación de Schirmer, disminución de la gravedad del ojo seco
|
Prueba = emulsión de aceite en agua
|
|
Guthrie et al., 2015 [426]
|
1
|
Usuarios de lentes de contacto sintomáticos
|
106
|
1 mes
|
Mejora del confort, tiempo de uso, epiteliopatía del párpado en limpiaparabrisas, tinción corneal
emulsión > gotas de control
|
Prueba = emulsión de aceite en agua,
control = gotas para lentes de contacto con contenido no lipídico
|
|
Simmons et al., 2015 [182]
|
1
|
EOS de leve a moderada (2 con SS)
|
288
|
3 meses
|
Mejora de síntomas subjetivos de sequedad, IESO, TDL
|
Prueba 1, 2, 3 = tres emulsiones de aceite en agua
|
|
Ousler et al., 2015 [427]
|
2
|
EOS de moderada a grave
|
42
|
2 semanas
|
Mejora de síntomas, tinción corneal, tinción de la conjuntiva y enrojecimiento de la conjuntiva
|
Prueba = emulsión de aceite en agua
|
|
OSDA= ojo seco con deficiencia acuosa; EOS = enfermedad de ojo seco; OSE = ojo seco evaporativo; HPMC = hidroxipropilmetilcelulosa; GCL = grosor de la capa lipídica; DGM = disfunción de la glándula de Meibomio; N = número de sujetos; IESO = índice de enfermedad de la superficie ocular; SS = síndrome de Sjögren; TDL = tiempo de desintegración lagrimal.
|
Tabla 8
Estudios de Nivel 1 y 2 de corticosteroides tópicos para la gestión de la enfermedad del ojo seco.
|
Autor
|
Grupo de sujetos/Fármaco
|
N
|
Duración del tratamiento
|
Beneficios notificados
|
Comentarios
|
|
Marsh & P?ugfelder, 1999 [547]
|
SS. Metilprednisolona no conservada al 1 %
|
21
|
2 semanas
|
Mejora de los síntomas, tinción corneal, queratitis filamentaria
|
Series de casos retrospectivos. El tratamiento prolongado durante un máximo de 6 meses provocó un aumento de la PIO y las cataratas
|
|
Sainz de la Maza Serra et al., 2000 [548]
|
SS. Metilprednisolona no conservada al 1 %
|
15
|
2 meses
|
Mejora de los síntomas, tinción corneal
|
Prospectivo. 15 sujetos tratados con tapones lagrimales después del corticosteroide.
Otros 15 sujetos también tratados solo con tapones lagrimales.
|
|
Avunduk et al., 2003 [549]
|
QCS con o sin SS. 3 grupos: Solo SLA; SLA más AINE (?urbiprofeno); SLA más corticosteroide tópico (FML al 0,1 %)
|
32
|
1 mes
|
En el grupo de SLA más corticosteroide habían mejorado los síntomas, se había reducido la TCF y había aumentado la tinción rosa de bengala, había mejorado la presencia de células calciformes y se habían reducido las células inflamatorias
|
ECA prospectivo, con enmascaramiento simple
|
|
P?ugfelder et al., 2004 [550]
|
QCS. Loteprednol etabonato al 0,5 % vs vehículo
|
64
|
1 mes
|
Mejora de los síntomas y la hiperemia en sujetos más graves
|
EAC prospectivo, con doble enmascaramiento y controlado con placebo. Sin aumento de la PIO con respecto al placebo
|
|
Lee et al., 2006 [551]
|
QCS. Gotas de prednisolona al 0,1 % en un ojo y gotas de AH al 0,1 % en el otro
|
41
|
1 mes
|
Mejora de los síntomas, de los niveles de NGF y de las puntuaciones de la citología de impresión solo en ojos tratados con prednisolona
|
ECA prospectivo con doble enmascaramiento
|
|
Yang et al., 2006 [552]
|
QCS. FML al 0,1 %
|
30
|
1 mes
|
Mejora de los síntomas, TCF, puntuación Schirmer, tiempo de lagrimal, hiperemia conjuntival
|
Prospectivo, no enmascarado
|
|
Jonisch et al., 2010 [553]
|
ESO. Dexametasona al 0,01 % (sin conservante)
|
31
|
3 meses
|
El 65 % informó de una resolución de moderada a completa de los síntomas, mientras que el 22 % tuvo una mejora leve y el 13 % no tuvieron cambios en los síntomas. Sin elevación relevante de la PIO.
|
Revisión retrospectiva de la gráfica
|
|
Sheppard et al., 2014 [554]
|
EOS de leve a moderada. El loteprednol etabonato (LE) o la SLA antes del inicio del tratamiento con ciclosporina A (CsA) tópica
|
61
|
6 semanas
|
El pretratamiento con LE redujo de forma significativa el escozor de la CsA. Ambos grupos mostraron una mejora significativa en las puntuaciones del IESO, que fue superior con LE. Ambas estrategias de pretratamiento mejoraron los síntomas, las puntuaciones Schirmer, la TCF, la tinción con lisamina y el uso complementario con SLA.
|
Prospectivo, multicéntrico, aleatorizado, con doble enmascaramiento y de grupos paralelos
|
|
Kheirkhah et al., 2015 [555]
|
QCS debido a DGM. 3 grupos: Solo SLA; loteprednol etabonato al 0,5 %; loteprednol etabonato al 0,5 % + tobramicina al 0,3 %
|
60
|
1 mes
|
Los sujetos tratados con SLA o loteprednol solo con fibra nerviosa subbasal inicial cerca de lo normal demostraron una mejora significativa de los síntomas y la TCF
|
ECA prospectivo con doble enmascaramiento
|
|
Lin & Gong, 2015 [556]
|
SS. FML al 0,1 % y AH al 0,1 % vs. CsA al 0,5 % y AH al 0,1 %
|
40
|
2 meses
|
Mejora de los síntomas, TCF, hiperemia conjuntival, DCC, TDL (FML > CsA)
|
ECA prospectivo, de grupos paralelos
|
|
Pinto-Fraga et al., 2016 [557]
|
QCS. FML al 0,1 % vs SLA APV
|
41
|
21 días
|
Los sujetos tratados con FML mantuvieron el estado de la superficie ocular tras la exposición al entorno adverso; aquellos tratados con lentes de lágrimas de APV tuvieron una disfunción notable en la tinción corneal y de la conjuntiva, así como hiperemia
|
EAC prospectivo, con doble enmascaramiento y controlado con placebo. Incluidas 2 horas de exposición a un entorno adverso
|
|
SLA = solución de lágrima artificial; RCF = tinción de la córnea con ?uoresceína; CsA = ciclosporina A; FML = ?uorometolona; DCC = densidad de células calciformes; AH = ácido hialurónico; PIO = presión intraocular; QCS = queratoconjuntivitis seca; DGM = disfunción de la glándula de Meibomio; N = número de sujetos; NGF = factor de crecimiento nervioso (nerve growth factor); AINE = colirio antiinflamatorio no esteroideo; EOS = enfermedad de la superficie ocular; IESO = índice de enfermedad de la superficie ocular; APV = alcohol polivinilo; SS = síndrome de Sjögren; TDL = tiempo de desintegración lagrimal.
|
Tabla 9
Estudios de nivel 1 y nivel 2 de ciclosporina tópica para la gestión de la enfermedad del ojo seco.
|
Autor
|
Grupo de sujetos
|
N
|
Duración del tratamiento (meses)
|
Beneficios notificados
|
Comentarios
|
|
Estudios de nivel 1
|
|
|
|
|
|
|
Baiza-Duran et al., 2010 [588]
|
EOS de moderada a grave (hispanos)
|
183
|
3,5
|
Mejora de sequedad, lagrimeo, SCE, TDL, tinción corneal y puntuación Schirmer
|
Solución acuosa al 0,1 % y al 0,05 %
|
|
Chen et al., 2010 [589]
|
EOS de moderada a grave (chinos)
|
233
|
2
|
Mejora de la sequedad, SCE, tinción corneal y puntuación Schirmer
|
Formulación de emulsión con CAB
|
|
Su et al., 2011 [590]
|
EOS de leve a grave
|
100
|
6
|
Mejora de IESO, TDL, tinción corneal, tinción conjuntival y puntuación Schirmer
|
Posología una vez al día vs. dos veces al día
|
|
Deveci et al., 2014 [591]
|
SS
|
26
|
1
|
Mejora del dolor, quemazón, TDL y puntuación Schirmer
|
|
|
Level 2 studies
|
|
|
|
|
|
|
Salib et al., 2006 [592]
|
EOS después de LASIK
|
42
|
3
|
Mejora de la puntuación Schirmer
|
|
|
Perry et al., 2008 [593]
|
EOS leve, moderada y grave
|
158
|
3
|
Mejora de IESO, TDL, puntuación Schirmer, tinción corneal y tinción conjuntival
|
|
|
CAB = cloruro de benzalconio; ESO = enfermedad del ojo seco; SCE = sensación de cuerpo extraño; LASIK = queratomileuisis in situ asistida con láser (laser in-situ keratomileusis); N = número de sujetos; IESO = índice de enfermedad de la superficie ocular; SS = síndrome de Sjögren; TDL = tiempo de desintegración lagrimal.
|
Tabla 10
Metanálisis publicados de la ciclosporina tópica para la gestión de la enfermedad de ojo seco.
|
Autor
|
N.º revisado/N.º total de pac.
|
Beneficio con respecto a síntomas
|
Beneficios con respecto a signos
|
Comentarios
|
|
Alves et al., 2013 [594]
|
6 estudios/1514
|
En todos los estudios
|
En todos los estudios
|
|
|
Sacchetti et al., 2014 [595]
|
18 estudios/2479
|
Mejora de los síntomas en el 100 % de los estudios,
|
Mejora de la puntuación Schirmer en el 72 %, tinción corneal en el 53 %, TDL en el 47 %
|
Gran heterogeneidad en las escalas de clasificación, duración del tratamiento
|
|
Zhou et al., 2014 [596]
|
12 estudios/1660
|
Mejora de la IESO
|
Mejora de la puntuación Schirmer con anestesia, TDL
|
|
|
Wan et al., 2015 [597]
|
12 estudios/1367
|
|
Mejora de IESO, TDL, tinción corneal, puntuación Schirmer sin anestesia, DCC
|
|
|
EOS = enfermedad del ojo seco; DCC = densidad de células calciformes; TDL = tiempo de desintegración lagrimal; IESO = índice de enfermedad de la superficie ocular.
|
Tabla 11
Estudios de nivel 1 del tratamiento de coclosporina tópica para la gestión del ojo seco evaporativo/disfunción de la glándula de Meibomio.
|
Autor
|
N
|
Duración del tratamiento (meses)
|
Beneficio con respecto a síntomas
|
Beneficios con respecto a signos
|
|
Perry et al., 2006 [599]
|
33
|
3
|
|
Inflamación del párpado, inclusiones de la GM
|
|
Rubin et al., 2006 [600]
|
30
|
3
|
Visión borrosa, quemazón, picor
|
Puntuación Schirmer, TDL, calidad de la secreción
|
|
Schechter et al., 2009 [601]
|
37
|
3
|
IESO
|
TDL, puntuación Schirmer, tinción corneal
|
|
Prabhasawat et al., 2013 [602]
|
70
|
3
|
IESO
|
TDL, inflamación del párpado, expresabilidad de la GM
|
|
GM = glándula de Meibomio; N = número de sujetos; IESO = índice de enfermedad de la superficie ocular; TDL = tiempo de desintegración lagrimal.
|
Tabla 12
Estudios de Nivel 1, 2 y 3 de azitromicina para la gestión de la enfermedad del ojo seco.
|
Autor
|
Grupo de sujetos
|
N
|
Variaciones en el tratamiento
|
Duración del tratamiento (meses)
|
Beneficios notificados
|
|
Luchs et al., 2008 [730]
|
Blefaritis
|
21
|
Tópico al 1 %
|
0,5
|
Mejora de síntomas y signos
|
|
Haque et al., 2010 [731]
|
Blefaritis grave
|
26
|
Tópico al 1 %
|
1
|
Mejora de síntomas y signos
|
|
Igami et al., 2011 [720]
|
Blefaritis grave
|
13
|
Oral 500 mg/día durante 3 días en 3 ciclos con intervalos de 7 días
|
1,8
|
Mejora de los síntomas y signos y de la función lagrimal
|
|
Optiz et al., 2011 [732]
|
Blefaritis
|
33
|
Tópico al 1 %
|
1
|
Mejora de síntomas y signos
|
|
Nichols et al., 2012 [733]
|
Ojo seco con lentes de contacto
|
50
|
Tópico al 1 %
|
1
|
Mejora de síntomas y signos
|
|
Fadlallah et al., 2012 [734]
|
Blefaritis grave
|
67
|
Tópico al 1,5 %
|
3
|
Mejora de síntomas y signos
|
|
Hosseini et al., 2016 [735]
|
Blefaritis
|
907
|
Dexametasona tópica al 0,1 %; azitromicina tópica al 1 %; combinación de ambos; vehículo
|
0,5
|
Mejora de los síntomas y signos en los grupos de combinación y de dexametasona al 0,1 %
|
|
|
Tabla 13
Principales ensayos clínicos de intervención publicados de suplementación oral con AGE ω-3 para la enfermedad del ojo seco.
|
Autor, año
|
N
|
Periodo del estudio
|
Intervención ω-3 oral (dosis diaria)
|
Control
|
Nivel de evidencia
|
Parámetros con mejoras significativas con respecto al controlg
|
Parámetros sin efecto significativo con respecto al controlg
|
|
Macsai, 2008 [849].
|
38f
|
12 meses
|
Aceite de linaza 3300 mg
|
Placebo (aceite de oliva)
|
1
|
Principal: Síntomas (IESO)
|
Secundario: TDL, puntuaciones de meibum, puntuación Schirmer, tinción corneal.
|
|
Wojtowicz et al., 2011 [850]
|
36
|
90 días
|
EPA 450 mg + DHA 300 mg + aceite de linaza 100 mg
|
Placebo (aceite de germen de trigo)
|
1e
|
Síntomas (IESO)
|
Puntuación de Schirmer, evaporimetría, composición lipídica de secreciones de la DGM, TDL
|
|
Bhargava et al., 2013 [851]
|
518
|
3 meses
|
EPA 650 mg + DHA 350 mg
|
Placebo (aceite de trigo)
|
1
|
Síntomas, TDL y puntuación Schirmer
|
Tinción rosa bengala y citología de impresión conjuntival
|
|
Olenik et al., 2013 [852]
|
61b
|
3 meses
|
EPA 127,5 mg + DHA 1050 mgc
|
Placeboc (aceite de girasol)
|
1
|
Síntomas (IESO), TDL, inflamación del margen del párpado, expresión de la GM y puntuación Schirmer
|
Ninguno
|
|
Kawakita et al., 2013 [853]
|
27
|
12 semanas
|
EPA 1245 mg + DHA 540 mg
|
Placebo (triglicéridos de cadena media)
|
1
|
Síntomas y TDL
|
Puntuación Schirmer, tinción de la superficie ocular con fluoresceína o rosa bengala
|
|
Kangari et al., 2013 [854]
|
64
|
30 días
|
EPA 360 mg + DHA 240 mg
|
Placebo (triglicéridos de cadena media)
|
1
|
Principal: TDL
Secundario: Síntomas (IESO) y puntuación Schirmer
|
Ninguno
|
|
Pinazo-Duran et al., 2013 [855]
|
66d
|
3 meses
|
EPA 85 mg + DHA 700 mg + 60 mg DPA + antioxidante
|
Ninguno (abierto)
|
2
|
No aplicable
|
Reducción de las citocinas lagrimales inflamatorias (solo con respecto al inicio)
|
|
Olenik, 2014 [856]
|
905
|
12 semanas
|
EPA 127,5 mg + DHA 1050 mg + DPA 90 mg
|
Ninguno (abierto)
|
2
|
No aplicable
|
Síntomasa (solo con respecto al inicio)
|
|
Bhargava, 2015 [857]
|
256
|
45 días
|
EPA 720 mg + DHA 480 mg
|
Placebo (aceite de oliva)
|
1
|
Principal: Síntomas.
Secundario: TDL y citología conjuntival
|
Secundario: Puntuación de Schirmer
|
|
Deinema et al., 2017 [858]
|
60
|
90 días
|
Aceite de krill (EPA 945 mg + DHA 510 mg) y aceite de pescado (EPA 1000 mg + DHA 500 mg)
|
Placebo (aceite de oliva)
|
1
|
Principal: Osmolaridad lagrimal y síntomas (IESO). Secundario: TDL, enrojecimiento balbular ocular, niveles lagrimales de la citocina proinflamatoria IL-17A.
|
Secundario: TDNI, puntuación Schirmer, ML, niveles de otras citocinas lagrimales IL-2, IL-4, IL-6, IL-10, IFN-gamma, TNF-alfa.
|
|
Epitropoulos et al., 2016 [859]
|
105
|
12 semanas
|
EPA 1680 mg + DHA 560 mg AGE ω-3 reesterificados
|
Aceite de cártamo (3136 mg)
|
1
|
Principal: Osmolaridad lagrimal. Secundario: TDL, síntomas (IESO), positividad de MMP-9.
|
Secundario: Tinción corneal con fluoresceína, prueba de Schrimer.
|
|
ADH = ácido docosahexaenoico; ADP = ácido docosapentaenoico; AEP = ácido eicosapentaenoico; IFN = interferón; IL = interleucina; GM = glándula de Meibomio; MMP-9 = matriz metaloproteinasa-9; N = número de sujetos; TDLNI = tiempo de desintegración lagrimal no invasivo; IESO = índice de enfermedad de la superficie ocular; TDL = tiempo de desintegración lagrimal; AML = altura del menisco lagrimal; TNF = factor de necrosis tumoral (tumor necrosis factor).
- No se evaluaron mediciones clínicas objetivas.
- La población del estudio incluyó solo a personas con DGM.
- Los grupos de intervención y de control recibieron instrucciones de realizar también trabajos de higiene del párpado, así como de utilizar lágrimas artificiales sin conservantes a diario durante todo el estudio.
- La población del estudio incluyó tanto a personas con EOS (n = 30) como a controles sanos (n = 36).
- Estudio piloto aleatorizado, controlado y con doble enmascaramiento que tenía una potencia inadecuada para detectar diferencias significativas entre los grupos del estudio.
- La población del estudio implicaba a personas con DGM y blefaritis.
- Los resultados principal y secundario se especifican cuando los autores los definen.
|
Tabla 14
Principales ensayos clínicos intervencionistas publicados de suplementación oral combinada de AGE ω-3 y ω-6 para la enfermedad del ojo seco.
|
Autor, año
|
N
|
Periodo del estudio
|
Intervención oral ω-6 (dosis diaria)
|
Control
|
Nivel de evidencia
|
Parámetros con mejoras significativas con respecto al controla
|
Parámetros sin efecto significativo con respecto al controla
|
|
Creuzot et al., 2006 [873]
|
71
|
6 meses
|
AEP 28 mg + ADH 392 mg + AGL 82 mg + AL 126 mg
|
Placebo (ácido oleico básico)
|
1b
|
Lagrimeo reflejo e hiperemia bulbar
|
Puntuación Schirmer, TDL, tinción de la superficie ocular con ?uoresceína y verde de lisamina
|
|
Larmo et al., 2010 [874]
|
86c
|
3 meses
|
Aceite de espino amarillo (2 g): AGE ω-3 de cadena larga 149 mg + ω-6 245 mg
|
Placebo (triglicéridos de cadena media)
|
1
|
Enrojecimiento bulbar y quemazón ocular
|
Osmolaridad lagrimal, puntuación de Schirmer, TDL
|
|
Brignole- Baudouin et al., 2011 [875]
|
106
|
3 meses
|
AEP 427,5 mg + ADH 285 mg + aceite de borraja 15 mg + zinc 10 mg + vitaminas
|
Placebo (triglicéridos de cadena media)
|
1
|
Reducción del porcentaje de células conjuntivales positivas para HLA-DR.
|
Puntuación Schirmer, TDL y tinción de la superficie ocular
|
|
Jackson et al., 2011 [876]
|
43
|
6 meses
|
AAL 1000 mg + AGL 500 mg
|
AAL 1000 mg + AGL 500 mg + ciclosporina tópica 2×día durante los últimos 3 meses
|
2d
|
No aplicable
|
Ambos grupos mostraron mejoras en los síntomas y del TDL solo con respecto al inicio
|
|
Creuzot- Garcher et al., 2011 [877]
|
181
|
6 meses
|
AEP 28 mg + ADH 392 mg + AGL 82 mg + AL 126 mg
|
Placebo (ácido oleico básico)
|
1
|
TDL, reducción de la puntuación de fatiga ocular
|
Puntuación Schirmer, tinción de la superficie ocular.
|
|
Sheppard et al., 2013 [878]
|
38e
|
6 meses
|
AAL 196 mg + AEP 128 mg + ADH 99 mg + ADP 39 mg + AL 710 mg + AGL 240 mg
|
Placebo (aceite de girasol)
|
1
|
Síntomas (IESO), índice de asimetría de la superficie corneal y expresión conjuntival de HLA-DR
|
TDL, tinción conjuntival con ?uoresceína y verde de lisamina, puntuación Schirmer.
|
|
AAL = ácido alfa linolénico; ADH = ácido docosahexaenoico; ADP = ácido docosapentaenoico; AGE = ácidos grasos esenciales; AEP = ácido eicosapentaenoico; AGL = ácido gamma-linolénico; HLA-DR = antígeno leucocitario humano relacionado con D (human leukocyte antigen D-related); AL = ácido linolénico; IESO = índice de la enfermedad de la superficie ocular; N = número de sujetos; TDL = tiempo de desintegración lagrimal.
- Los resultados principal y secundario se especifican cuando los autores los definen.
- Los procedimientos de enmascaramiento no están claros.
- Los grupos de intervención y de control incluían a usuarios de lentes de contacto.
- No hubo enmascaramiento ni para los evaluadores de los resultados clínicos ni para los participantes (estudio abierto).
- La población del estudio incluyó únicamente a mujeres menopáusicas.
|
Tabla 15
Principales ensayos clínicos intervencionistas publicados de suplementación oral con AGE ω-6 para la enfermedad del ojo seco.
|
Autor, año
|
N
|
Periodo del estudio
|
Intervención oral ω-6 (dosis diaria)
|
Control
|
Nivel de evidencia
|
Parámetros con mejoras significativas con respecto al controlf
|
Parámetros sin efecto significativo con respecto al controlf
|
|
Manthorpe et al., 1984 [867]
|
36c
|
3 semanas
|
ácido cis-linoleico 365 mg + GLA 45 mg
|
Placebo
|
1
|
Puntuación en la prueba Schirmer
|
TFL, tinción con verde de lisamina, sensibilidad corneal y lisozima lagrimal
|
|
Oxholm et al., 1986 [868]
|
28c
|
8 semanas
|
ácido cis-linoleico 2190 mg + GLA 270 mg
|
Placebo
|
1
|
Ninguno
|
Sin mejoras en la puntuación Schirmer, el TDL o la tinción con verde de lisamina
|
|
Theander et al., 2002 [869]
|
90c
|
6 meses
|
Dos dosis probadas: (1) GLA 800 mg; (2) GLA 1600 mg
|
Placebo (aceite de trigo)
|
1
|
Ninguna.
|
Sin mejoras con ninguna de las dosis en el dolor de ojos, los síntomas de ojo seco, la prueba de Schirmer o la tinción verde de lisamina
|
|
Barabino et al., 2003 [872]
|
26d
|
45 días
|
LA 57 mg + GLA 30 mge
|
Placeboe
|
1
|
Síntomas, reducción de la expresión conjuntival de HLA-DR y tinción con verde de lisamina.
|
TDL, puntuación en la prueba Schirmer
|
|
Aragona et al., 2005 [870]
|
40c
|
1 mes
|
LA 112 mg + GLA 15 mg
|
Placebo (fructosa)
|
1
|
Síntomas, niveles aumentados de lágrima PGE1 y TCF
|
TDL, secreción basal de lágrima
|
|
Pinna et al., 2007 [871]
|
57a
|
6 meses
|
LA 28,5 mg + GLA 15 mg
|
Ninguno
|
2b
|
No aplicable
|
Síntomas, turbidez en la secreción de la GM y obstrucción de la GM (solo respecto al inicio)
|
|
TCF = tinción corneal con ?uoresceína; AGL = ácido gamma-linolénico; HLA-DR = antígeno leucocitario humano relacionado con D (human leukocyte antigen D-related); AL = ácido linolénico; N = número de sujetos; PGE1 = prostaglandina E1; TDL = tiempo de desintegración lagrimal.
- La población del estudio incluyó solo a personas con DGM.
- Solo con enmascaramiento para el investigador.
- La población del estudio incluyó solo a personas con síndrome de Sjögren primario.
- La población del estudio incluyó solo a personas con EOS con déficit acuoso.
- Los grupos de intervención y de control recibieron instrucciones de utilizar lágrimas artificiales sin conservantes a diario durante todo el estudio.
- Los resultados principal y secundario se especifican cuando los autores los definen.
|
Tabla 16
Recomendaciones de gestión y tratamiento graduales para la enfermedad del ojo secoa,b,c.
|
Paso 1:
- Formación acerca de la afección, su gestión, tratamiento y pronóstico
- Modificación del entorno local
- Formación sobre posibles modificaciones de la dieta (incluida la suplementación oral de ácidos grasos esenciales)
- Identificación y posible modificación/eliminación de medicamentos sistémicos y tópicos perjudiciales
- Lubricantes oculares de distintos tipos (si hay presencia de DGM, se deben considerar los suplementos con contenido lipídico)
- Higiene del párpado y compresas de calor de distintos tipos
Paso 2:
Si las opciones anteriores son inadecuadas, considere:
- Lubricantes oculares sin conservantes para minimizar la toxicidad inducida por los conservantes
- Tratamiento con aceite del árbol del té para Demodex (si hubiera)
- Conservación de las lágrimas
- Oclusión del conducto lagrimal
- Gafas con cámara de humedad
- Tratamientos nocturnos (como pomada o dispositivos de cámara de humedad)
- Calentamiento físico en la consulta y expresión de las glándulas de Meibomio (incluidos tratamientos asistidos con dispositivo, como LipiFlow)
- Tratamiento con luz pulsada intensa en la consulta para la DGM
- Fármacos con receta para gestionar la EOSd
- Antibióticos tópicos o combinación de antibióticos/esteroides aplicados en los márgenes de los párpados para blefaritis anterior (si hubiera)
- Corticosteroide tópico (duración limitada)
- Secretagogos tópicos
- Fármacos inmunomoduladores no glucocorticoides tópicos (como la ciclosporina)
- Fármacos tópicos antagonistas de LFA-1 (como li?tegrast)
- Macrólido oral o antibióticos con tetraciclina
Paso 3:
Si las opciones anteriores son inadecuadas, considere:
- Secretatogos orales
- Colirios de suero autólogos/alogénicos
- Opciones de lentes de contacto terapéuticas
- Lentes blandas de vendaje
- Lentes esclerales rígidas
Paso 4:
Si las opciones anteriores son inadecuadas, considere:
- Corticosteroide tópico para mayor duración
- Injertos de membrana amniótica
- Oclusión quirúrgica de los conductos lagrimales
- Otros enfoques quirúrgicos (p. ej., tarsorrafía, trasplante de glándula salival)
|
DGM = disfunción de la glándula de Meibomio; EOS = enfermedad del ojo seco.